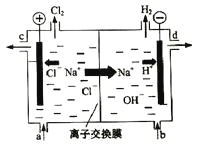
-
已知:HCN(aq)与NaOH(aq)反应的△H=-l2.1kJ/mol;HCl(aq)与NaOH(aq)反应的△H=-55.6kJ/mol,则HCN 在水溶液中电离的△H等于
A. -67.7kJ/mol B. -43.5 kJ/mol C. +43.5 kJ/mol D. +67.7 kJ/mol
难度: 简单查看答案及解析
-
根据以下两幅图,可判断出下列离子方程式中错误的是( )
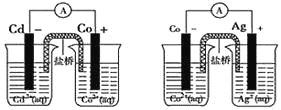
A. 2Ag(s)+Cd2+(aq)=2Ag+(aq)+Cd(s)
B. Co2+(aq)+Cd(s)=Co(s)+Cd2+(aq)
C. 2Ag+(aq)+Cd(s)=2Ag(s)+Cd2+(aq)
D. 2Ag+(aq)+Co(s)=2Ag(s)+Co2+(aq)
难度: 困难查看答案及解析
-
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:①NH4I(s)
NH3(g)+HI(g) ②2HI(g)
H2(g)+I2(g) 达到平衡时,c(H2)=0.5 mol·L-1,c(HI)=4 mol·L-1,,则此温度下反应①的平衡常数为
A. 9 B. 16 C. 20 D. 25
难度: 中等查看答案及解析
-
3-甲基戊烷的一氯代产物有(不考虑立体异构)( )
A. 3种 B. 4种 C. 5种 D. 6种
难度: 简单查看答案及解析
-
将氢氧化钠稀溶液滴加到醋酸稀溶液中,下列各图示意混合溶液有关量或性质的变化趋势,其中错误的是
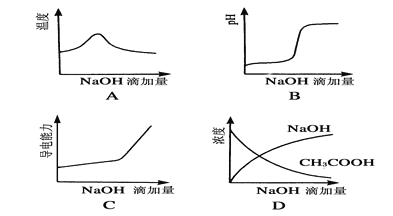
难度: 中等查看答案及解析
-
下列化合物中既能使溴的四氯化碳溶液褪色,又能在光照下与溴发生取代反应的是
A. 甲苯 B. 乙醇 C. 丙烯 D. 乙烯
难度: 中等查看答案及解析
-
微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是

A. 正极反应中有CO2生成 B. 微生物促进了反应中电子的转移
C. 质子通过交换膜从负极区移向正极区 D. 电池总反应为C6H12O6+6O2═6CO2+6H2O
难度: 简单查看答案及解析
-
下列各组中的物质均能发生加成反应的是
A. 乙烯和乙醇 B. 苯和氯乙烯 C. 乙酸和溴乙烷 D. 丙烯和丙烷
难度: 简单查看答案及解析
-
Mg—AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是
A. 负极反应式为Mg-2e-=Mg2+
B. 正极反应式为Ag++e-=Ag
C. 电池放电时Cl-由正极向负极迁移
D. 负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑
难度: 简单查看答案及解析
-
一定温度下,下列溶液的离子浓度关系式正确的是( )
A. pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5mol·L-1
B. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C. pH=2的乙二酸(H2C2O4)溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)
D. pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
难度: 中等查看答案及解析
-
下列反应中,属于取代反应的是
①CH3CH=CH2+Br2
CH3CHBrCH2Br
②CH3CH2OH
CH2=CH2+H2O
③CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O ④ CH3Cl+Cl2→CH2Cl2+HCl
A. ①② B. ③④ C. ①③ D. ②④
难度: 简单查看答案及解析
-
已知异丙苯的结构简式如下,下列说法错误的是
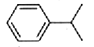
A. 异丙苯的分子式为C9H12
B. 异丙苯的沸点比苯高
C. 异丙苯中碳原子可能都处于同一平面
D. 异丙苯和苯为同系物
难度: 中等查看答案及解析
-
羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g)
COS(g)+H2(g) K=0.1。 反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是( )
A. 升高温度,H2S浓度增加,表明该反应是吸热反应
B. 通入CO后,正反应速率逐渐增大
C. 反应前H2S物质的量为7mol
D. CO的平衡转化率为80%
难度: 简单查看答案及解析
-
某有机物的结构简式如图所示,其名称正确的是( )
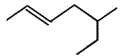
A. 5-乙基-2-己烯
B. 3-甲基庚烯
C. 3-甲基-5-庚烯
D. 5-甲基-2-庚烯
难度: 中等查看答案及解析
-
下列在制定溶液中的各组离子,一定能够大量共存的是
A. 无色溶液中:CO32-、Al3+、Cl-、NO3-
B. 无色溶液中:NH4+、K+、CH3COO-、Cl-
C. pH=l的溶液中:Fe2+、NH4+、Mg2+、NO3-
D. 水电离的c(H+)=10-12mol/L 的溶液中:Fe3+、SO42-、K+、Na+
难度: 中等查看答案及解析
-
下列说法正确的是
A. 将AlCl3溶液和Na2SO3溶液加热蒸干并灼烧可分别得到Al2O3、Na2SO3
B. 在溶液的稀释过程中,离子浓度有的可能增大,有的可能减小,有的可能不变
C. A1露置在空气中会形成致密的氧化膜,Fe露置在空气中也会形成致密的氧化膜
D. 反应为Cu+2AgNO3=Cu(NO3)2+2Ag的原电池装置中,盐桥中通常装有含琼胶的KCl饱和溶液
难度: 中等查看答案及解析
-
某单烯烃与H2加成后的产物是
 则该烯烃的结构式可能有
则该烯烃的结构式可能有A. 4种 B. 5种 C. 6种 D. 7种
难度: 中等查看答案及解析
-
下列说法正确的是
A. 植物油氢化过程中发生了加成反应
B. 淀粉和纤维素互为同分异构体
C. 环己烷与苯可用酸性KMnO4溶液鉴别
D. 水可以用来分离溴苯和苯的混合物
难度: 中等查看答案及解析
-
由下列实验及现象不能推出相应结论的是
实验
现象
结论
A
向2mL0.1mol·L-1的FeCl3溶液中加足量铁粉,振荡,加1滴KSCN溶液
黄色逐期消失,加KSCN溶液颜色不变
还原性:Fe>Fe2+
B
将金属钠在燃烧匙中点燃,迅速伸入集满CO2的集气瓶
集气瓶中产生大量白烟,瓶内有黑色颗粒产生
CO2具有氧化性
C
加热盛有少NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸
石蕊试纸变蓝
NH4HCO3显碱性
D
向2支盛有2mL相同浓度银氨溶液的试管中分别加入2滴相同浓度的NaCl和NaI溶液
一只试管中产生黄色沉淀,另一支中无明显现象
Ksp(AgI)<Ksp(AgCl)
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
两种气态烃组成的混合气体0.1mol,完全燃烧得0.15mol CO2和3.6g H2O,下列关于该混合气体的说法正确的是
A. 一定有乙烯 B. 一定没有乙烯
C. 一定有甲烷 D. 可能有乙烷
难度: 中等查看答案及解析
-
在一定温度下,将气体X 和气体Y 各0.16mol 充入10L 恒容密闭容器中,发生反应X(g) +Y (g)
2Z (g) △H<0,一段时间后达到平衡,反应过程中测定的数据如下表,下列说法正确的是
t/min
2
4
7
9
(Y)/mol
0.12
0.11
0.10
0.10
A. 应前2min 的平均速率v(Z)=2.0x10-3mol(L·min)
B. 其他条件不变,降低温度,反应达到新平衡前v (逆) >v (正)
C. 该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
难度: 中等查看答案及解析