-
水煤气是一种高效气体燃料,其主要成分是CO和H2,可用水蒸气通过炽热的炭制得:C(s)+H2O(g)
CO(g)+H2(g)△H=+131kJ•mol-1
(1)某温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示.请填写表中相应的空格.
(2)另有一个容积可变的密闭容器.恒温恒压下,向其中加入1.0mol炭和1.0mol水蒸气 (H2O),发生上述反应,达到平衡时,容器的体积变为原来的1.25 倍.平衡时水蒸气的转化率为______;向该容器中补充 a mol 炭,水蒸气的转化率将______(填“增大”、“减小”、“不变”).容器
编号c(H2O)
/mol•L-1c(CO)
/mol•L-1c(H2)
/mol•L-1v正、v逆比较 I 0.06 0.60 0.10 v正=v逆 II 0.06 0.50 0.40 ① III 0.12 0.40 0.80 v正<v逆 IV 0.12 0.30 ② v正=v逆
(3)在一定条件下用水煤气能合成甲醇:CO(g)+2H2(g)CH3OH(g) 据研究,给合成甲醇反应体系中通入少量CO2有利于维持催化剂Cu2O的量不变,原因是(用化学方程式表示)______.
(4)熔融盐燃料电池具有高的发电效率,该电池用Li2CO3和Na2CO3的熔融盐混合物作电解质,其中一极通入CO,另一极通入空气和CO2的混合气体.根据上述信息,该燃料电池:负极反应式为______;正极反应式为______.难度: 中等查看答案及解析
-
I.已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数分别为:
醋酸 K=1.75×10-5
碳酸 K1=4.30×10-7 K2=5.61×10-11
亚硫酸 K1=1.54×10-2 K2=1.02×10-7
(1)写出碳酸的第一级电离平衡常数表达式:K1=______.
(2)在相同条件下,试比较CH3COONa、Na2CO3和Na2SO3水溶液的碱性强弱:______>______>______.
(3)在相同条件下,试比较同浓度同体积H2SO3、NaHSO3和Na2SO3溶液中粒子的数目:______>______>______.
(4)若保持温度不变,在醋酸溶液中加入少量盐酸,下列量会变小的是______(填序号).
A.c(CH3COO-) B.c(H+) C.醋酸电离平衡常数 D.醋酸的电离程度
II.某化工厂废水中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01mol•L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
(5)你认为往废水中投入______(填字母序号),沉淀效果最好.难溶电解质 AgI AgOH Ag2S PbI2 Pb(OH)2 PbS KSP 8.3×10-17 5.6×10-8 6.3×10-50 7.1×10-9 1.2×10-15 3.4×10-28
A.NaOH B.Na2S C. KI D.Ca(OH)2
(6)如果用食盐处理其只含Ag+的废水,测得处理后的废水中NaCl的质量分数为0.117%.若环境要求排放标准为c(Ag+)低于1.0×10-8mol•L-1,问该工厂处理后的废水中c(Ag+)=______[已知:Ksp(AgCl)=c(Ag+)•c(Cl-)=1.8×10-10mol2•L-2].难度: 中等查看答案及解析
-
研究发现某些金属离子如Fe3+、Cu2+等对H2O2的分解也具有催化作用,为了比较MnO2与Fe3+和Cu2+的催化效果,某同学设计了如图甲、乙所示的实验.请回答相关问题:
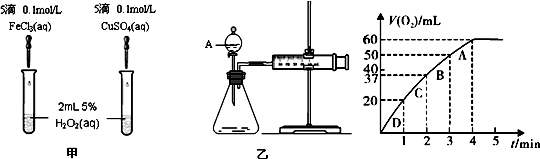
(1)定性分析:图甲可通过观察______,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3或者将CuSO4改为CuCl2更为合理,其理由是______.
(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略.检查乙装置气密性的方法是______,实验中需要测量的数据是______.
(3)加入0.10mol MnO2粉末于50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示.
①写出H2O2在二氧化锰作用下发生反应的化学方程式______ 2H2O+O2↑难度: 中等查看答案及解析
-
CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.
已知:①CuCl可以由CuCl2用适当的还原剂如SO2、SnCl2等还原制得:2Cu2++2Cl-+SO2+2H2O2CuCl↓+4H++SO42-
2CuCl2+SnCl2═2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子: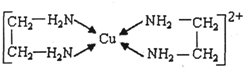
请回答下列问题:
(1)基态Cu原子的核外电子排布式为______,H、N、O三种元素的电负性由大到小的顺序是______.
(2)SO2分子的空间构型为______,与SnCl4互为等电子体的一种离子的化学式为______.
(3)乙二胺分子中氮原子轨道的杂化类型为______,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是______.
(4)②中所形成的配离子中含有的化学键类型有______.a.配位键 b.极性键 c.离子键 d.非极性键
(5)CuCl的晶胞结构如下图所示,其中Cl原子的配位数为______.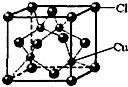
难度: 中等查看答案及解析
-
[化学-选修有机化学基础]
Ⅰ.对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛.结构简式如图(1)该有机物的分子式为______,其中含氧官能团的名称是______.
(2)该有机物能发生的反应类型是(填写代号)______.
A.氧化反应 B.消去反应 C.加聚反应 D.水解反应
一定条件下,1mol该有机物与H2完全加成时,最多需要______mol H2.
Ⅱ.芳香族化合物C10H10O2有如下的转化关系: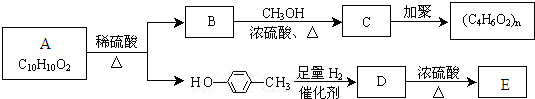
已知E能使Br2/CCl4溶液褪色.请回答下列问题:
(3)请分别写出A、E的结构简式:A______、E______.
(4)若有机物F与C互为同分异构体,则与有机物B互为同系物的F的同分异构体有______ 种.
(5)请写出B→C反应的化学方程式:______难度: 中等查看答案及解析