-
对于化学反应3W(g)+2X(g)=4Y(g)+3Z(g),下列反应速率关系中,正确的是( )
A.v(W)=3v(Z)
B.2v(X)=3v(Z)
C.2v(X)=v(Y)
D.3v(W)=2v(X)难度: 中等查看答案及解析
-
短周期元素X、Y、Z所在的周期序数依次增大,它们的原子序数之和为20,且Y2-与Z+核外电子层的结构相同.下列化合物中同时存在极性和非极性共价键的是( )
A.Z2Y
B.X2Y2
C.Z2Y2
D.ZYX难度: 中等查看答案及解析
-
下列有机物中既能发生取代反应,也可发生加成反应,还能使酸性高锰酸钾溶液褪色的是( )
A.乙烷
B.乙醇
C.甲苯
D.乙烯难度: 中等查看答案及解析
-
1molCH2=CH2先与Cl2完全加成,再与Cl2发生取代反应,最后生成六氯代烷.整个过程中,参加反应的Cl2物质的量是( )
A.1mol
B.3mol
C.4mol
D.5mol难度: 中等查看答案及解析
-
已知:①A+B2+=A2++B,②D+2H2O=D(OH)2+H2↑,③以B、E为电极与E的盐溶液组成原电池,电极反应为:E2++2e-=E,B-2e-=B2+.则A2+、B2+、D2+、E2+的氧化性强弱关系是( )
A.D2+>A2+>B2+>E2+
B.E2+>B2+>A2+>D2+
C.D2+>E2+>A2+>B2+
D.A2+>B2+>D2+>E2+难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列叙述中错误的是( )
A.标准状况下,22.4LCH4与18gH2O所含有的电子数均为10NA
B.室温下,21.0g乙烯和丁烯的混合气体含有的碳原子数目为1.5NA
C.等物质的量的甲基(-CH3)与羟基(-OH)所含电子数相等
D.1mol乙烷含有的共价键数目为8NA难度: 中等查看答案及解析
-
在通常条件下,下列各组物质的性质排列正确的是( )
A.热稳定性:HF>H2O>NH3
B.水溶性:HCl>SO2>NH3
C.沸点:乙烷>戊烷>丁烷
D.酸性:H2SO4>H3PO4>HClO4难度: 中等查看答案及解析
-
在一定温度、压强下,向100mLCH4和Ar的混合气体中通入400mLO2,点燃使其完全燃烧,最后在相同条件下得到干燥气体460mL,则反应前混合气体中CH4和Ar物质的量之比是( )
A.1:4
B.1:3
C.1:2
D.1:1难度: 中等查看答案及解析
-
能用于鉴别淀粉、肥皂和蛋白质三种溶液的一种试剂是( )
A.碘水
B.浓硝酸
C.NaOH溶液
D.MgSO4溶液难度: 中等查看答案及解析
-
检验酒精中是否含有少量水,应选用的试剂是( )
A.无水氯化钙
B.金属钠
C.无水硫酸铜
D.生石灰难度: 中等查看答案及解析
-
下列说法正确的是( )
A.16O与18O是氧元素的两种不同核素
B.16O2与18O2互为同分异构体
C.16O与18O核外电子排布方式不同
D.通过化学变化可实现16O与18O间的相互转化难度: 中等查看答案及解析
-
下列实验中,不能观察到明显变化的是( )
A.把绿豆大的钾投入少量水中
B.把一段打磨过的镁带放入少量冷水中
C.把溴水加入到淀粉KI溶液中
D.氢气和氯气等体积混合后强光照射难度: 中等查看答案及解析
-
下列装置中,明显有电流产生的是( )
A.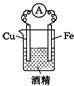
B.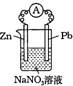
C.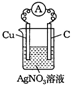
D.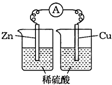
难度: 中等查看答案及解析
-
含有非极性键且分子中各原子都满足8电子稳定结构的是( )
A.CH4
B.CO2
C.BeCl2
D.N2难度: 中等查看答案及解析
-
下列关于核糖(CH2OH-CHOH-CHOH-CHOH-CHO)的叙述中正确的是( )
A.与葡萄糖互为同分异构体
B.可与银氨溶液作用形成银镜
C.可使紫色石蕊试液变红
D.常温下遇碘变蓝难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.生成物总能量一定低于反应物总能量
B.放热反应速率总是大于吸热反应速率
C.形成离子键的阴、阳离子间只存在静电吸引力
D.元素周期律是元素原子核外电子排布周期性变化的结果难度: 中等查看答案及解析
-
取5.06g 由等物质的量的NaBr和NaI组成的混合物样品溶于水,然后通入224mL(标准状况下)Cl2充分反应,则被氧化的Br-的物质的量是( )
A.0
B.0.01mol
C.0.02mol
D.0.04mol难度: 中等查看答案及解析
-
下列叙述中错误的是( )
A.油脂和蛋白质都是能发生水解反应的高分子化合物
B.一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应
C.乙醇、乙酸和乙酸乙酯能用饱和碳酸钠溶液鉴别
D.加热时,乙醇在Ag催化下可被O2氧化为乙醛难度: 中等查看答案及解析
-
下列化合物分子中的所有原子都处于同一平面的是( )
A.甲苯
B.丙烯
C.氯乙烯
D.乙醇难度: 中等查看答案及解析
-
某温度下,浓度都是1mol/L的两种气体X2和Y2,在密闭容器中反应生成Z,反应2min后,测得参加反应的X2为0.6mol/L,用Y2变化表示的反应速率v(Y2)=0.1mol/(L⋅min),生成的c(Z)=0.4mol/L,则该反应方程式为( )
A.X2+2Y2⇌2XY2
B.2X2+Y2⇌2X2Y
C.3X2+Y2⇌2X3Y
D.X2+3Y2⇌2XY3难度: 中等查看答案及解析
-
下列关于化学反应限度的叙述中正确的是( )
A.改变外界条件不能改变化学反应的限度
B.当某反应在一定条件下达到反应限度时即达到了化学平衡状态
C.当某反应体系中气体压强不再改变时,该反应一定达到反应限度
D.当某反应达到限度时,反应物和生成物的浓度一定相等难度: 中等查看答案及解析
-
亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理是:Li2NH+H2=LiNH2+LiH.下列叙述中正确的是( )
A.此法储氢和钢瓶储氢原理相同
B.Li+和H+的离子半径相等
C.该反应中H2既是氧化剂又是还原剂
D.金属锂在空气中燃烧生成Li2O2难度: 中等查看答案及解析
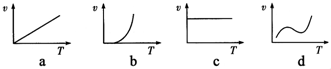

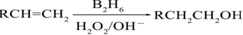 (B2H6为乙硼烷)
(B2H6为乙硼烷)