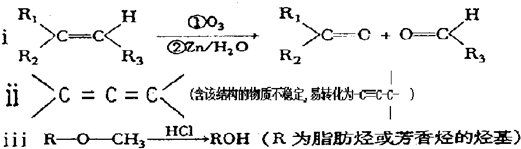
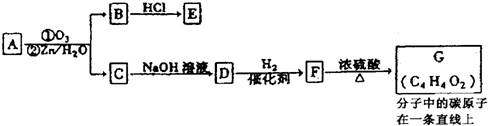
-
下列关于电解质溶液的正确判断是( )
A.在pH=12的溶液中,K+、Cl-、HCO3-、Na+可以常量共存
B.在pH=0的溶液中,Na+、NO3-、SO32-、K+可以常量共存
C.由0.1mol•L-1一元碱BOH溶液的pH=10,可推知BOH溶液存在BOH=B++OH-
D.由0.1mol•L-1一元碱HA溶液的pH=3,可推知NaA溶液存在A-+H2O⇋HA+OH-难度: 中等查看答案及解析
-
下列说法正确的是( )
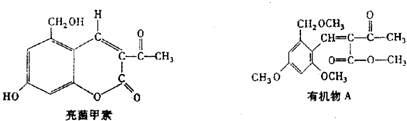
A.HCHO溶液、(NH4)2SO4溶液均能使蛋白质变性
B.能与NaOH溶液反应且分子式为C2H4O2的有机物不一定是羧酸
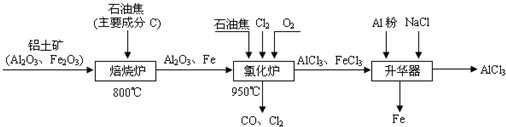
C.煤的干馏是物理变化,煤的气化和液化是化学变化
D.纤维素、蛋白质、油脂、葡萄糖在一定条件下都能发生水解反应难度: 中等查看答案及解析
-
氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是( )
A.再通入少量氯气,减小
B.通入少量SO2,溶液漂白性增强
C.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-)
D.加入少量固体NaOH,溶液的pH会略微增大难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
A.在标准状况下,V升SO3含氧原子个数是3VNA/22.4
B.常温常压下,1mol重水所含电子总数为10NA
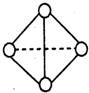
C.金刚石中,碳原子数与碳碳共价键数之比为1:2
D.常温常压下,NA个甲烷分子体积大于22.4L难度: 中等查看答案及解析
-
化学中常用图象直观地描述化学反应的进程或结果.下列图象描述正确的是( )
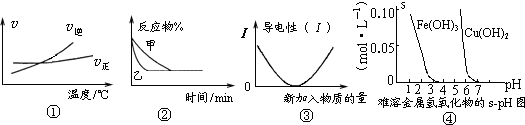
A.根据图①可判断可逆反应“A2(g)+3B2(g)⇌2AB3(g)”的△H>0
B.图②表示压强对可逆反应2A(g)+2B(g)⇌3C(g)+D(s)的影响,乙的压强大
C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D.根据图④,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO,至pH在4左右难度: 中等查看答案及解析
-
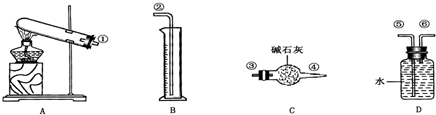
绿色:环境保护也是我们的生活理念.下列实验符合“绿色环保”思想的是( )
A.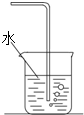
氯气溶于水制氯水
B.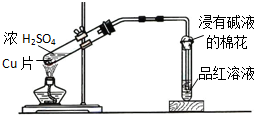
铜与浓硫酸反应
C.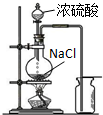
实验室制备并收集氯化氢气体
D.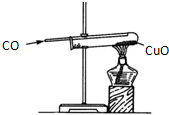
一氧化碳还原氧化铜难度: 中等查看答案及解析
-
有关下列装置图的说法正确的是( )
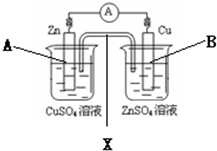
A.若X是盐桥,则上述装置可以形成原电池
B.若X是铜条,则上述装置不发生任何反应
C.若X是铜条,上述装置中,B电极是阴极
D.若X是铜条,上述装置中,A电极的电极反应式是:Cu2++2e-=Cu难度: 中等查看答案及解析