-
某阳离子Mn+的核外共有x个电子,核内有a个中子,则M的质量数为
A. a+x-n B. a+x+n
C. a-x-n D. a-x+n
难度: 中等查看答案及解析
-
元素X、Y和Z可结合形成化合物XYZ3;X、Y和Z的原子序数之和为26;Y和Z在同一周期.下列有关推测正确的是()
A. XYZ3是一种可溶于水的酸,且X与Y可形成共价化合物XY
B. XYZ3是一种微溶于水的盐,且X与Z可形成离子化合物XZ
C. XYZ3是一种易溶于水的盐,且Y与Z可形成离子化合物YZ
D. XYZ3是一种离子化合物,且Y与Z可形成离子化合物YZ3
难度: 中等查看答案及解析
-
已知同周期X、Y、Z三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为HXO4>H2YO4>H3ZO4,则下列判断中正确的是
A. 元素非金属性技X、Y、Z的顺序减弱
B. 阴离子的还原性按X、Y、Z的顺序减弱
C. 气态氢化物的稳定性按X、Y、Z的顺序增强
D. 单质的氧化性按X、Y、Z的顺序增强
难度: 简单查看答案及解析
-
含硒(Se) 的保健品已开始进入市场。已知硒与氧、硫同主族,与溴同周期,则下列关于硒的叙述中,正确的是
A. 非金属性比硫强 B. 氢化物比HBr稳定
C. 原子序数为34 D. 最高价氧化物的水化物显碱性
难度: 中等查看答案及解析
-
甲、乙是周期表中相邻同主族的两种元素,若甲的原子序数为x,则乙的原子序数不可能是
A. x+2 B. x +4 C. x+8 D. x+18
难度: 中等查看答案及解析
-
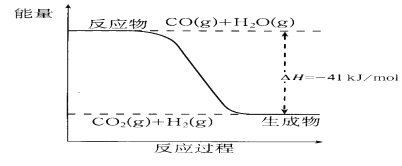
已知反应X+Y=M+N为吸热反应,对这个反应的下列说法中正确的是( )
A. X的能量一定低于M的,Y的能量一定低于N的
B. 因为该反应为吸热反应,故一定要加热反应才能进行
C. 破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
D. X和Y的总能量一定低于M和N的总能量
难度: 简单查看答案及解析
-
一些科学家预言,存在稳定的超重元素,如:Z=114,N=184的原子,它位于元素周期表的第7周期,第ⅣA族,下列说法正确的是( )
A. 第七周期有50种元素 B. 该原子的质量数为184
C. 该元素的相对原子质量为298 D. 该原子核外有114个电子
难度: 中等查看答案及解析
-
铋(Bi)在医药方面有重要应用。下列关于
和
的说法正确的是( )
A.
和
都含有83个中子
B.
和
互为同位素
C.
和
的核外电子数不同
D.
和
分别含有126和127个质子
难度: 简单查看答案及解析
-
下列物质中既含有离子键又含有非极性共价键的是( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
下列排列顺序错误的是( )
A. 酸性

B. 碱性

C. 氢化物的稳定性

D. 原子半径
难度: 简单查看答案及解析
-
X、Y是元素周期表中第ⅦA族的两种元素。下列叙述中能说明X的非金属性比Y强的是:
A. X原子的电子层数比Y原子的电子层数多
B. X的氢化物的沸点比Y的氢化物的沸点低
C. X的气态氢化物比Y的气态氢化物稳定
D. Y的单质能将X从NaX溶液中置换出来
难度: 中等查看答案及解析
-
下列既属于氧化还原反应,又属于吸热反应的是( )
A. 铝片与稀盐酸反应
B.
与
的反应
C. 灼热的碳与水蒸气的反应
D. 铝热反应
难度: 简单查看答案及解析
-
石墨烯是由碳原子构成的单层片状结构的新材料(结构示意图如下),可由石墨剥离而成,具有极好的应用前景。下列说法正确的是
A.石墨烯与石墨互为同位素
B.0.12g石墨烯中含有6.02×1022个碳原子
C.石墨烯是一种有机化合物
D.石墨烯中的碳原子间以共价键结合
难度: 中等查看答案及解析
-
下列关于元素周期表和元素周期律的说法错误的是( )
A. Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多
B. 第二周期元素从Li到F,非金属性逐渐增强
C. 因为Na比K容易失去电子,所以Na比K的还原性强
D. O与S为同主族元素,且O比S的非金属性强
难度: 简单查看答案及解析
-
下列叙述中不正确的是( )
A. 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素
B. 硫酸的酸性比磷酸的酸性强,所以硫的非金属性比磷强
C. 氟化氢是最稳定的气态氢化物
D. 氢氧化铝的碱性强于氢氧化镁的碱性
难度: 简单查看答案及解析
-
下列叙述中正确的是( )
A. 阳离子一定含有金属元素, 阴离子一定只含有非金属元素
B. 某金属元素的阳离子和某非金属元素的阴离子组成的物质一定是纯净物
C. 全部由非金属组成的化合物一定是共价化合物
D. 金属钾不可能从盐的水溶液中置换出金属单质
难度: 简单查看答案及解析
-
氢氧燃料电池可以使用在航天飞机上,其反应原理如图所示。
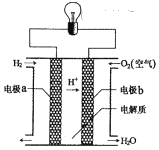
下列有关氢氧燃料电池的说法不正确的是( )
A. 该电池工作时化学能转化为电能
B. 该电池中电极b是正极
C. 外电路中电子由电极b通过导线流向电极a
D. 该电池的总反应为:2H2+O2===2H2O
难度: 中等查看答案及解析
-
A、B、C、D、E 是同一短周期的五种元素,A和B的最高价氧化物对应的水化物呈碱性, 且碱性前者强于后者, C和D的气态氢化物的水溶液呈酸性, 且酸性前者强于后者, 五种元素形成的简单离子中,E的离子半径最小, 则它们的原子序数由大到小的顺序是
A. B A D C E B. E C D A B
C. B A E D C D. C D E B A
难度: 中等查看答案及解析
-
新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于新能源
①煤 ②石油 ③太阳能 ④生物质能 ⑤氢能
A.①②③ B.①②⑤ C.②③⑤ D.③④⑤
难度: 简单查看答案及解析
-
下列有关碱金属元素的说法正确的是( )
A. 锂与过量氧气反应,生成过氧化锂
B. 从锂到铯,密度由小到大
C. 从锂到铯,熔沸点依次升高
D. 钠与水反应不如钾与水反应剧烈
难度: 简单查看答案及解析
-
据报道,科学家已成功合成了少量N4,有关N4的说法正确的是( )
A. N4与N2互为同素异形体
B. N4与N2互为同位素
C. 相同质量的N4和N2含原子个数比为1∶2
D. N4的摩尔质量是56 g
难度: 简单查看答案及解析
-
下列各对物质,化学键完全相同的是( )。
①NaCl和NaOH ②
和
③
和
④
和
⑤晶体硅和水晶
A. ①②③ B. ②④ C. ② D. ②④⑤
难度: 中等查看答案及解析
-
“摇摇冰”是一种即用即冷的饮料。吸食时将饮料罐隔离层中的化学物质和水混合后摇动即会制冷。该化学物质可能是
A.氯化钠 B.固体硝酸铵 C.生石灰 D.蔗糖
难度: 中等查看答案及解析
-
根据下表部分短周期元素信息,判断以下叙述正确的是( )
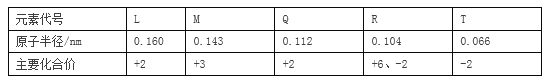
A. 氢化物的沸点为H2T<H2R B. 单质与稀盐酸反应的剧烈程度L<Q
C. M与T形成的化合物具有两性 D. L2+与R2﹣的核外电子数相等
难度: 中等查看答案及解析