-
下列说法不正确的是
A.纤维素、蛋白质、脂肪都属于高分子化合物
B.S8、P4O10、C60晶体都属于分子晶体
C.NaClO、NaHCO3、Na2SiO3都属于盐
D.Na2O、FeO、Fe2O3都属于碱性氧化物
难度: 中等查看答案及解析
-
如图为元素周期表中短周期的一部分,关于说法正确的是
A.简单离子半径:
B.Y、Z、M三种元素的气态氢化物中,Y元素的气态氢化物最稳定
C.X、Y、Z、M四种元素中,Y元素原子的第一电离能最大
D.组成为ZM2的分子中,中心原子Z是sp杂化
难度: 中等查看答案及解析
-
下列反应的离子方程式中正确的是
A.过氧化钠与水反应:O22- + 2H2O =2OH- + H2↑
B.用纯碱溶液溶解苯酚:CO32-+2C6H5OH = 2C6H5O- + CO2↑+H2O
C.用石墨作电极电解AlCl3溶液:2Cl- + 2H2O
Cl2↑ + H2↑ + 2OH-
D.将0.2 mol/L的NH4Al(SO4)2溶液与0.3 mol/L的Ba(OH)2溶液等体积混合:2Al3++3SO42-+3Ba2++6OH-= 2Al(OH)3↓+3BaSO4↓
难度: 中等查看答案及解析
-
下列实验操作中完全正确的是
编号 实验 操作
A 钠与水反应 用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中
B 排除碱式滴定管尖嘴部分的气泡 将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出
C 配制一定浓度的氯化钾溶液1000mL 准确称取氯化钾固体,放入到1000mL的容量瓶中,加水溶解,振荡摇匀,定容
D 取出分液漏斗中所需的上层液体 下层液体从分液漏斗下管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出
难度: 中等查看答案及解析
-
现有常温下的五种溶液(如下表)。
①
②
③
④
⑤
溶液
氨水
氢氧化钠
醋酸
盐酸
醋酸钠
pH
11
11
3
3
8.3
下列有关叙述中正确的是
A.五种溶液中,水电离出的c(OH-)最小的是⑤
B.将①、④两种溶液等体积混合,所得溶液中:c(Cl-) >c(NH4+)>c(H+)>c(OH-)
C.分别将①、②、③、④加水稀释100倍,稀释后四种溶液的pH:①>②>③>④
D.在⑤中加入适量的④至溶液呈中性,所得溶液中:c(Na+)>c(Cl-)=c(CH3COOH)
难度: 中等查看答案及解析
-
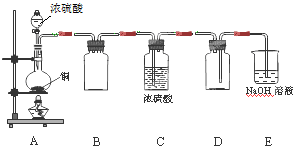
在一定条件下,CO(g)和H2(g)发生反应:CO(g) + 2H2(g)
CH3OH(g) △H=akJ/mol在容积固定的2L密闭容器中充入2mol CO(g)和4molH2(g)发生反应,测定在不同温度、不同时段下CO的转化率如下表:

下列说法中正确的是
A.热化学方程式中a>0
B.T1℃下,在第一小时内用H2表示的化学反应速率为0.4mol/(L.h)
C.T1℃下,该反应的化学平衡常数为25
D.T2℃下,ɑ1=ɑ2﹥80%
难度: 中等查看答案及解析
-
某磁黄铁矿的主要成分是FexS(S为-2价),既含有Fe2+又含有Fe3+。将一定量的该磁黄铁矿与100mL的盐酸恰好完全反应(注:矿石中其他成分不与盐酸反应),生成硫单质2.4g,FeCl2 0.425mol和一定量H2S气体,且溶液中无Fe3+。则下列说法正确的是
A.100mL的盐酸中HCl物质的量浓度为7.5mol/L
B.生成的H2S气体在标准状况下的体积为2.24L
C.该磁黄铁矿中FexS的x=0.85
D.该磁黄铁矿FexS中,Fe2+与Fe3+的物质的量之比为3:1
难度: 中等查看答案及解析
-
有A、E、R、X、Y、Z六种前四周期元素,原子序数依次增大,基态A原子的2p轨道处半充满状态,原子的第一电离能E﹤A, R是地壳中含量最高的金属元素,X原子核外的M层中有三对成对电子,Y为周期表前四周期中电负性最小的元素, Z原子核外电子数为24。
请回答下列问题:
(1)基态Z原子的核外电子排布式是________。AE2+与二氧化碳分子互为等电子体,AE2+的电子式是____。AX3 分子的VSEPR模型是________。
(2)某化合物由E、Y两种元素组成,其晶胞如图,该化合物的化学式为______。
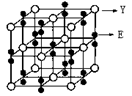
(3)在化合物Y2ZE4的水溶液入适量硫酸,能观察到的现象是________。
(4)A的简单氢化物极易溶于E的简单氢化物,其原因是________ 。
(5)A的最高价氧化物对应水化物的稀溶液与R的单质反应时,A被还原到最低价,该反应的化学方程式是________。
难度: 困难查看答案及解析
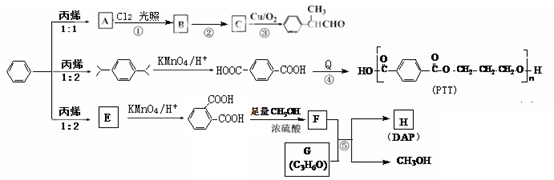
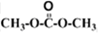 )发生酯交换反应,生成一种高分子化合物M和甲醇,写出M的结构简式________。
)发生酯交换反应,生成一种高分子化合物M和甲醇,写出M的结构简式________。