-
氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法不正确的是( )
A.太阳能催化分解水制氢气比电解水制氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.氢氧燃料电池可将化学能转化为电能
D.以稀H2SO4、KOH为介质的氢氧燃料电池的负极电极反应式相同难度: 中等查看答案及解析
-
某课外实验小组设计的下列实验不合理的是( )
A.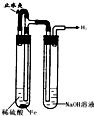
制备并观察氢氧化亚铁
B.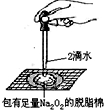
证明过氧化钠与水反应放热
C.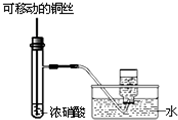
制备并收集少量NO2气体
D.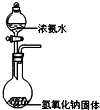
实验室制备少量氨气难度: 中等查看答案及解析
-
下列有关有机物的叙述正确的是( )
A.有机物不导电
B.粮食酿的酒在一定条件下密封保存一定时间会更香醇
C.棉、毛及合成纤维完全燃烧都只生成CO2和H2O
D.乙酸、蔗糖都是弱电解质难度: 中等查看答案及解析
-
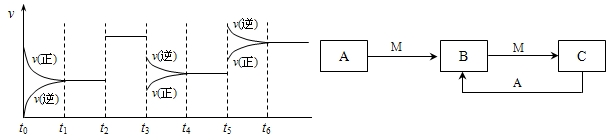
下表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
选项 a b c A Fe FeCl3 FeCl2 B Al(OH)3 NaAlO2 Al2O3 C HNO3 NO NO2 D CO2 C CO
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
类比推理是化学学习中的一种重要方法.下列类推结论正确的是( )
类比对象 结论 A Cl2+H2O=HCl+HClO F2+H2O=HF+HFO B MgCl2 Mg+Cl2↑
2AlCl3 2Al+3Cl2↑
C CH4+Cl2 CH3Cl+HCl
CH2=CHCH3+Cl2 CH2=CHCH2Cl+HCl
D Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO Ca(ClO)2+SO2+H2O=CaSO3↓+2HClO
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
关于下列四个图象的说法中正确的是( )

A.图①表示将SO2气体通入溴水中
B.图②表示反应N2(g)+3H2(g)2NH3(g)△H<0的平衡常数K随温度的变化
C.图③中阴、阳两极收集到的气体体积之比一定为1:1
D.图④中的△H1<△H2难度: 中等查看答案及解析
-
在某稀溶液中含有0.1mol HNO3和x mol H2SO4,向其中加入9.6g 铜粉,充分反应后产生的气体在标准状况下的体积为2.24L,则x值至少为( )
A.0.1
B.0.12
C.0.15
D.0.2难度: 中等查看答案及解析