-
下列氯化物中不能用金属和氯气直接反应制得的是( )
A. CuCl2 B. FeCl2 C. MgCl2 D. KCl
难度: 简单查看答案及解析
-
将一小块金属钠长期露置于空气中发生一系列变化,最终产物是
A. NaOH B. Na2O C. Na2O2 D. Na2CO3
难度: 简单查看答案及解析
-
镁、铝、铜三种金属粉末混合物, 加入过量盐酸充分反应, 过滤后向滤液中加入过量烧碱溶液, 再过滤, 滤液中存在的离子有( )
A. AlO2- B. Cu2+ C. Al3+ D. Mg2+
难度: 中等查看答案及解析
-
不能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是 ( )
A. 分别加热这两种固体物质,并将生成的气体通入澄清的石灰水中
B. 分别在这两种物质的溶液中,加入CaCl2溶液
C. 分别在这两种固体中,加入同浓度的稀盐酸
D. 分别在这两种物质的溶液中,加入少量澄清的石灰水
难度: 中等查看答案及解析
-
在实验室里,要想使AlCl3溶液中的Al3+全部沉淀出来,应选用下列试剂中的
A. 石灰水 B. 氢氧化钠溶液 C. 硫酸 D. 氨水
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 钠保存在煤油里的原因之一是它极易与氧气反应
B. 铝在空气中很容易燃烧
C. 镁表面的氧化膜疏松,不能保护内层金属
D. 铁锈的主要成分是Fe3O4
难度: 简单查看答案及解析
-
下列说法正确的是
A. 硅酸可由二氧化硅与水反应制得
B. Na2SiO3是硅酸盐,但不能溶于水
C. 硅是非金属元素,它的单质是灰黑色有金属光泽的固体
D. 硅是制造光导纤维的材料
难度: 简单查看答案及解析
-
Cl2用来消毒生活用水的原因是
A.Cl2能杀灭细菌
B.Cl2有毒
C.Cl2是氧化性很强的气体
D.Cl2与水反应生成HClO有强氧化性,可杀灭水中细菌
难度: 中等查看答案及解析
-
下列检验Fe3+的方法错误的是( )
A. 加入NaOH溶液,生成灰白色沉淀迅速变成灰绿色,最后变成红褐色
B. 加入NaOH溶液,生成红褐色沉淀
C. 加入硫氰化钾溶液,显示红色
D. 加入氨水,生成红褐色沉淀
难度: 简单查看答案及解析
-
下列各组物质相互作用,生成物不随反应条件或反应物的用量变化而变化的是
A. Na和O2 B. Na2CO3和HCl
C. AlCl3和NaOH D. NaOH和NaHCO3
难度: 简单查看答案及解析
-
下列物质中,不属于合金的是
A. 硬铝 B. 黄铜 C. 钢铁 D. 金箔
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A. 硅在自然界中能够以单质形式存在
B. SiO2是酸性氧化物, 所以不与任何酸反应
C. 可用Na2SiO3溶液和CO2反应来制备H2SiO3
D. NaOH溶液可以盛装在带玻璃塞的磨口试剂瓶中
难度: 简单查看答案及解析
-
除去镁粉中混有的少量铝粉,可选用的试剂是
A. 稀盐酸溶液 B. 稀硝酸溶液 C. 稀氨水 D. 稀氢氧化钠溶液
难度: 简单查看答案及解析
-
为了除去FeCl2溶液中混有的少量FeCl3,最好的方法是向此溶液中
A. 通入氯气 B. 加入Zn C. 加入Fe D. 加入Cu
难度: 中等查看答案及解析
-
相同质量的两份铝粉,分别放入足量的盐酸和氢氧化钠溶液中,放出的氢气在同温同压下的体积之比是( )
A. 1:1 B. 1:6 C. 2:3 D. 3:2
难度: 简单查看答案及解析
-
含有HCl和AlCl3的混合溶液中加入NaOH溶液,生成的沉淀和加入NaOH溶液的体积关系的大致图像为
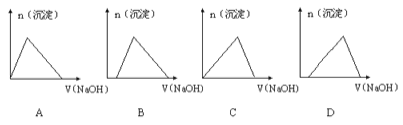
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列有关铁及其化合物的说法中正确的是( )
A. Fe3O4是一种红棕色粉末,俗称铁红
B. Fe(OH)2为白色固体,不溶于水,能在空气中稳定存在
C. Fe2(SO4)3与KSCN反应产生血红色沉淀
D. 除去FeCl3溶液中的FeCl2杂质,可以向溶液中通入适量的氯气
难度: 简单查看答案及解析
-
下列各项正确的是
A. 钠与水反应的离子方程式:Na+H2O = Na++OH-+H2↑
B. 氯气与水反应的离子方程式:Cl2+H2O
2H++Cl-+ClO-
C. AlCl3溶液中滴入过量的氨水:Al3++3NH3·H2O = Al(OH)3↓+3NH4+
D. 钠和硫酸铜溶液反应的离子方程式:2Na+Cu2+ = 2Na++Cu
难度: 简单查看答案及解析
-
下列说法正确的是
A. 浓硝酸在光照条件下变黄,说明浓硝酸不稳定,生成的有色产物能溶于浓硝酸
B. 在KI淀粉溶液中通入氯气,溶液变蓝,说明氯气能与淀粉发生显色反应
C. 在某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,说明溶液中一定含SO42-
D. 将铜片放入浓硫酸中,无明显实验现象,说明铜在冷的浓硫酸中发生钝化
难度: 中等查看答案及解析
-
下列关于硫的叙述中不正确的是
A. 实验室常用酒精除去附着在试管壁上的硫黄
B. 单质硫既有氧化性,又有还原性
C. SO2通入酸性高锰酸钾溶液中使之褪色说明SO2具有还原性
D. SO2通入饱和H2S溶液中析出浅黄色沉淀说明SO2具有氧化性
难度: 简单查看答案及解析
-
下图是实验室进行氨溶于水的“喷泉实验”的装置,下列叙述不正确的是( )
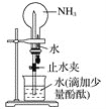
A. 该实验说明氨气极易溶于水
B. 进入烧瓶中的液体颜色由无色变为红色,说明氨水呈碱性
C. 氨水很稳定,将烧瓶内的红色溶液加热颜色不会发生变化
D. 形成“喷泉”的主要原因是氨气溶于水后,烧瓶内的气压小于大气压
难度: 简单查看答案及解析
-
把铁、铜、盐酸、FeCl3、FeCl2和CuCl2溶液混在一起,铁有剩余,则溶液中所含最多的阳离子是
A. H+ B. Cu2+ C. Fe3+ D. Fe2+
难度: 中等查看答案及解析
-
在标准状况下将2.24 LCO2通过一定量的固体过氧化钠后收集到1.68L气体,则收集到的气体中O2 的体积为
A. 0.28L B. 0. 56L C. 1.12L D. 2.24L
难度: 中等查看答案及解析
-
200mL 1mol•L—1的氯化铝溶液中加入一定体积的2mol•L—1的NaOH溶液,最终产生7.8g沉淀,则加入的NaOH溶液的体积可能为
①350mL ②90mL ③150mL ④200mL
A. 只有① B. ①③ C. ②④ D. ②③
难度: 中等查看答案及解析
-
1.92g铜投入一定量浓HNO3中,铜完全溶解,生成气体颜色越来越浅,共收集到672mL气体(标况)。将盛有此气体的容器倒扣在水中,通入标况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积可能是
A. 504mL B. 168mL C. 336mL D. 224mL
难度: 困难查看答案及解析