-
我国古代就有湿法炼铜的记载“曾青得铁则化为铜”,反应为Fe+CuSO4=Cu+FeSO4。有关该反应的说法正确的是
A. Fe是氧化剂 B. CuSO4是还原剂
C. Fe被氧化 D. CuSO4发生氧化反应
难度: 中等查看答案及解析
-
下列溶液中溶质的物质的量浓度为1 mol·L-1的是
A. 将58.5 g NaCl溶解于1 L水中配成的溶液
B. 将80 g SO3溶于水并配成1 L溶液
C. 将0.5 mol·L-1的NaNO3溶液100 mL加热蒸发掉50 g水的溶液
D. 含K+为2 mol的K2SO4溶液
难度: 简单查看答案及解析
-
下列物质分类的正确组合是( )
碱
酸
盐
酸性氧化物
A
纯碱
盐酸
烧碱
二氧化硫
B
烧碱
硫酸
食盐
一氧化碳
C
苛性钠
醋酸
石灰石
水
D
苛性钾
碳酸
苏打
三氧化硫
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列电离方程式中正确的是
A. Al2(SO4)3=2Al3++3SO42- B. Na2SO4=2Na++SO4-2
C. Ca(NO3)2=Ca2++2(NO3)2- D. Ba(OH)2=Ba2++OH2-
难度: 简单查看答案及解析
-
某盐的混合物中含有0.2mol Na+、0.4mol Mg2+、0.4mol Cl-,则SO42-为
A. 0.1mol B. 0.3mol C. 0.5mol D. 0.15mol
难度: 中等查看答案及解析
-
氧化还原反应的实质是( )
A. 元素化合价发生变化 B. 反应中有氧原子的得失
C. 反应中有电子得失或电子偏移 D. 反应后生成新物质
难度: 中等查看答案及解析
-
在下列物质类别中,前者包含后者的是
A. 混合物 溶液 B. 电解质 化合物
C. 浊液 胶体 D. 单质 化合物
难度: 中等查看答案及解析
-
浓H2SO4应贴下列哪个危险化学品的标志
A. 剧毒品 B. 遇湿易燃物品 C. 腐蚀品 D. 有害品
难度: 简单查看答案及解析
-
下列说法正确的是
A. 氧气的气体摩尔体积是22.4L B. 硫酸的摩尔质量是98g
C. CO2的相对分子质量是44g D. CO32—摩尔质量是60g/mol
难度: 简单查看答案及解析
-
下列实验操作或装置正确的是
A. 点燃酒精灯
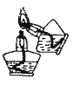 B. 蒸馏
B. 蒸馏 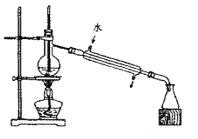
C. 过滤
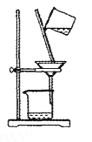 D. 稀释浓硫酸
D. 稀释浓硫酸
难度: 中等查看答案及解析
-
下列各组物质,需要用丁达尔效应区分的是
A. 氯化钠溶液与氯化铁溶液 B. 氢氧化铁胶体与碘化银胶体
C. 红褐色的某溶液和氢氧化铁胶体 D. 氯化钠溶液和硫酸铜溶液
难度: 简单查看答案及解析
-
下列实验仪器不宜直接用来加热的是
A. 试管 B. 燃烧匙 C. 蒸发皿 D. 烧杯
难度: 简单查看答案及解析
-
能正确表示下列化学反应的离子方程式的是
A. 氢氧化钡溶液与硫酸的反应 OH+H+ = H2O
B. 澄清的石灰水与稀盐酸反应 Ca(OH)2 + 2H+ = Ca2+ + 2H2O
C. 铜片插入硝酸银溶液中 Cu + Ag+ = Cu2+ + Ag
D. 碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2
难度: 中等查看答案及解析
-
在下列溶液中Cl-的物质的量浓度最大的是
A. 0.5L 0.1mol/L的NaCl溶液 B. 100mL 0.2mol/L的MgCl2溶液
C. 1L 0.2mol/L的AlCl3溶液 D. 1L 0.3 mol/L盐酸溶液
难度: 中等查看答案及解析
-
在2FeBr2+3Cl2===2FeCl3+2Br2的反应中,被氧化的元素是
A. Fe B. Br C. Fe和Br D. Cl
难度: 简单查看答案及解析
-
下列各组反应中,不能用同一个离子方程式表示的是
A. 盐酸分别与NaOH溶液、Ca(OH)2溶液反应
B. 硫酸分别与NaOH溶液、Ba(OH)2溶液反应
C. 硝酸分别与Na2CO3溶液、K2CO3溶液反应
D. 锌分别与稀盐酸、稀硫酸反应
难度: 中等查看答案及解析
-
下列离子可以大量共存的是
A. K+ SO42- Na+ HCO3- B. K+ Ag+ Cl- NO3-
C. Ba2+ Na+ OH- CO32- D. Al3+ NH4+ NO3- OH-
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数,下列叙述中正确的是
A. 常温常压下,11.2L NH3所含的原子数为2NA
B. 常温常压下,80g SO3含有的氧原子数为3NA
C. 标准状况下,22.4L H2中所含原子数为NA
D. 标准状况下,1molH2O的体积约为22.4L
难度: 简单查看答案及解析
-
常温常压下,用等质量的CH4、CO2、O2、SO2四种气体分别吹出四个气球,其中气体为CO2的是
A.
B.
C.
D.
难度: 中等查看答案及解析
-
为了除去粗盐中的CaCl2、MgCl2、Na2SO4及泥沙,可将粗盐溶于水,然后进行下列五项操作①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液。下列操作顺序中最合适的是
A. ①④②⑤③ B. ④①②⑤③ C. ②⑤④①③ D. ⑤②④③①
难度: 中等查看答案及解析