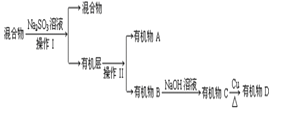
-
下列各物质的沸点按由高到低顺序排列的是
①1,2,2—三氯丙烷 ②乙烷 ③丙烷 ④异戊烷 ⑤2,2—二甲基丙烷
A. ①④⑤③② B. ①③④②⑤ C. ⑤④①③② D. ⑤①③④②
难度: 中等查看答案及解析
-
一种气态烷烃和一种气态烯烃的混合物共10 g,平均相对分子质量为25。使混合气通过足量溴水,溴水增重8.4 g,则混合气中的烃可能是
A. 甲烷和乙烯 B. 甲烷和丙烯
C. 乙烷和乙烯 D. 乙烷和丙烯
难度: 困难查看答案及解析
-
下列过程通电后才能进行的是( )
①电离 ②电解 ③电镀 ④电化学腐蚀.
A. ①②③ B. ①②④ C. ②③ D. 全部
难度: 简单查看答案及解析
-
下列反应不属于取代反应的是
A. 乙烷与氯气反应 B. 乙烯与溴水的反应
C. 苯的硝化反应 D. 苯与液溴的反应
难度: 简单查看答案及解析
-
下列化学用语或概念的表达不正确的是
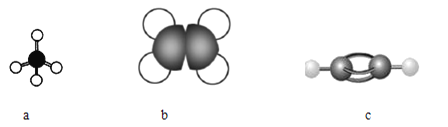
①丙烷的球棍模型
 ②丙烯的结构简式为
②丙烯的结构简式为③
和
一定互为同系物 ④
与
一定互为同分异构体
A. ①② B. ②③ C. ③④ D. ②④
难度: 中等查看答案及解析
-
下列关于铜电极的叙述中,正确的是
A. 铜锌原电池中铜是正极 B. 用电解法精炼粗铜时粗铜作阴极
C. 在镀件上电镀铜时可用金属铜作阴极 D. 电解稀疏酸制
、
时铜作阳极
难度: 中等查看答案及解析
-
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是 ( )
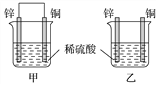
A. 两烧杯中溶液的pH均增大
B. 甲中铜片是正极,乙中铜片是负极
C. 两烧杯中铜片表面均无气泡产生
D. 产生气泡的速度甲比乙慢
难度: 简单查看答案及解析
-
对有机物
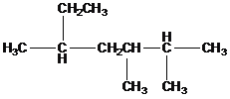 说法正确的是
说法正确的是A. 1mol该物质所含原子数为
B. 该物质系统命名为2,3-二甲基-5-乙基己烷
C. 该物质一个分子中最多10个碳原子共平面
D. 该物质为某炔烃加氢后的产物,则可能的炔烃的结构只有一种
难度: 中等查看答案及解析
-
有一种有机物结构简式为
CH=CH2推测它不可能具有下列哪种性质
A. 能被酸性高锰酸钾溶液氧化 B. 能与溴水发生加成反应褪色
C. 能发生加聚反应 D. 易溶于水,也易溶于有机溶剂
难度: 中等查看答案及解析
-
已知化合物C6H6(苯)与B3N3H6(硼氮苯)的分子结构相似,如图所示,则硼氮苯的二氯取代物B3N3H4Cl2的同分异构体的数目为
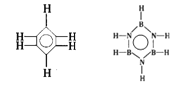
A. 2 B. 3 C. 4 D. 6
难度: 困难查看答案及解析
-
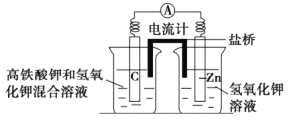
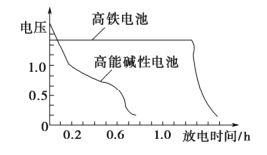
碱性电池具有容量大、放电电流大的特点而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:
 ,下列说法错误的是
,下列说法错误的是A. 电池工作时,锌失去电子
B. 用该电池电解水时,电子通过外电路流向电解池阳极
C. 电池正极电极反应式

D. 外电路中每通过0.2mol电子,锌的质量理论上减小6.5g
难度: 中等查看答案及解析
-
用阳极
和阴极
电解
的水溶液,电解一段时间后,再加入
,能使溶液恢复到电解前的状态,符合题意的一组是
A
B
溶液
C
D
晶体
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
镍镉可充电电池,电极材料是
和
,电解质是
,放电时的电极反应式是
,
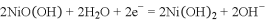 。下列说法不正确的是
。下列说法不正确的是A. 电池的总反应式是
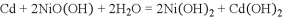
B. 电池充电时,镉元素被还原
C. 电池充电时,电池的负极和电源的负极连接
D. 电池放电时,电池负极周围溶液的
不断增大
难度: 中等查看答案及解析
-
1 L(标准状况下)某气态烃,完全燃烧生成的CO2和水蒸气在273 ℃、1.01×105 Pa下体积为y L,当冷却至标准状况时体积为x L。下列用x、y表示该烃的化学式正确的是
A. CxHy-2x B. CxHy-x C. CxH2y-2x D. CxHy
难度: 困难查看答案及解析
-
如图,四种装置中所盛有的溶液体积均为200ml,浓度均为0.6mol/L,工作一段时间后,测得导线上均通过了0.2mol电子,此时溶液中的
由大到小的顺序是
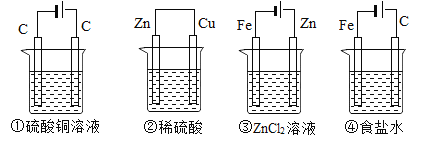
①硫酸铜溶液 ②稀硫酸 ③氯化锌溶液 ④食盐水
A. ④②①③ B. ④③①② C. ④③②① D. ①③②④
难度: 中等查看答案及解析
-
将图1所示装置中的盐桥(琼脂-饱和
溶液)换成铜导线与石墨棒连接得到图2所示装置,发现电流计指针仍然有偏转。下列说法正确的是
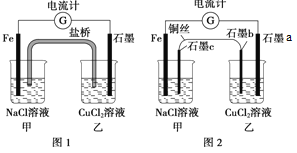
A. 图1中,铁棒质量减少5.6g,则甲池
溶液的质量增加5.6g
B. 图1中的石墨电极与图2中乙池石墨
电极的电极反应式相同
C. 两图所示装置的能量变化均是将化学能转化为电能
D. 图2中电子流向为
电流计→石墨a→石墨b→铜丝→石墨c→
难度: 困难查看答案及解析