-
海水淡化可解决淡水资源缺乏的问题。下列可应用于海水淡化技术的操作是( )
A. 蒸馏 B. 过滤 C. 萃取 D. 结晶
难度: 简单查看答案及解析
-
向空气中“挖矿”,为人类粮食增产做出巨大贡献的化学工业是( )
A. 硫酸工业 B. 合成氨工业 C. 纯碱工业 D. 石油化工
难度: 简单查看答案及解析
-
下列含氮微粒的化学用语表达正确的是( )
A. 氮-14原子:
B. 氮原子的轨道表示式:
C. 氨气的电子式:
D. 氮气的结构式:N
N
难度: 中等查看答案及解析
-
和纯铁相比,生铁不具有的特点是( )
A. 硬度更大 B. 熔点更低 C. 更耐腐蚀 D. 易冶炼得到
难度: 简单查看答案及解析
-
不是煤干馏产物的是( )
A. 煤油 B. 焦炭 C. 焦炉气 D. 粗氨水
难度: 简单查看答案及解析
-
铵态氮肥在使用时要注意低温保存和深施盖土,原因是铵态氮肥( )
A. 易溶于水 B. 遇碱易跑氨 C. 易被氧化 D. 受热易分解
难度: 简单查看答案及解析
-
葡萄酒中加入少量SO2,可防止酒中的乙醇转化为乙酸,这是利用了SO2的( )
A. 氧化性 B. 还原性 C. 漂白性 D. 酸性
难度: 中等查看答案及解析
-
关于氯化氢的说法错误的是( )
A. 溶于水时破坏共价键 B. 可用于做喷泉实验
C. 遇氨气产生白烟 D. 可通过共价键形成晶体
难度: 简单查看答案及解析
-
下列物质中,不能使酸性高锰酸钾溶液褪色的是
A. 乙烯 B. 乙炔 C. 苯 D. 甲苯
难度: 简单查看答案及解析
-
下列物质露置在空气中,会发生化学反应且有颜色变化的是( )
A. NaClO B. NaOH C. Na2O2 D. NaCl
难度: 中等查看答案及解析
-
用烧碱固体配制0.100mol/L NaOH溶液的部分操作如图所示,其中不需要的是( )
A.
检漏 B.
量取 C.
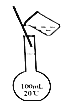 转移 D.
转移 D. 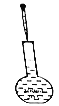 定容
定容难度: 简单查看答案及解析
-
关于氧化铝和氢氧化铝的说法错误的是( )
A. 都是白色固体 B. 都难溶于水
C. 都具有两性 D. 都受热易分解
难度: 简单查看答案及解析
-
港珠澳大桥设计寿命为120年,对桥体钢制构件采用了多种防腐措施,下列防腐措施错误的是( )
A. 用导线与石墨相连 B. 用导线与电源负极相连
C. 钢制构件上焊接锌块 D. 表面喷涂分子涂层
难度: 中等查看答案及解析
-
用标准盐酸滴定待测NaOH溶液时,相关说法正确的是( )
A. 可用石蕊作指示剂 B. 滴定时眼睛注视滴定管中液面下降
C. 需做平行实验2~3次 D. 当溶液颜色变化时立即读数
难度: 简单查看答案及解析
-
下列关于实验室制备乙酸乙酯的操作错误的是( )
A. 配料:加入过量乙醇 B. 加热:用水浴加热
C. 分离:用边反应边分离的方法 D. 净化:产物用氢氧化钠溶液洗涤
难度: 简单查看答案及解析
-
A、B、C、D四种短周期元素在周期表中的位置如图所示,有关说法正确的是( )
A. 元素最高正价数值最大的是A
B. 单质熔点最高的是C
C. 离子半径:A<C
D. 金属性:B>C
难度: 中等查看答案及解析
-
如图所示,将浓硫酸滴至下列物质上,无明显现象的是( )
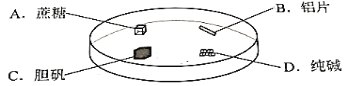
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
某含氧衍生物的球棍模型如下图所示,下列关于该物质的说法错误的是( )
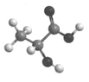
A. 分子式为C3H6O3
B. 含有两种官能团
C. 能发生取代反应,不能发生消去反应
D. 既能与生石灰反应,又能与氢溴酸反应
难度: 中等查看答案及解析
-
氨碱法与侯氏制碱法的生产工艺中,相同的是( )
A. 主反应原理 B. 副产品
C. 食盐利用率 D. 循环物质
难度: 中等查看答案及解析
-
某溶液中可能含有Na+、Fe2+、NH4+、K+、Cl-、SO42-、SO32-中的几种,且所含离子物质的量浓度均为0.01mol/L。向溶液中滴加少量溴水后,溶液呈无色。下列关于该溶液的判断正确的是( )
A. 可能含有Na+ B. 可能含有SO42- C. 一定不含Cl- D. 一定含有NH4+
难度: 困难查看答案及解析
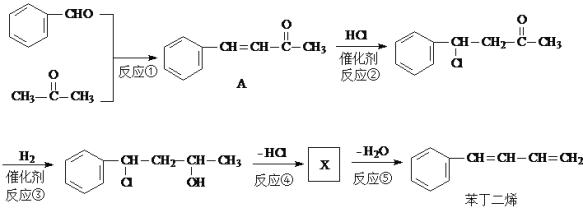
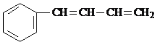 )的途径如下:
)的途径如下: