-
X、Y、Z、W是短周期元素,X元素原子的最外层未达到8电子稳定结构,工业上通过分离液态空气获得其单质;Y元素原子最外电子层上s、p电子数相等;Z元素+2价阳离子的核外电子排布与氖原子相同;W元素原子的M层有1个未成对的p电子。下列有关这些元素性质的说法一定正确的是
A. X元素的氢化物的水溶液显碱性
B. Z元素的离子半径大于W元素的离子半径
C. Z元素的单质在一定条件下能与X元素的单质反应
D. Y元素最高价氧化物的晶体具有很高的熔点和沸点
难度: 困难查看答案及解析
-
短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4∶3,Z原子比X原子的核外电子数多4。下列说法正确的是( )
A. W、Y、Z的电负性大小顺序一定是Z>Y>W
B. W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z
C. Y、Z形成的分子的空间构型可能是正四面体
D. WY2分子中σ键与π键的数目之比是2∶1
难度: 中等查看答案及解析
-
现有四种元素的基态原子的电子排布式如下,则下列有关比较中正确的是( )。
①1s22s2 2p63s23p4; ②1s22s22p63s23p3; ③1s22s2 2p3; ④1s22s22p5。
A. 第一电离能:④>③>②>① B. 原子半径:④>③>②>①
C. 电负性:④>③>②>① D. 最高正化合价:④>③=②>①
难度: 中等查看答案及解析
-
下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示,单位为kJ·mol-1)。关于元素R的判断中一定正确的是( )
I1
I2
I3
I4
……
R
740
1 500
7 700
10 500
①R的最高正价为+3价 ②R元素位于元素周期表中第ⅡA族 ③R元素第一电离能大于同周期相邻元素 ④R元素基态原子的电子排布式为1s22s2
A. ①② B. ②③ C. ③④ D. ①④
难度: 中等查看答案及解析
-
下列轨道表示式所表示的元素原子中,其能量处于最低状态的是( )
A.
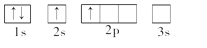
B.
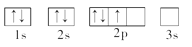
C.
D.
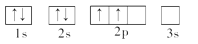
难度: 中等查看答案及解析
-
已知元素X的基态原子最外层电子排布为nsn-1npn+2,则X元素的原子序数为( )
A. 9 B. 10 C. 17 D. 18
难度: 简单查看答案及解析
-
下列各组分子中都属于含极性键的非极性分子的是( )
A. CO2、H2S B. C2H4、CH4 C. Cl2、C2H2 D. NH3、HCl
难度: 中等查看答案及解析
-
下列分子中,中心原子是sp杂化的是( )
A. BeCl2 B. H2O C. CH4 D. BF3
难度: 简单查看答案及解析
-
氯化亚砜(SOCl2)是一种很重要的化学试剂,可以作为氯化剂和脱水剂。下列关于氯化亚砜分子的几何构型和中心原子(S)采取杂化方式的说法正确的是
A. 三角锥形、sp3 B. V形、sp2 C. 平面三角形、sp2 D. 三角锥形、sp2
难度: 中等查看答案及解析
-
氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键的夹角为120°,它能水解,有关叙述正确的是( )
A. 氯化硼液态时能导电而固态时不导电
B. 氯化硼中心原子采用sp杂化
C. 氯化硼分子呈正三角形,属非极性分子
D. 三氯化硼遇水蒸气不会产生白雾
难度: 简单查看答案及解析
-
下列叙述中正确的是( )
A. P4、CO、CO2都是极性分子
B. HCN、CCl4都是含有极性键的非极性分子
C. HF、HCl、HBr、Hl的稳定性依次减弱
D. CS2、H2O、C2H2都是直线型分子
难度: 中等查看答案及解析
-
下列粒子属于等电子体的是( )
A. CH4和NH4+ B. NO和O2
C. NH2-和H3O+ D. HCl和H2O
难度: 中等查看答案及解析
-
下列过程中,共价键被破坏的是( )
A. 碘升华 B. 溴蒸气被木炭吸附
C. 酒精溶于水 D. 氯化氢气体溶于水
难度: 简单查看答案及解析
-
下列物质中所含微粒的个数比是1∶1的是( )
A. CH3COONa溶液中CH3COO-和Na+
B. NH4+中的质子和电子
C. Na2O2固体中阴、阳离子
D.
原子中的质子和中子
难度: 中等查看答案及解析
-
N2的结构可以表示为
,CO的结构可以表示为
,其中椭圆框表示π键,下列说法中不正确的是()
A. N2分子与CO分子中都含有叁键
B. CO分子中有一个π键是配位键
C. N2与CO互为等电子体
D. N2与CO的化学性质相同
难度: 中等查看答案及解析
-
我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:HCHO+O2
CO2+H2O △H<0。下列有关说法正确的是( )
A. 该反应为吸热反应
B. CO2分子中的化学键为非极性键
C. HCHO分子中既含σ键又含π键
D. 每生成1.8g H2O消耗2.24 L O2
难度: 中等查看答案及解析
-
二茂铁[(C5H5)2Fe]是由一个二价铁离子和2个环戊烯基负离子构成,它的发现可以说是有机金属化合物研究中具有里程碑意义的事件,它开辟了金属有机化合物研究的新领域。已知:二茂铁熔点是173 ℃(在100 ℃时开始升华),沸点是249 ℃,不溶于水,易溶于苯、乙醚等非极性溶剂。下列说法正确的是( )
A. 二茂铁属于离子晶体
B. 在二茂铁结构中,C5H5-与Fe2+之间形成的化学键类型是离子键
C. 已知:环戊二烯的结构式为:
 ,则其中碳环上有2个π键和5个σ键
,则其中碳环上有2个π键和5个σ键D. 二价铁离子的基态电子排布式为:[Ar]3d44s2
难度: 中等查看答案及解析
-
如图所示晶体结构是一种具有优良的压电、电光碘功能的晶体材料的最小结构单元(晶胞)。这种晶体材料的化学式是(各元素所带电荷均已略去)( )
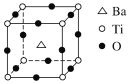
A. BaTi8O12 B. BaTi4O9 C. BaTiO3 D. BaTi2O3
难度: 简单查看答案及解析
-
向盛有硫酸铜水溶液的试管里滴加氨水,首先形成难溶物,继续滴加氨水,难溶物溶解,得到深蓝色的透明溶液,下列对此现象的说法正确的是( )
A. 开始滴加氨水时形成的难溶物为Cu2(OH)2CO3
B. 沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4]2+,配位数为4
C. 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
D. 在[Cu(NH3)4]2+中,Cu2+给出孤电子对,NH3提供空轨道
难度: 简单查看答案及解析
-
下列对一些实验事实的理论解释正确的是( )
选项
实验事实
理论解释
A
SO2溶于水形成的溶液能导电
SO2是电解质
B
白磷为正四面体分子
白磷分子中P-P键的键角是109°28′
C
1体积水可以溶解700体积氨气
氨是极性分子且分子间存在氢键影响
D
HF的沸点高于HCl
H-F的键长比H-Cl的短
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
关于氢键,下列说法正确的是( )
A. 每一个水分子内含有两个氢键
B.
的熔沸点明显高于
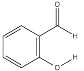 ,对羟基苯甲醛分子间存在氢键,而邻羟基苯甲醛存在分子内氢键。
,对羟基苯甲醛分子间存在氢键,而邻羟基苯甲醛存在分子内氢键。C. H2O是一种非常稳定的化合物,这是由于氢键所致
D. SO2易溶于水,重要的原因之一是由于SO2与H2O之间能形成氢键
难度: 中等查看答案及解析
-
Co(Ⅲ)的八面体配合物CoClm·nNH3,若1 mol配合物与AgNO3作用生成1 molAgCl沉淀,则m、n的值是( )
A. m=1,n=5 B. m=3,n=4
C. m=5,n=1 D. m=4,n=5
难度: 中等查看答案及解析
-
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
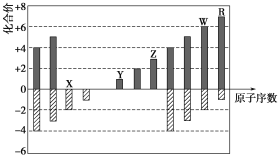
A. 原子半径:Z>Y>X
B. 气态氢化物的稳定性:R<W
C. WX3和水反应形成的化合物是离子化合物
D. Y和Z两者最高价氧化物对应的水化物能相互反应
难度: 简单查看答案及解析
-
X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示。若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
A. X的最常见气态氢化物的水溶液显酸性
B. 最高价氧化物对应水化物的酸性W比Z强
C. Z的单质与氢气反应比Y单质与氢气反应容易
D. X的原子半径小于Y
难度: 中等查看答案及解析