-
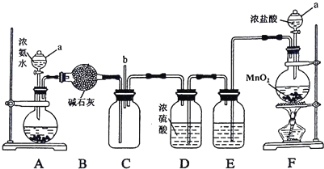
下列仪器中不能用于加热的是( )
A. 试管 B. 烧杯 C. 量筒 D. 坩埚
难度: 中等查看答案及解析
-
下列物质中,属于电解质的是( )
A. NaCl B. Al C. C2H5OH D. NaOH溶液
难度: 简单查看答案及解析
-
在氧化还原反应中,水作为氧化剂的是( )
A. 2Na +2H2O = 2NaOH + H2 ↑ B. 3NO2+ H2O = 2HNO3+ NO
C. 2Na2O2+2H2O = 4NaOH + O2 ↑ D. 2F2+ 2H2O = 4HF + O2
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A. 分散质粒子的直径在1~100 nm之间的微粒称为胶体
B. 电泳现象可证明胶体属于电解质溶液
C. 利用丁达尔效应可以区别溶液与胶体
D. Fe (OH)
胶体带正电荷,可以产生电泳现象
难度: 中等查看答案及解析
-
下列物质或溶液不能与CO2反应的是( )
A. Na2O2 B. CaCl2溶液 C. NaOH溶液 D. Na2CO3溶液
难度: 简单查看答案及解析
-
下列反应的离子方程式正确的是( )
A. 往碳酸镁中滴加稀盐酸:CO32-+2H+=CO2↑+H2O
B. 用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O
C. 盐酸滴入氨水中:H++OH-=H2O
D. 锌溶解于稀硝酸中:Zn+2H+=Zn2++H2↑
难度: 简单查看答案及解析
-
不能说明氯元素的非金属性比硫元素强的事实是( )
A. Cl2与H2S溶液发生置换反应 B. 受热时H2S能分解,HCl则不能
C. 单质硫可在空气中燃烧,Cl2不能 D. HClO4酸性比H2SO4酸性强
难度: 简单查看答案及解析
-
下列离子在强酸性溶液中能大量共存的是( )
A. K+、Cl
、NO
、 HCO
B. K
、NO
C. Na
、Ca
、Cl
、 CO
D. Na
、Cl
、NO
、SO
难度: 简单查看答案及解析
-
0.5 L1mol/L的FeCl3溶液与0.2 L 1 mol/L的KCl溶液中,Cl-浓度比为( )
A. 15∶2 B. 1∶1 C. 3∶1 D. 1∶3
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 在常温常压下,11.2LN2含有的分子数为0.5 NA
B. 标准状况下,22.4LH2和O2的混合物所含分子数为NA
C. 标准状况下,18gH2O的体积是22.4 L
D. 1 mol SO2的体积是22.4L
难度: 中等查看答案及解析
-
下列结论正确的是的是( )
A. 微粒半径:K+>Al3+>S2->Cl- B. 氢化物的稳定性:HF>HCl>H2S>PH3
C. 离子的还原性:S2->Cl->Br->I- D. 金属性:Be>Mg>Ca>K
难度: 简单查看答案及解析
-
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如下图所示,若Y原子的最外层电子是次外层电子数的3倍,下列说法正确的是( )
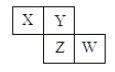
A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性:Z>W>X
C. 4种元素的单质中,Z单质的熔沸点最低
D. W单质能与水反应,生成一种具有漂白性的物质
难度: 简单查看答案及解析
-
下列关于元素周期表的说法正确的是( )
A. 元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行
B. 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
C. 除短周期外,其它周期均为18种元素
D. 周期表中所有元素都是从自然界中发现的
难度: 简单查看答案及解析
-
几种短周期元素的原子半径及主要化合价如表:
元素代号
X
Y
Z
M
R
原子半径/nm
0.186
0.102
0.075
0.074
0.143
主要化合价
+1
+6、−2
+5、−3
−2
+3
已知X是短周期中最活泼的金属,且与R同周期。下列叙述不正确的是( )
A. 离子半径大小:R3+<X+<M2−
B. Y与M组成的化合物是光化学烟雾的原因之一
C. 将YM2通入Ca(OH)2溶液中有白色沉淀产生
D. Z的单质是空气的主要的成分之一
难度: 简单查看答案及解析
-
假设R元素无同位素,元素R原子的质量数为A,Rm-的核外电子数为x,则WgRm-离子所含中子的物质的量为( )
A. (A-x+m) mol
B. (A-x-m) mol
C.
(A-x+m) mol
D.
(A-x-m) mol
难度: 简单查看答案及解析
-
将0.06 mol FeCl2加入100 mL K2Cr2O7溶液中,恰好使溶液中Fe2+全部转化为Fe3+,Cr2O
被还原为Cr3+。则K2Cr2O7溶液的物质的量浓度为( )
A. 0.4 mol/L B. 0.2mol/L C. 0.1 mol/L D. 0.08mol/L
难度: 中等查看答案及解析