-
为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法都正确的是( )
序号
不纯物
除杂试剂
分离方法
A
CH4(C2H4)
酸性KMnO4溶液
洗气
B
苯(Br2)
NaOH溶液
过滤
C
C2H5OH(H2O)
生石灰
蒸馏
D
乙酸乙酯(乙酸)
饱和Na2CO3溶液
蒸馏
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列用系统命名法命名的有机物名称正确的是( )
A. 2 -甲基--4--乙基戊烷 B. 2, 3 --二甲基--1--戊烯
C. 3, 4, 4--三甲基己烷 D. 2, 2--二甲基-2-丁烯
难度: 简单查看答案及解析
-
化学已渗透到人类生活的各个方面。下列说法正确的是( )
A. 乙醇和汽油都是可再生能源,应大力推广使用“乙醇汽油”
B. 地沟油的主要成分是高级脂肪酸甘油酯,可用于制肥皂和生产生物柴油
C. 某雨水样品放置一段时间后pH由4.98变为4.68,是因为水中溶解的CO2增多了
D. 高纯度的硅单质广泛用于制作光导纤维,光导纤维是新型高分子非金属结构材料
难度: 简单查看答案及解析
-
下列关于乙烯和聚乙烯的叙述中正确的是( )
A. 二者都能使溴水褪色 B. 二者互为同系物
C. 二者最简式相同 D. 二者相对分子质量相同
难度: 简单查看答案及解析
-
维生素P的结构如图所示,其中R为烷烃基,维生素P是一种营养增补剂。下列关于维生素P的叙述正确的是( )
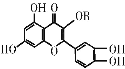
A. 分子中的官能团有羟基、碳碳双键、醚键、酯基
B. 若R为甲基,则该物质的分子式可以表示为C16H14O7
C. 该化合物遇三氯化铁溶液发生显色反应
D. 1 mol该化合物与氢气加成所需氢气的物质的量最多是7 mol
难度: 简单查看答案及解析
-
一种气态烷烃和一种气态烯烃组成的混合物共0.1 mol,完全燃烧得0.16 mol二氧化碳和3.6 g水。下列说法正确的是( )
A. 一定有甲烷 B. 一定是甲烷和乙烯 C. 可能有乙烷 D. 一定有乙炔
难度: 中等查看答案及解析
-
下列不能用勒夏特列原理解释的事实是( )
A. 棕红色的NO2加压后颜色先变深后变浅
B. 加催化剂,使N2和H2在一定条件下转化为NH3
C. 鼓入过量空气有利于SO2转化为SO3
D. 合成氨工业使用高压以提高氨的产量
难度: 简单查看答案及解析
-
已知热化学方程式:
①CO(g)+1/2O2(g)=CO2(g)ΔH=-283.0kJ·mol-1
②H2(g)+1/2O2(g)=H2O(g)ΔH=-241.8 kJ·mol-1
则下列说法正确的是( )
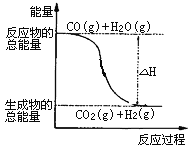
A. H2的燃烧热为241.8kJ·mol-1
B. 由反应①、②可知上图所示的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g)ΔH=-41.2 kJ·mol-1
C. H2(g)转变成H2O(g)的化学反应一定要放出能量
D. 根据②推知反应H2(g)+1/2O2(g)=H2O(l)ΔH>-241.8 kJ·mol-1
难度: 中等查看答案及解析
-
分子式为C5 H10 O 2的有机物在适当条件下能与饱和碳酸氢钠反应,则其结构(不考虑立体异构)最多有( )
A. 2种 B. 3种 C. 4种 D. 5种
难度: 中等查看答案及解析
-
下列反应属于氧化还原反应,且能量变化如下图所示的是( )
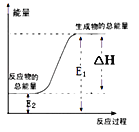
A. 锌粒和稀硫酸反应
B. 灼热的木炭与CO2反应
C. 甲烷在空气中燃烧的反应
D. Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
难度: 简单查看答案及解析
-
在铁与稀硫酸反应制氢气的实验中,下列因素对产生H2速率没有影响的是( )
A. 加几滴硫酸铜溶液 B. 将铁块换成铁粉
C. 初始加入的稀硫酸由5 mL变成10 mL D. 升温
难度: 简单查看答案及解析
-
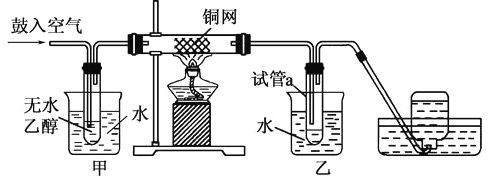
用下列装置完成相关实验,不合理的是( )
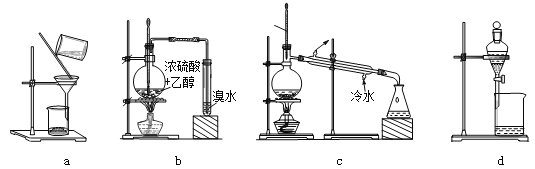
A. 用a趁热过滤提纯苯甲酸 B. 用b制备并检验乙烯
C. 用c除去溴苯中的苯 D. 用d分离硝基苯与水
难度: 中等查看答案及解析
-
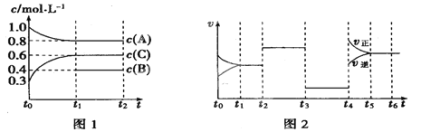
对于反应2A(g)+B(g)
2C (g)ΔH<0,下列图象正确的是( )
A.
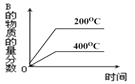 B.
B. 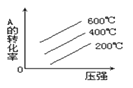
C.
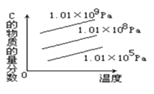 D.
D. 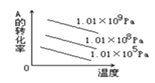
难度: 中等查看答案及解析
-
t ℃时,将一定量的混合气体在密闭容器中发生反应:aA(g)+bB(g)
cC(g)+dD(g),平衡后测得B气体的浓度为0.6 mol·L-1。恒温下,将密闭容器的容积扩大1倍,重新达到平衡后,测得B气体的浓度为0.4 mol·L-1。下列叙述中正确的是
A. 重新达到平衡时,D的体积分数减小 B. a+b<c+d
C. 重新达到平衡时,A气体的浓度增大 D. 平衡向右移动
难度: 中等查看答案及解析