-
用惰性电极电解下列各组中的三种电解质溶液,在电解的过程中,溶液的pH依次为升高、不变、降低的是( )
A. AgNO3 CuCl2 Cu(NO3)2 B. KCl Na2SO4 CuSO4
C. CaCl2 KOH NaNO3 D. HCl HNO3 K2SO4
难度: 中等查看答案及解析
-
下列有关能量的判断和表示方法正确的是( )
A. 由C(s,石墨)===C(s,金刚石) ΔH=+1.9 kJ,可知:石墨比金刚石更稳定
B. 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量更多
C. 由H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ/mol,可知:含1 mol/L CH3COOH的溶液与含1 mol/L NaOH的溶液混合,放出热量小于57.3 kJ
D. 2 g H2完全燃烧生成液态水放出285.8 kJ热量,则氢气燃烧的热化学方程式为H2(g)+1/2O2(g) =H2O(l) ΔH=-285.8 kJ/mol
难度: 中等查看答案及解析
-
100 mL 2 mol·L-1 H2SO4溶液与过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成H2的总量,可向反应物中加入适量( )
A. 硝酸钠溶液 B. NaCl固体 C. 硫酸铵固体 D. 硫酸钾溶液
难度: 中等查看答案及解析
-
反应A(g)+3B(g)===2C(g)+2D(g)在四种不同情况下的反应速率分别为①v(A)=0.45 mol·L-1·s-1 ②v(B)=0.6 mol·L-1·s-1 ③v(C)=0.4 mol·L-1·s-1④v(D)=0.45 mol·L-1·s-1。下列有关反应速率的比较中正确的是( )
A. ④>③=②>① B. ①>②>③>④ C. ①>④>②=③ D. ④>③>②>①
难度: 中等查看答案及解析
-
某化学反应其△H=+122 kJ/mol,∆S=—231 J/(mol·K),下列说法正确的是( )
A. 在任何温度下都不能自发进行 B. 在任何温度下都能自发进行
C. 仅在高温下自发进行 D. 仅在低温下自发进行
难度: 中等查看答案及解析
-
可逆反应2NO2
2NO+O2,在恒压密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n molO2的同时生成2n molNO2
②单位时间内生成n molO2的同时生成2n mol NO
③NO2、NO、O2 的物质的量浓度为2:2:1
④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态
A. ①③④ B. ②③⑤ C. ①④⑤ D. ①②③④⑤
难度: 中等查看答案及解析
-
下列事实不能用勒夏特列原理解释的是( )
A. 黄绿色的氯水光照后颜色变浅
B. 温度过高对合成氨不利
C. 由H2、I2蒸气、HI组成的平衡体系加压后颜色变深
D. 溴水中有平衡:Br2+ H2O
HBr+ HBrO,当加入AgNO3溶液后,溶液颜色变浅
难度: 中等查看答案及解析
-
在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)
zC(g),平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的体积扩大一倍,测得A的浓度变为0.15 mol/L,下列有关判断正确的是( )
A. x+y<z B. 平衡逆向移动 C. A的转化率降低 D. C的体积分数减小
难度: 中等查看答案及解析
-
某温度下,H2(g)+CO2(g)
H2O(g)+CO(g)的平衡常数K=9/4,该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示,
起始浓度
甲
乙
丙
c(H2)(mol/L)
0.010
0.020
0.020
c(CO2)(mol/L)
0.010
0.010
0.020
下列判断不正确的是( )
A. 平衡时,乙中H2的转化率大于60%
B. 平衡时,甲中和丙中H2的转化率均是60%
C. 平衡时,丙中c(CO)是甲中的2倍,是0.012 mol/L
D. 反应开始时,丙中的反应速率最快,甲中的反应速率最慢
难度: 中等查看答案及解析
-
常温下,下列四种溶液中,由水电离出的氢离子浓度之比为( )
①pH=0的盐酸 ②0.1 mol·L-1的盐酸③0.01 mol·L-1的NaOH溶液 ④pH=11的NaOH溶液
A. 1000∶100∶10∶1 B. 1∶10∶100∶1 000
C. 14∶13∶12∶11 D. 11∶12∶13∶14
难度: 中等查看答案及解析
-
如图是Zn和Cu形成的原电池,则下列结论中正确的是( )
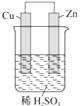
①铜为阳极,锌为阴极;②铜极上有气泡;③SO42-向铜极移动;④若有0.5 mol 电子流经导线,则可产生0.25 mol气体;⑤电子的流向是铜到锌;⑥正极反应式:Cu+2e-=Cu2+。
A. ①②③ B. ②④ C. ④⑤⑥ D. ④⑤
难度: 中等查看答案及解析
-
早在1807年化学家戴维用电解熔融氢氧化钠制得钠:4NaOH(熔融)
4Na+O2↑+2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为3Fe+4NaOH(熔融)
Fe3O4+2H2↑+4Na↑。下列有关说法正确的是( )
A. 电解熔融氢氧化钠制钠,阳极发生的电极反应为2OH--2e- =H2↑+O2↑
B. 盖·吕萨克法制钠原理是利用铁的还原性比钠强
C. 若戴维法与盖·吕萨克法制得等量的钠,则两反应中转移的电子总数也相同
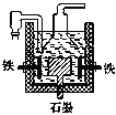
D. 目前工业上常用电解熔融氯化钠法制钠(如右图),电解槽中石墨为阳极,铁为阴极
难度: 中等查看答案及解析
-
500 mL KNO3和Cu(NO3)2的混合溶液中c(NO3-)= 6.0 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
A. 原混合溶液中c(K+)为1 mol·L-1 B. 上述电解过程中共转移2 mol电子
C. 电解得到的Cu的物质的量为0.5 mol D. 电解后溶液中c(H+)为4 mol·L-1
难度: 中等查看答案及解析
-
下列微粒在指定条件下可以大量共存的是( )
A. 在小苏打溶液中:NO3-、CO32-、NH4+、K+
B. 氢氧化铁胶体中:H+、K+、Cl-、S2-
C. 水电离出的c(H+)=10—12 mol/L的溶液中:Ca2+、K+、Cl-、HCO3-
D. 在pH=0的溶液中:Ca2+、ClO-、Cl-、Al3+
难度: 中等查看答案及解析
-
下列有机物用系统命名法命名正确的是( )
A.
2—乙基丙烷 B.
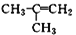 2—甲基—2—丙烯
2—甲基—2—丙烯C. CH3CH2CH2CH2OH 1−丁醇 D.
对二甲苯
难度: 中等查看答案及解析
-
下列各对物质中,互为同系物的是( )
A.
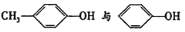 B.
B. 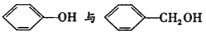
C. HCOOC2H5与CH3COOCH3 D. CH3—CH=CH2与
难度: 中等查看答案及解析
-
柠檬烯是一种食用香料,其结构简式如图所示。下列有关柠檬烯的说法不正确的是( )
A. 它的核磁共振氢谱有8组吸收峰
B. 它的分子中所有的碳原子不可能在同一平面上
C. 它和丁基苯(
)互为同分异构体
D. 一定条件下,它可以发生加成、取代、氧化等反应
难度: 中等查看答案及解析
-
下列说法不正确的是( )
A. 二溴乙烷和水、溴苯和水、硝基苯和水三对物质都能用分液漏斗进行分离
B. 苯不能使酸性高锰酸钾溶液褪色,但可以使溴水褪色
C. 甲苯与足量H2加成的产物的一氯代物有5种同分异构体
D. 利用核磁共振氢谱可以准确判断有机物分子中含有哪些官能团
难度: 中等查看答案及解析
-
为提纯下列物质(括号内为杂质),选用的试剂和分离方法都正确的是( )
物质
试剂
分离方法
①
乙烷(乙烯)
H2
催化剂加热
②
乙酸乙酯(乙酸)
饱和碳酸钠溶液
过滤
③
乙醇(水)
生石灰
蒸馏
④
溴苯(Br2)
CCl4
萃取分液
A. ①② B. ①③ C. ③④ D. 只有③
难度: 中等查看答案及解析
-
0.5mol 气态烃A 最多和1 mol HCl加成,生成氯代烷B,1mol B与4 mol Cl2 发生取代反应,生成只含碳、氯两种元素的化合物C,则A的分子式为( )
A. C2H4 B. C2H2 C. C3H4 D. C4H6
难度: 中等查看答案及解析


