-
为检验一种氮肥的成分,某学习小组的同学进行了以下实验:①加热氮肥样品生成两种气体,其中一种气体能使湿润的红色石蕊试纸变蓝,另一种气体能使澄清石灰水变浑浊。②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化。由此可知该氮肥的主要成分是
A. NH4HCO3 B. NH4Cl C. (NH4)2CO3 D. NH4NO3
难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是
A. 用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+
B. 氯气跟水反应:Cl2 + H2O= H+ + Cl- + HClO
C. 钠与水的反应:Na+H2O=Na++OH-+H2↑
D. AlCl3溶液中加入足量的氨水:Al3++ 3OH-══ Al(OH)3↓
难度: 简单查看答案及解析
-
下列有关试剂的保存方法,错误的是
A. 浓硝酸保存在无色玻璃试剂瓶中
B. 少量的钠保存在煤油中
C. 氢氧化钠溶液保存在带橡皮塞的玻璃试剂瓶中
D. 新制的氯水通常保存在棕色玻璃试剂瓶中
难度: 中等查看答案及解析
-
下列反应中水作为氧化剂的是
A. Cl2+H2O = HCl +HClO B. 3Fe+4H2O(g)
Fe3O4+4H2
C. 2F2+2H2O = 4HF+O2 D. 3NO2+H2O = 2HNO3+NO
难度: 中等查看答案及解析
-
下列物质既能与盐酸又能与氢氧化钠溶液反应的是
①Al ②Al2O3 ③ Al(OH)3 ④NaHCO3
A. ①② B. ②③ C. ①②③ D. ①②③④
难度: 中等查看答案及解析
-
下列说法正确的是
A. 硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
B. 蔗糖、硫酸钠和水分别属于非电解质、强电解质和弱电解质
C. 工业上用铝罐车装运浓硫酸和浓硝酸,说明铝与浓硫酸和浓硝酸不反应
D. 含0.2mol H2SO4的浓硫酸与足量的铜反应,生成标准状况下的气体2.24 L
难度: 中等查看答案及解析
-
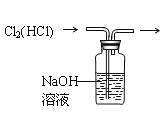
下列装置所示的实验中,能达到实验目的的是
A. 分离碘和酒精
B. 除去Cl2中的HCl
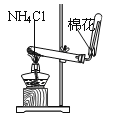
C. 实验室制氨气
 D. 排水法收集NO
D. 排水法收集NO难度: 中等查看答案及解析
-
某无色酸性溶液中,一定能够大量共存的离子组是
A. Fe2+、Ba2+、NO3-、Cl- B. Na+、NH4+、SO42-、Cl-
C. Na+、K+、HCO3-、NO3- D. Na+、K+、MnO4-、Br-
难度: 中等查看答案及解析
-
下列说法正确的是
A. 二氧化硫使溴水褪色利用了二氧化硫的还原性
B. 向饱和FeCl3溶液中滴加过量氨水,可制取Fe(OH)3胶体
C. 将润湿的红色石蕊试纸伸入瓶内,试纸变蓝则氨气已经收集满
D. 用蒸馏的方法分离植物油和水的混合物
难度: 中等查看答案及解析
-
括号内为杂质,除去下列物质中的杂质,选用试剂正确的是
A. NH3(水):浓硫酸 B. Na2CO3溶液(NaHCO3):CO2
C. FeCl2溶液(FeCl3):Fe粉 D. Al2O3(SiO2):NaOH溶液
难度: 中等查看答案及解析
-
下列用品的主要成分不正确的是
A
B
C
D
用品
水玻璃
“84”消毒液
小苏打
光导纤维
主要成分
Na2SiO3
NaClO
NaHCO3
Si
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
以下物质间不能通过单质与单质直接化合的是
A. FeCl2 B. NO
C. FeS D. CuCl2
难度: 中等查看答案及解析
-
用NA代表阿伏加德罗常数的值,下列有关说法正确的是
A. 1 mol Cl2中含有的原子数为NA
B. 标准状况下,22.4L SO3含有分子数NA
C. 常温常压下,46g NO2气体中含有的氧原子数为2NA
D. 钠在氧气中燃烧,1 mol O2作氧化剂时得到的电子数为4NA
难度: 中等查看答案及解析
-
纯二氧化硅可用下列流程制得.下列说法不正确的是

A. X可用作木材防火剂
B. 步骤Ⅱ的反应是Na2SiO3+H2SO4═H2SiO3(胶体)+ Na2SO4
C. 步骤Ⅱ中的稀硫酸可用CO2来代替
D. SiO2既能与盐酸反应,又能与氢氟酸反应,所以SiO2是两性氧化物
难度: 中等查看答案及解析
-
下列有关实验的操作或结论正确的是
实验
操作或结论
A.浓硫酸加入到蔗糖中
蔗糖变黑体现了浓硫酸的吸水性
B.实验室收集NO
可用排空气法收集
C.SO2通入高锰酸钾溶液
高锰酸钾溶液褪色,说明SO2具有漂白性
D.CCl4萃取碘水中的I2
先从分液漏斗下口放出有机层,后从上口倒出水层
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列反应产生氢气的物质的量最多的是
A. 足量的Mg与0.5mol·L-1的稀硝酸200mL
B. 足量的Cu与5mol·L-1的硫酸400mL
C. 足量的Al与0.3mol·L-1的氢氧化钠溶液200mL
D. 足量的Mg与0.5mol·L-1的稀盐酸200mL
难度: 中等查看答案及解析