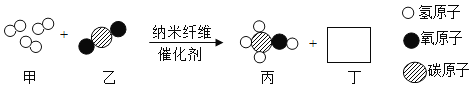
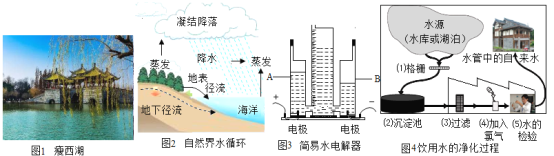
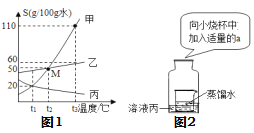
-
科学家最近用激光与高压冰的结合发现了一种新的水的存在方式,即水同时处于固态和液态,这种水被称为“超离子水”。下列有关“超离子水”的说法正确的是( )
A.超离子水和普通水的组成元素相同 B.超离子水属于混合物
C.超离子水中的水分子有的静止有的运动 D.超离子水和普通水的性质完全相同
难度: 简单查看答案及解析
-
我国古代文献记载中蕴含着丰富的化学知。下列记载中不涉及化学变化的是( )
A. 《易经》—“泽中有火,上火下泽”
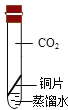
B. 《淮南万毕术》—“曾青得铁则化为铜”
C. 《抱朴子》—“丹砂(HgS)烧之成水银,积变又还成丹砂”
D. 《天工开物》—“侯潮一过,明月天睛,半日晒出盐霜”
难度: 简单查看答案及解析
-
下列观点不正确的是
A.使用元素符号、化学式等化学用语,是为了增加化学科学的神秘色彩
B.人们根据不同的需求,通过控制反应条件,促进或抑制化学反应
C.可通过鼓入空气,使燃料燃烧更充分
D.物质本身没有好与坏之分,而人们对物质的利用却存在合理与不合理之分
难度: 简单查看答案及解析
-
“钻石恒久远,一颗永留传”这句广告词被美国《广告时代》评为20世纪的经典广告之一,该广告词能体现的钻石性质是
A.密度大 B.不能导电 C.化学性质稳定 D.熔点低
难度: 简单查看答案及解析
-
下列符号中,既表示一个原子,又表示一种元素,还能表示一种物质的是:
A.He B.N2 C.H D.2O2
难度: 简单查看答案及解析
-
苏州盛产杨梅。杨梅中含有丰富的叶酸,对防癌抗癌有积极作用,其化学式为Cl9Hl9N7O6。下列有关叶酸的说法中正确的是
A. 叶酸的相对分子质量为441 g
B. 叶酸中氮元素的质量分数大于氧元素的质量分数
C. 叶酸中碳、氢、氮、氧四种元素质量比为19:19:7:6
D. 叶酸由19个碳原子、19个氢原子、7个氮原子和6个氧原子构成
难度: 中等查看答案及解析
-
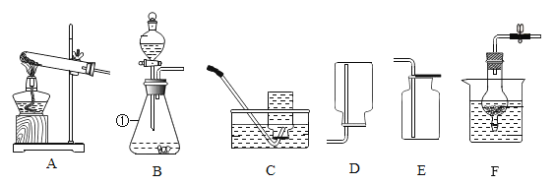
下列实验的操作或设计正确的是( )
A.药品取用:将试管竖直,垂直放入锌粒
B.区别物质:用pH试纸可以区别两种不同浓度的NaCl溶液
C.气体净化:除去CO2中混有的少量CO,可通入O2点燃
D.气体收集:CO2和O2密度比空气大,故都能用向上排空气法收集
难度: 简单查看答案及解析
-
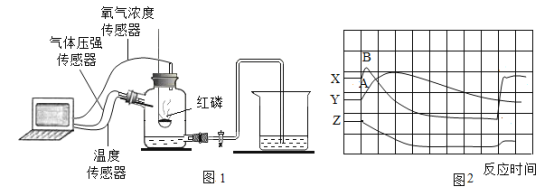
下列对化学实验现象的描述,不正确的是
A.硫在空气中燃烧产生淡蓝色火焰
B.铜绿受热后固体变成黑色,试管内壁有小液滴
C.细铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成黑色固体
D.蜡烛在氧气里燃烧生成二氧化碳和水
难度: 中等查看答案及解析
-
下列加热高锰酸钾制取氧气的部分操作示意图中,正确的是
A.
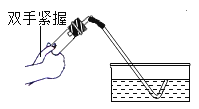 检查装置气密性 B.
检查装置气密性 B.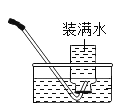 加热立即收集
加热立即收集C.
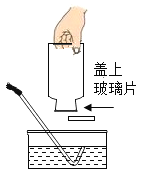 收满后移出集气瓶 D.
收满后移出集气瓶 D.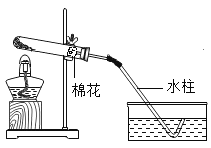 结束时停止加热
结束时停止加热难度: 中等查看答案及解析
-
下列各组物质,仅用水无法鉴别的是
A.KMnO4、I2 B.CaCl2、NaCl C.CaCO3、NH4HCO3 D.NH4NO3、NaCl
难度: 中等查看答案及解析
-
根据下列各组原子结构示意图,判断元素的化学性质相似的一组是( )
A.
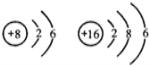 B.
B. 
C.
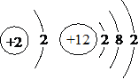 D.
D. 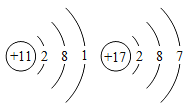
难度: 中等查看答案及解析
-
科学家用石墨烯薄膜制成“筛子”,可以筛掉盐类物质。当海水流过该膜时,钠离子和氯离子被水分子包裹而不能通过,独立的水分子却能通过(如图)。下列关于石墨烯膜“筛掉”氯化钠的说法错误的是( )

A.该过程属于物理变化
B.该过程可应用于海水淡化
C.“筛掉”氯化钠过程类似于过滤操作
D.海水经过“筛子”后,氯化钠的溶质质量分数增大
难度: 简单查看答案及解析
-
下图表示三种物质在密闭容器中反应前后质量比例的变化,下列说法正确的是
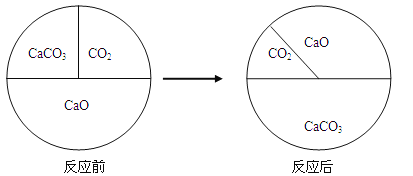
A.该反应中CaO起催化作用 B.该反应中CO2是生成物
C.该反应是复分解反应 D.该反应是化合反应
难度: 中等查看答案及解析
-
下列4个坐标图分别表示4个实验过程中某些质量的变化,其中正确的是( )
A
B
C
D
向一定量石灰石滴加稀盐酸
向一定量过氧化氢溶液加入少量二氧化锰
向相同铁粉和锌粉加入足量稀盐酸
向一定量硫酸铜溶液不断加入铁粉
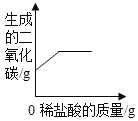
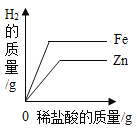
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
相同质量的镁、铝、锌分别与相同质量20%的盐酸充分反应,产生氢气质量(直接用各金属表示)大小关系有以下几种猜测,其中正确的是
A.Mg>Al>Zn B.Zn>Mg>Al
C.Al=Mg>Zn D.Al>Mg=Zn
难度: 困难查看答案及解析
-
实验室配制50g溶质质量分数为15%的氯化钠溶液。下列说法中错误的是
A.实验的步骤为计算、称取、量取、溶解
B.溶解过程中玻璃棒的作用是搅拌,以加快氯化钠的溶解速率
C.把配制好的氯化钠溶液倒入刚用蒸馏水洗过的试剂瓶中,并贴上标签
D.量取水时,用规格为50mL的量筒量取42.5mL蒸馏水
难度: 中等查看答案及解析
-
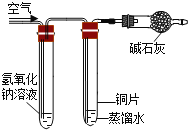
英国科学家瑞利在研究氮气的密度时,重复多次发现除去空气中的O2与CO2得到的N2样品的密度总是大于纯N2的密度(同温同压下等体积的不同气体含有相同的分子数)。你认为样品中含哪种气体可解释该结果
A.氦气 B.氩气 C.甲烷 D.水蒸气
难度: 中等查看答案及解析
-
氮气和氢气在一定条件下化合生成氨气。工业上合成氨的主要流程如图所示(已知:同等条件下气体体积比等于其分子个数比)。下列说法不正确的是
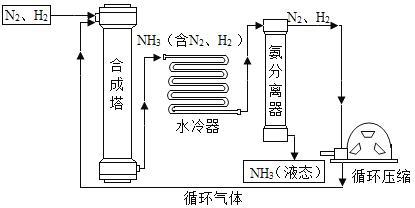
A.流程中可循环利用的物质只有氮气
B.由图中可知氨气的沸点高于氮气和氢气
C.氨气由气态变为液态,分子间空隙变小
D.理论上通入合成塔内的氮气和氢气的体积比应为1:3
难度: 中等查看答案及解析