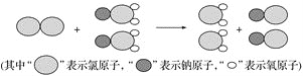
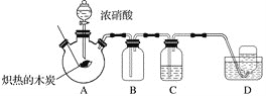
-
下列过程中化学反应速率的加快对人类有益的是( )
A. 金属的腐蚀 B. 食物的腐败
C. 塑料的老化 D. 氨的合成
难度: 简单查看答案及解析
-
将5 mol·L-1的盐酸10 mL稀释到200mL,再取出5 mL,这5 mL溶液的物质的量浓度是( )
A. 0.05 mol·L-1 B. 0.25 mol·L-1 C. 0.1 mol·L-1 D. 0.5 mol·L-1
难度: 简单查看答案及解析
-
下列变化过程中,画横线的元素被氧化的是( )
A. CO2→CO B. FeCl3→FeCl2
C. HCl→AgCl D. KI→I2
难度: 简单查看答案及解析
-
有下列氧化物:①FeO、②Fe2O3、③Fe3O4、④CuO,其中颜色相同的是( )
A. ①②③ B. ①②④ C. ②③④ D. ①③④
难度: 简单查看答案及解析
-
电解质电离时一定相等的是( )
A. 阴离子与阳离子的总数 B. 阳离子和阴离子的质量
C. 正电荷总数和负电荷总数 D. 每个阳离子和阴离子所带电荷数
难度: 中等查看答案及解析
-
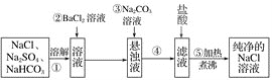
提纯含有少量Ba(NO3)2杂质的KNO3溶液,可以使用的方法为( )
A. 加入过量碳酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
B. 加入过量硫酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
C. 加入过量碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
D. 加入过量硫酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
难度: 中等查看答案及解析
-
下列叙述中,正确的是
A. 自然界中存在大量的单质硅
B. 石英、水晶、硅石的主要成分都是二氧化硅
C. 二氧化硅的化学性质活泼,能跟酸或碱的溶液发生化学反应
D. 自然界中硅元素都存在于石英中
难度: 简单查看答案及解析
-
下列叙述正确的是( )
①两种原子构成的共价化合物分子中的化学键都是极性键 ②两种不同非金属元素原子间形成的化学键都是极性键 ③含有非极性键的化合物一定是共价化合物 ④只要是离子化合物,其熔点就比共价化合物的熔点高 ⑤难失去电子的原子,易形成阴离子 ⑥单质分子中不存在化学键,化合物分子中才存在化学键 ⑦离子化合物中一定含有离子键
A. ②⑦ B. ③⑦ C. ⑦ D. ①⑤⑦
难度: 中等查看答案及解析
-
下列实验现象的描述正确的是( )
A. 氢气在氯气中燃烧,发出苍白色火焰,瓶口上方有白色烟雾
B. 铜在氯气中燃烧,产生棕黄色烟,产物溶于水,溶液呈蓝绿色
C. 铁丝在氯气中燃烧,产生红色的浓烟,产物溶于水,溶液呈浅绿色
D. 钠在空气中燃烧,发出黄色的火焰,生成白色固体
难度: 简单查看答案及解析
-
称取(NH4)2SO4和NH4HSO4混合物样品7.24g,加入含0.1molNaOH的溶液,完全反应后加热,生成NH31792mL(标准状况),则下列说法正确的是( )
A. NaOH只与NH4HSO4反应
B. (NH4)2SO4在水中的电离方程式:(NH4)2SO4=NH4++2SO42-
C. NH4HSO4的物质的量是0.04 mol
D. (NH4)2SO4和NH4HSO4物质的量之比是1.87∶1
难度: 中等查看答案及解析
-
下列各项正确的是( )
A. 镁、铝与沸水不可能反应
B. 铁在一定条件下可以与水反应
C. 钠与水反应的离子方程式:Na+H2O=Na++OH-+H2↑
D. 钠和硫酸铜溶液反应的离子方程式:2Na+Cu2+=2Na++Cu
难度: 简单查看答案及解析
-
同温同压下,等质量的氧气和二氧化碳相比较,下列叙述正确的是( )
A. 质子数之比为1∶1 B. 密度比为11∶8
C. 物质的量之比为8∶11 D. 原子个数比1∶1
难度: 简单查看答案及解析
-
下列说法不正确的是( )
A. 氯元素在自然界中存在游离态,只是量极少
B. 海水中的氯元素主要以氯化钠等盐的形式存在
C. 人体的血液中含有氯化钠,其浓度大约为0.9%
D. 氯化钠对维持人体的生理功能有着重要作用
难度: 简单查看答案及解析
-
在某100 mL混合液中,HNO3和H2SO4的物质的量浓度分别是0.4 mol·L-1和0.1 mol·L-1。向该混合溶液中加入1.92 g铜粉,加热,待充分反应后(假设反应前后溶液体积不变),所得溶液中Cu2+的物质的量浓度是( )
A. 0.15 mol·L-1 B. 0.225 mol·L-1 C. 0.35 mol·L-1 D. 0.45 mol·L-1
难度: 困难查看答案及解析
-
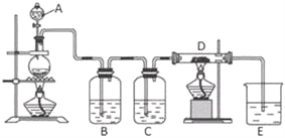
利用下列装置可以制备无水氯化铁。下列有关说法正确的是( )
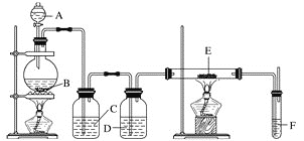
A. 烧瓶B中制备氯气的反应物为MnO2和稀盐酸
B. 装置C、D中分别盛有浓硫酸、饱和食盐水
C. 装置E和装置F之间需要增加一个干燥装置,才能制得无水氯化铁
D. 装置F的目的是检验有无氯气逸出
难度: 简单查看答案及解析
-
氰气的化学式为(CN)2,它的性质和卤素相似,称为拟卤素。对其性质和有关化合物性质的叙述不正确的是( )
A. NaCN和AgCN都易溶于水 B. HCl和HCN都易形成白雾
C. MnO2可与HCN反应生成(CN)2 D. (CN)2和NaOH溶液反应生成NaCN、NaCNO和H2O
难度: 中等查看答案及解析
-
配制一定物质的量浓度的KOH溶液时,导致浓度偏低的原因可能是( )
A. 用敞口容器称量KOH且时间过长
B. 配置前先向容量瓶中加入少量蒸馏水
C. 容量瓶盛过KOH溶液,使用前未洗涤
D. 溶解后快速转移到容量瓶,然后加足量蒸馏水,定容
难度: 中等查看答案及解析
-
既可用于给液体加热,又可用于给固体加热的玻璃仪器是( )
A. 试管 B. 烧瓶 C. 烧杯 D. 蒸发皿
难度: 简单查看答案及解析
-
最新科技报道,美国夏威夷联合天文中心的科学家发现了新型的氢粒子,这种粒子是由3个氢原子核(没有中子)和2个电子构成。对这种粒子,下列说法中正确的是( )
A. 是氢的一种新单质 B. 是氢的一种新的同位素
C. 它的组成可用H3表示 D. 它比普通H2分子多一个氢原子核
难度: 简单查看答案及解析
-
不具有放射性的同位素称之为稳定同位素,稳定同位素分析法近20年来在植物生理学、生态学和环境科学研究中获得广泛应用。如在陆地生态系统研究中,2H、13C、15N、18O、34S等常用作环境分析指示物。下列有关说法正确的是( )
A. 34S原子核内中子数为16
B. 1H216O和1H218O的相对分子质量不同
C. 13C和15N原子核内的质子数相差2
D. 2H+结合OH-的能力比1H+的更强
难度: 简单查看答案及解析
-
在密闭容器中,A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示,且v(A)、v(B)、v(C)之间有以下关系:v(B)=3v(A)、3v(C)=2v(B),则此反应可表示为( )
A. 2A+3B=2C B. A+3B=2C
C. 3A+B=2C D. 3A+B=C
难度: 简单查看答案及解析
-
M、R均为主族元素,已知M的一个原子失去2个电子,R的一个原子得到1个电子后形成稀有气体元素的电子层结构。下列关于M与R形成的化合物的叙述正确的是( )
A. M与R可以形成MR2型离子化合物
B. 在MR2中M的离子半径比R的离子半径大
C. 形成的两种离子分别是M+和R2-
D. MR2的电子式为
难度: 简单查看答案及解析
-
一定条件下,碘单质与砹单质以等物质的量进行反应可得AtI。它与Zn、NH3都能发生反应,化学方程式分别如下:2AtI+2Zn=ZnI2+ZnAt2,AtI+2NH3(l)=NH4I+NH2At。下列关于AtI性质的叙述正确的是( )
A. ZnI2既是氧化产物,又是还原产物
B. ZnAt2既是氧化产物,又是还原产物
C. AtI与液氨反应,AtI既是氧化剂,又是还原剂
D. AtI与液氨反应,是自身氧化还原反应
难度: 简单查看答案及解析
-
X、Y-、Z2+三种微粒的电子层结构相同,则一定不能再相等的是( )
A. 中子数 B. 质量数 C. 电子数 D. 核电荷数
难度: 简单查看答案及解析