-
化学在很多领域中发挥着重要的作用,下列说法正确的是
A. 实验室里熔化氢氧化钠时,可选用石英坩埚和铁坩埚
B. 家庭用食醋代替CO2来增强漂白粉溶液的漂白性
C. 纯铁易被腐蚀,可以在纯铁中混入碳制成“生铁”,以提高其抗腐蚀能力
D. 生活中用明矾净水只包含物理变化
难度: 中等查看答案及解析
-
饮茶是中国人的传统饮食文化之一。为方便饮用,可通过以下方法制取罐装饮料茶:
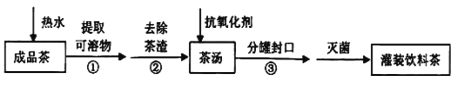
关于上述过程涉及的实验方法、实验操作和物质作用说法不正确的是
A. 使用热水可以加快溶解速率
B. ②是过滤
C. ③是分液
D. 维生素C可作抗氧化剂
难度: 中等查看答案及解析
-
NA为阿伏加德罗常数的值,下列说法正确的是
A. 78g Na2O2与足量SO2反应,转移电子数为NA
B. 标准状况下,11.2L的HF中含有 H—F键的数目为0.5NA
C. 100g CaS与CaSO4的混合物中含有32g硫,则含有的氧原子数为1.75NA
D. 一定温度下,1L0.5mol·L-1NH4Cl溶液与2L0.25mol·L-1NH4Cl溶液含有NH4+的物质的量相同
难度: 中等查看答案及解析
-
短周期主族元素W、X、Y、Z的原子序数依次增大,它们的原子最外层电子数总和等于Z的原子序数,由这四种元素组成一种化合物M具有如下性质下列推断正确的是
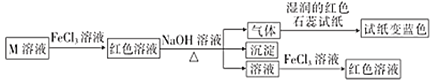
A. 原子半径:Z>Y>X>W
B. 最高价氧化物对应的水化物酸性:Y>X
C. 简单阴离子的还原性:W<Z
D. W、Y、Z组成的化合物只含共价键
难度: 中等查看答案及解析
-
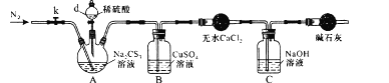
下列实验目的、装置、现象及对应发生反应的方程式均正确的是
选项
目的
装置
现象
方程式
A
验证SO2性质
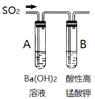
A中出现浑浊;
B中颜色变浅
A:SO2+Ba2++2OH-=BaSO3↓+H2O
B:5SO2+2H2O+2MnO4—
=5SO42—+2Mn2++4H+
B
鉴别Br2(g)与NO2(g)

通NO2所得溶液无色;通Br2所得溶液呈黄色
3NO2+H2O=2HNO3+NO
Br2+H2O=2H++Br-+BrO-
C
检验Fe3+
滴加铁氰化钾溶液,产生蓝色沉淀
2Fe3++3[Fe(CN)4]2-=Fe2[Fe(CN)4]3↓
D
探究浓度对反应速率的影响
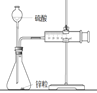
注射器中收集到气体,测定收集一定体积气体所需时间
Zn+H2SO4=ZnSO4+H2↑
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
某课题组以纳米Fe2O3作为电极材料制备锂离子电池(另一极为金属锂和石墨的复合材料),通过在室温条件下对锂离子电池进行循环充放电,成功地实现了对磁性的可逆调控(如图)。下列说法错误的是
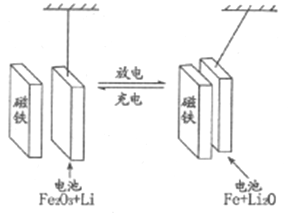
A. 放电时,负极的电极反应式为Li-e-=Li+
B. 放电时,电子通过电解质从Li流向Fe2O3
C. 充电时,Fe做阳极,电池逐渐摆脱磁铁吸引
D. 充电时,阳极的电极反应式为2Fe+3Li2O-6e-= Fe2O3+6Li+
难度: 中等查看答案及解析
-
在25℃时,将1.0L w mol・L-1CH3COOH溶液与0.1molNaOH固体混合,充分反应。然后向混合液中加入CH3COOH或 CH3COONa固体(忽略溶液体积和温度变化),溶液pH变化如图所示。下列叙述正确的是
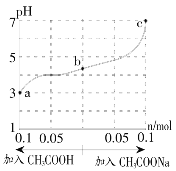
A. a、b、c对应的溶液中,水的电离程度由大到小的顺序是:c>a>b
B. w≥0.1
C. 从b到a的过程中,[c(Na+)·c(OH-)]/c(CH3COO-)增大
D. 25℃时,CH3COOH的电离平衡常数
难度: 中等查看答案及解析
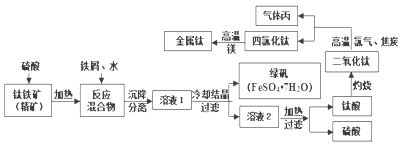
 FeCO3达到沉淀溶解平衡时,室温下测得溶液的pH为8,c(Fe2+)为1.0×10-5 mol/L。请通过计算判断所得FeCO3固体中是否混有Fe(OH)2_____(已知: Ksp[Fe(OH)2] = 4.9×10-17)
FeCO3达到沉淀溶解平衡时,室温下测得溶液的pH为8,c(Fe2+)为1.0×10-5 mol/L。请通过计算判断所得FeCO3固体中是否混有Fe(OH)2_____(已知: Ksp[Fe(OH)2] = 4.9×10-17)