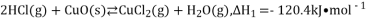-
下列属于吸热反应的是
A. 氧化钙与水反应 B. 铁丝在氧气中燃烧
C. NaOH溶液与盐酸反应 D. Ba(OH)2·8H2O晶体与NH4Cl晶体反应
难度: 简单查看答案及解析
-
垃圾分类并回收利用,可以节约自然资源,符合可持续发展的要求。与废弃矿泉水瓶对应的垃圾分类标志是
A.
 B.
B.  C.
C.  D.
D. 
难度: 简单查看答案及解析
-
在48mL0.1mol/LHNO3溶液中加入12mL0.4mol/LKOH溶液时,所得到的溶液呈
A.弱酸性 B.强酸性 C.碱性 D.中性
难度: 中等查看答案及解析
-
为了除去
,酸性溶液中的
,可在加热搅拌的条件下加人一种试剂,过滤后,再向滤液中加入适量盐酸。这种试剂是 ( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
工业合成氨的反应原理为:
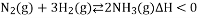 ,下列措施既能加快反应速率又能提高产率的是 ( )
,下列措施既能加快反应速率又能提高产率的是 ( )A. 升高温度 B. 分离出
C. 增大压强 D. 使用催化剂
难度: 简单查看答案及解析
-
氧化亚铜常用于制船底防污漆。用CuO与Cu高温烧结可制取
,已知反应:
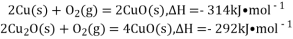
则
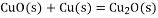 的
的等于
A.
B.
C.
D.
难度: 简单查看答案及解析
-
铅蓄电池是最常用的二次电池,其反应方程式为:
.
则充电时
( )
A. 在阳极生成 B. 在阴极生成
C. 在两个电板上生成 D. 在两个电板上除去
难度: 简单查看答案及解析
-
某同学运用电解原理实现在铁棒上镀铜,设计如图装置,下列判断不正确的是 ( )
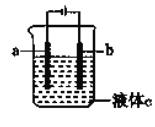
A. a是铁
B. 液体c可用硫酸铜溶液
C. 该实验过程中
基本保持不变
D. b上发生反应的方程式为
难度: 中等查看答案及解析
-
用电解的方法分析水的组成时,需向水中加人电解质,不宜选用的是 ( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
在定温定容的密闭容器中合成
。下列不能说明反应2SO2(g)+O2(g)
2SO3(g)达到化学平衡状态的是 ( )
A.
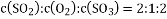
B. 容器内的压强不再改变
C. SO3的生成速率与SO2 的生成速率相等
D. SO2 的转化率不再改变
难度: 简单查看答案及解析
-
下列实验事实不能用平衡移动原理解释的是 ( )
A. 升高温度水的离子积增大
B. 镁条与氯化铵溶液反应生成氢气
C. 碳酸钙与稀盐酸反应生成二氧化碳
D. 加入少量硫酸铜可增大锌与稀硫酸反应的速率
难度: 中等查看答案及解析
-
下列事实能说明醋酸是弱电解质的是 ( )
A. 醋酸能使石蕊溶液变红
B.
时.
醋酸的pH约为3
C. 向醋酸中加入氢氧化钠溶液,溶液pH增大
D. 醋酸能与碳酸钙反应产生
气体
难度: 简单查看答案及解析
-
关于
溶液,下列判断不正确的是 ( )
A. 粒子种类与
溶液相同
B. 升高温度,
增大
C. 加入
溶液,
减小
D.
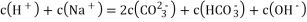
难度: 中等查看答案及解析
-
实验:①将
溶液和
溶液等体积混合得到浊液;②取少量①中浊液,滴加
溶液,出现红褐色沉淀;③将①中浊液过滤取少量白色沉淀,滴加
溶液.沉淀变为红褐色。下列说法中,不正确的是 ( )
A. 将①中浊液过滤,所得滤液中含少量
B. ①中浊液存在平衡:
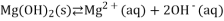
C. ②中沉淀颜色变化说明
转化为
D. ③可以证明
,比
更难溶
难度: 中等查看答案及解析
-
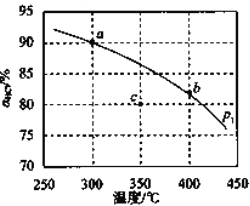
运用反应原理
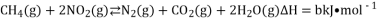 可设计清除氮氧化物的污染。在温度
可设计清除氮氧化物的污染。在温度和
时,分别将
和
,充入体积为1L的密闭容器中,测得
随时间变化如图。下列说法正确的是 ( )
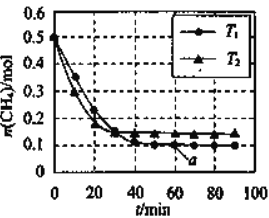
A.
B.
C. a点时
的转化率为
D. 温度为
,达平衡时反应的热效应为
难度: 困难查看答案及解析
-
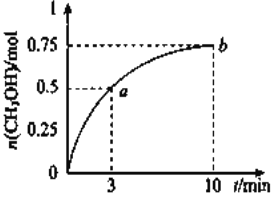
某温度下,在容积为1L的密闭容器中充入
和
发生
 测得
测得的物质的量随时间的变化如图所示,(已知,此温度下,该反应的平衡常数
)下列说法正确的是 ( )
A.
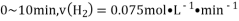
B. 点b所对应的状态为化学平衡状态
C.
的生成速率,点a低于点b
D. 欲增大平衡状态时
,可保持其他条件不变,升高温度
难度: 困难查看答案及解析
-
用石墨电极电解饱和食盐水的原理示意图如图所示。下列说法正确的是 ( )
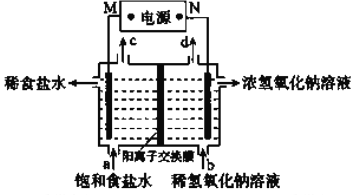
A. M为负极
B. 通电使氯化钠发生电离
C. c出口收集到的物质是氯气
D. 电解一段时间后,阴极区pH降低
难度: 中等查看答案及解析
-
下列关于金属保护的说法不正确的是 ( )
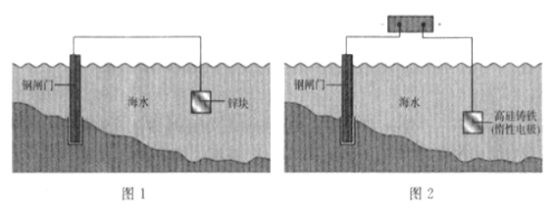
A. 图1是牺牲阳极阴极保护法,图2是外加电流阴极保护法
B. 钢闸门均为电子输入的一端
C. 锌和高硅铸铁的电板反应均为氧化反应
D. 两图所示原理均发生了反应:
难度: 简单查看答案及解析
-
丙烯是重要的有机化工原料。以丁烯和乙烯为原料反应生成丙烯的方法被称为“烯烃歧化法”,主要反应为
已知相关燃烧热数据:
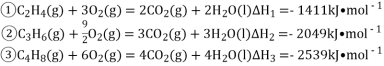
下列说法不正确的是 ( )
A. 消耗等物质的量的原料,反应③的放热最显著
B. 放出相等的热量,反应①产生的
最少
C. “烯烃歧化“反应中消耗
,放热
D. “烯烃歧化”反应中断键吸收的能量比成键放出的能量多
难度: 中等查看答案及解析
-
已知:
时
化学式
电离平衡常数
下列说法正确的是 ( )
A. 醋酸稀释过程中,
逐渐减小
B.
溶液中:
C. 向醋酸或HCN溶液中加入
,均产生
D. 物质的量浓度相同时

难度: 困难查看答案及解析
-
常温时,用
滴定
某一元酸HX,滴定过程中pH变化曲线如图所示。
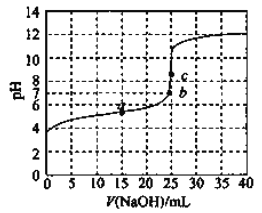
下列说法正确的是
A. HX溶液显酸性的原因是
B. 点a,
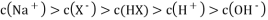
C. 点b,
与
恰好完全反应
D. 点c,
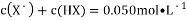
难度: 中等查看答案及解析

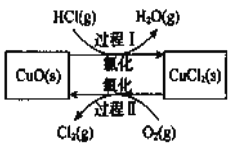
 分别溶于10mL蒸馏水或10mL
分别溶于10mL蒸馏水或10mL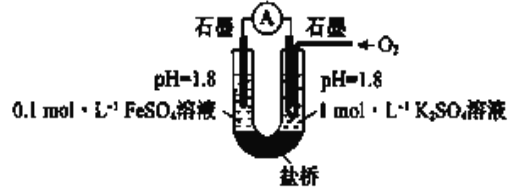
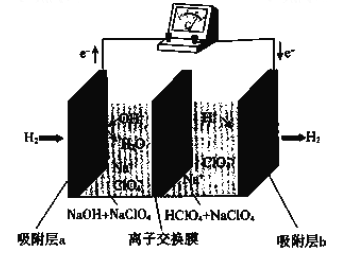
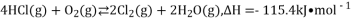 。该反应分两步进行,其基本原理如下图所示:
。该反应分两步进行,其基本原理如下图所示: