-
依据国家相关法律规定,自2011年5月1日起,机动车驾驶员醉驾将受到刑事处罚. 检测驾驶员是否酒后驾车,可用一种装有重铬酸钾(K2Cr2O7)的仪器.在K2Cr2O7中铬元素(Cr)的化合价是( )
A. +2 B. +3 C. +6 D. +7
难度: 简单查看答案及解析
-
在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如表所示,下列说法不正确的是( )
物质
X
Y
Z
W
反应前质量/g
10
3
90
0
反应后质量/g
3.2
3
待测
3.2
A.W可能是单质
B.Y可能是催化剂
C.该反应是分解反应
D.反应后Z物质的质量为86.4g
难度: 中等查看答案及解析
-
千姿百态的物质世界存在着多种相互作用,也不断发生变化。下列变化属于化学变化的是
A.冰雪融化 B.玻璃破碎
C.车胎爆炸 D.食物腐烂
难度: 简单查看答案及解析
-
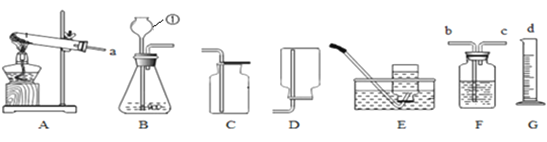
正确的实验操作对实验结果、人身安全非常重要.下列实验操作正确的是(
A.
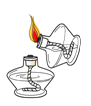 点燃酒精灯 B.
点燃酒精灯 B. 滴加液体 C.
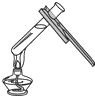 加热液体 D.
加热液体 D. 读取液体体积
难度: 简单查看答案及解析
-
下列变化既属于氧化反应,又属于化合反应的是:
A. 丙烷 + 氧气
二氧化碳+水
B. 高锰酸钾
锰酸钾 + 二氧化锰 + 氧气
C. 一氧化碳+ 氧气
二氧化碳
D. 酒精+ 氧气
二氧化碳 + 水
难度: 简单查看答案及解析
-
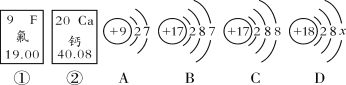
我国南海海底蕴藏着丰富的锰结核﹣﹣含有锰、铁、铜等金属的矿物.已知锰原子的质子数为25,相对原子质量为55,则锰原子的电子数为( )
A. 25 B. 30 C. 55 D. 80
难度: 简单查看答案及解析
-
生活中常接触到“加碘食盐”、“高钙牛奶”,其中的“碘”和“钙”应理解为
A.元素 B.分子 C.单质 D.原子
难度: 简单查看答案及解析
-
煤气中加入有特殊气味的乙硫醇可提示煤气是否泄漏。乙硫醇(用X表示)燃烧时发生的反应为:
,则X是( )
A.C4H12S2
B.C2H6S
C.C2H6O2
D.C2H6
难度: 简单查看答案及解析
-
下列各图中
和
分别表示不同元素的原子,则其中表示化合物的是( )
A.
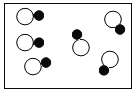 B.
B.C.
D.
难度: 中等查看答案及解析
-
逻辑推理是化学中常用的学习思维方法,以下推理方法正确的是( )
A.单质都是由一种元素组成的,所以由一种元素组成的物质一定是单质
B.氧化物含有氧元素,所以含氧元素的化合物都是氧化物
C.有新物质生成的变化一定是化学变化,所以化学变化一定有新物质生成
D.金属元素原子最外层电子一般少于4个,所以最层电子数少于4个的一定是金属元素
难度: 中等查看答案及解析