-
空气中含量最多的物质是
A. 氧气 B. 氮气
C. 水蒸气 D. 稀有气体
难度: 简单查看答案及解析
-
常见物质中属于纯净物的是
A. 纯碱 B. 天然气
C. 矿泉水 D. 食醋
难度: 简单查看答案及解析
-
市场销售的加铁酱油、加铁麦片、加碘食盐等物质中的铁和碘指的是
A. 原子 B. 分子
C. 元素 D. 单质
难度: 简单查看答案及解析
-
加水能形成溶液的是
A. 牛奶 B. 白糖
C. 面粉 D. 植物油
难度: 简单查看答案及解析
-
不属于有机物的是
A. 淀粉 B. 一氧化碳
C. 酒精 D. 葡萄糖
难度: 简单查看答案及解析
-
属于同素异形体的一组物质是
A. 冰和干冰 B. 氧气和液氧
C. 红磷和白磷 D. 汞和水银
难度: 简单查看答案及解析
-
交警常用重铬酸钾K2Cr2O7查酒驾,其中Cr元素的化合价是
A. +2 B. +4
C. +6 D. +7
难度: 简单查看答案及解析
-
某同学测得生活中常见物质的pH如下表,其中能使紫色石蕊试液变红的物质是
物质
牙膏
肥皂水
橘汁
草木灰水
食盐水
pH
8.2
9.2
3.5
10.6
7.0
A. 食盐水 B. 牙膏
C. 草木灰 D. 橘汁
难度: 简单查看答案及解析
-
物质的俗称与化学式不相符合的是
A. 干冰CO2 B. 苛性钠 NaOH
C. 熟石灰 Ca(OH)2 D. 石碱 Na2CO3
难度: 简单查看答案及解析
-
下列物质中只含有游离态氧元素的是
A. 空气 B. 水
C. 臭氧 D. 四氧化三铁
难度: 简单查看答案及解析
-
火箭发射时燃料燃烧的反应为 2X +N2O4
3N2+ 4H2O,其中X的化学式是
A. N2 B. N2H4
C. NH3 D. NO2
难度: 中等查看答案及解析
-
属于化学变化的是
A. 呼吸 B. 焰色反应
C. 干冰降雨 D. 用砂皮纸去金属锈
难度: 简单查看答案及解析
-
属于可溶性碱的是
A. Mg(OH)2 B. KOH
C. Cu(OH)2 D. Al(OH)3
难度: 简单查看答案及解析
-
下列实验基本操作中正确的是
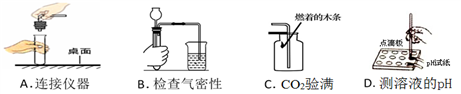
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列实验现象描述不正确的
A. 铁丝在氧气中燃烧,火星四射,生成黑色固体
B. 铁丝插入盐酸中,有气泡产生,溶液呈黄色
C. 红磷在空气中燃烧,产生大量白烟
D. 盐酸滴入氢氧化钠溶液中,无明显现象
难度: 中等查看答案及解析
-
下列化学方程式符合事实且书写正确的是
A. 2NaOH+SO2→Na2SO4+H2O
B. 2Fe + 6HCl →2FeCl3 + 3H2↑
C. K2CO3+2HCl→2KCl+H2CO3
D. Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
难度: 简单查看答案及解析
-
关于物质的量描述正确的是
A. 摩尔是基本物理量之一
B. 1摩尔任何物质都含有6.02×1023个构成微粒
C. 1摩尔O2的质量是32g/mol
D. 0.5molH2SO4中含有3.5mol原子
难度: 中等查看答案及解析
-
如下图所示进行实验,容器I、II体积相同,装置气密性良好,实验开始前红墨水左右两端液面相平。实验时同时将针筒内溶质质量分数相同且足量的稀硫酸全部迅速注入容器中,实验操作如下表:
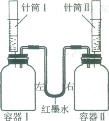
实验编号
容器Ⅰ
针筒Ⅰ
容器Ⅱ
针筒Ⅱ
甲
0.01mol镁
15mL稀硫酸
0.01mol 锌
15mL稀硫酸
乙
0.01mol锌
15mL稀硫酸
0.01mol铝
15mL稀硫酸
丙
0.01mol铜
15mL稀硫酸
0.01molg锌
15mL稀硫酸
实验结束红墨水左右两端液面呈现左高右低。能符合该实验现象的实验编号为
A. 甲、乙 B. 甲、丙
C. 乙、丙 D. 甲、乙、丙
难度: 中等查看答案及解析
-
已知某混合液由HCl、Na2CO3、H2SO4、FeCl3溶液中的两种混合而成,向该混合液中加Ba(OH)2溶液,产生沉淀量与加入的Ba(OH)2溶液体积关系如图,该混合液的组成是

A. HCl、FeCl3 B. HCl、Na2CO3
C. H2SO4、FeCl3 D. HCl、H2SO4
难度: 中等查看答案及解析
-
取5.0克氧化镁与氧化铜的混合物,加入稀盐酸(含0.2mol的HCl),恰好完全反应生成盐和水,原混合物中金属元素的质量是
A. 4.8g B. 3.4g C. 3.2g D. 2.4g
难度: 中等查看答案及解析