-
为纪念日军侵华战争中死难的中国同胞,中国政府设立12月13日为国家公祭日。在侵华史上,日军曾使用芥子气(化学式C4H8Cl2S)屠杀中国军民,下列对芥子气的说法正确的是
A. 有机物 B. 碱 C. 盐 D. 单质
难度: 简单查看答案及解析
-
氧元素有16O,17O,18O三种核素,下列对18O 的叙述正确的是
A. 质子数为10 B. 质量数为18
C. 电子数为18 D. 中子数为18
难度: 简单查看答案及解析
-
下列关于二氧化硫的说法正确的是
A. 无色无味 B. 密度比空气小 C. 可用排水法收集 D. 有毒
难度: 简单查看答案及解析
-
下列物质中含有共价键的离子化合物的是
A. Cl2 B. H2O C. NaCl D. NH4Cl
难度: 简单查看答案及解析
-
下列语句描绘的变化不属于化学变化的是
A. 蛋白质变性 B. 油脂水解 C. 滴水成冰 D. 钢铁吸氧腐蚀
难度: 简单查看答案及解析
-
下列互为同分异构体的一组是
A. 12C和14C B. C2H6和CH4
C. O2和O3 D. CH3CH2OH和CH3OCH3
难度: 简单查看答案及解析
-
化学与生活密切相关。下列生活中常见物质与化学式相对应的是
A. 明矾:KAl(SO4)2 B. 水玻璃:CaSiO3
C. 酒精——C2H5OH D. 小苏打:Na2CO3
难度: 简单查看答案及解析
-
下列是吸热反应的是
A. Mg+Cl2
MgCl2 B. NaOH+HCl = H2O+NaCl
C. CaCO3
CO2↑+CaO D. 2Na+2H2O=2NaOH+H2↑
难度: 简单查看答案及解析
-
在强碱性溶液中还可能大量存在的离子是
A. Ba2+ B. Al3+ C. NH4+ D. Fe2+
难度: 简单查看答案及解析
-
下列有关物质用途的说法错误的是
A. 液氯可以保存在钢瓶中
B. 二氧化硫具有漂白性,可以用来加工食品,使食品增白
C. 可用铁质容器盛装冷的浓硝酸
D. 液氨常用作制冷剂
难度: 中等查看答案及解析
-
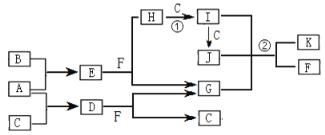
不能实现下列物质间直接转化的元素是
单质
氧化物
酸或碱
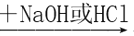 盐
盐A. 钠 B. 碳 C. 硫 D. 铝
难度: 中等查看答案及解析
-
影响化学反应速率的因素很多,下列措施能加快化学反应速率的是
A. 增大反应物的用量 B. 升高温度 C. 减小压强 D. 降低反应物浓度
难度: 简单查看答案及解析
-
下列关于乙烯的说法正确的是
A. 易溶于水 B. 1 mol乙烯可以加成2mol氢气
C. 易发生取代反应 D. 能使酸性高锰酸钾褪色
难度: 中等查看答案及解析
-
下列叙述正确的是
A. 乙酸的结构简式为:C2H4O2 B. 硫离子的结构示意图为:
C. NaHCO3电离:NaHCO3=Na++H++CO32- D. H2O的电子式:
难度: 中等查看答案及解析
-
有关Fe2O3+3CO
2Fe+3CO2的反应,下列说法正确的是
A. 该反应是置换反应 B. CO是氧化剂
C. CO2是氧化产物 D. 该反应有56gCO参与反应时,电子转移6mol
难度: 中等查看答案及解析
-
下列有关实验原理或操作正确的是
图1
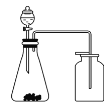 图2
图2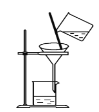
A. 选择合适的试剂,用图1所示装置可制取和收集少量CO2、NO和O2
B. 实验室制备氢氧化铝时,可向硫酸铝溶液中逐滴加入稀氨水
C. 可用图 2装置分离碘和四氯化碳溶液
D. 配制100mL 0.1 mol/L NaCl溶液时,用托盘天平准确称取NaCl固体5.85g
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值。下列判断正确的是
A. 活泼金属与盐酸反应置换生成1mol H2时,转移电子数是2NA
B. 22.4 L氢气中,含有的氢原子数是2NA
C. 1mol/L的K2SO4溶液中含有的钾离子的物质的量浓度为0.5mol/L
D. 在常温常压下,28g CO气体中含有的原子数是NA
难度: 中等查看答案及解析
-
下列离子方程式正确的是
A. 铝与氢氧化钠溶液反应:2Al+2OH-+2H2O =2AlO2-+3H2↑
B. 钠与水反应:Na+ H2O = Na++OH一+ H2↑
C. 稀硫酸与氢氧化钡溶液反应:H++OH一= H2O
D. 铜与氯化铁溶液反应: 3Cu+2Fe3+=2Fe+ 3Cu2+
难度: 中等查看答案及解析
-
某固体酸燃料电池以CHSO4固体为电解质传递OH一,其基本结构见下图,电池总反应可表示为:2H2+O2===2H2O,下列有关说法不正确的是

A. 电子通过外电路从a极流向b极
B. b电极为正极
C. a极上的电极反应式为:H2-2e-=== 2 H+
D. 该装置能将化学能转变为电能
难度: 中等查看答案及解析
-
下列有关实验操作、 现象和解释或结论都正确的是
选项
实验操作
现象
解释或结论
A
一定量的Fe粉与适量稀HNO3充分反应后,滴入KSCN溶液
溶液呈红色
稀HNO3具有强氧化性,溶液中只生成Fe3+
B
向Na2SiO3溶液中滴加稀盐酸
溶液变浑浊
酸性:H2SiO3>HCl
C
将SO2通入紫色石蕊试液中
溶液先变红后褪色
SO2的水溶液具有酸性,且具有漂白性
D
用玻璃棒蘸取浓氨水点到红色石蕊试纸上
试纸变蓝色
浓氨水呈碱性
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列属于取代反应的是
A.
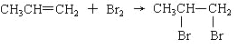
B.
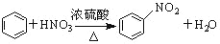
C. 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
D.
难度: 简单查看答案及解析
-
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,Y、Z、R三原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水;Z与W在元素周期表中相邻,X的单质是空气的主要成分之一,且其氢化物的水溶液能使酚酞变红。下列说法正确的是
A. 原子半径: R> Z>X B. 气态氢化物的稳定性:W>R
C. 最高价氧化物的水化物的碱性:Y>Z D. 工业上电解Z与R的化合物制取Z
难度: 中等查看答案及解析
-
某硫酸铵样品中混有硫酸氢铵。称取不同质量的样品分别于100mL 2.300mol/L的氢氧化钠溶液充分反应,得到的实验数据入下表:
实验序号
Ⅰ
Ⅱ
样品质量(g)
14.35
28.70
氨气质量(g)
3.570
3.570
下列说法错误的是
A. 样品中硫酸铵与硫酸氢铵的物质的量之比为9:1
B. 实验Ⅰ中氢氧化钠一定过量
C. 要使实验Ⅱ的样品完全反应,需要再加入氢氧化钠0.2100mol
D. 样品中氮元素的质量分数是20.49%
难度: 困难查看答案及解析