-
下列常见物质的俗名与化学式对应正确的是 ( )
A. 生石灰——Ca(OH)2 B. 铁红——Fe2O3
C. 水玻璃——H2SiO3 D. 酒精——CH3COOH
难度: 中等查看答案及解析
-
下列做法不应该提倡的是( )
A. 用布袋到超市购物 B. 将废电池深埋到泥土里
C. 积极推广氢能等新能源的使用 D. 对生活垃圾进行分类放置
难度: 简单查看答案及解析
-
下列诗句描述的过程包含化学变化的是( )
A. 有麝自来香,不用大风扬 B. 野火烧不尽,春风吹又生
C. 只要功夫深,铁杵磨成针 D. 夜来风雨声,花落知多少
难度: 中等查看答案及解析
-
据报道,某些建筑材料会产生放射性同位素
,从而对人体产生伤害。该同位素原子的中子数与质子数之差是
A. 50 B. 136 C. 86 D. 222
难度: 简单查看答案及解析
-
反应SiO2+2C
2CO+Si可用于工业上制取粗硅,该反应属于( )
A. 化合反应 B. 复分解反应 C. 置换反应 D. 分解反应
难度: 简单查看答案及解析
-
下列化学用语表示正确的是( )
A. 葡萄糖的结构简式:C6H12O6
B. 氮气的电子式:
C. 氯离子的结构示意图:
D. 硫酸钠的电离方程式:Na2SO4=2Na++SO42-
难度: 简单查看答案及解析
-
既可用排水法又可用向上排空气法收集的气体是( )
A. O2 B. NO C. NH3 D. NO2
难度: 简单查看答案及解析
-
下列物质中含有共价键的离子化合物是( )
A. NH4Cl B. NaCl C. H2O D. Cl2
难度: 简单查看答案及解析
-
在密闭容器中进行的反应:N2+3H2
2NH3,下列说法正确的是
A.加入催化剂能加快反应速率
B.增大压强能减慢反应速率
C.达到平衡时,反应速率:v(正) = v(逆) = 0
D.达到平衡时,N2和H2能100%转化为NH3
难度: 中等查看答案及解析
-
在含有大量H+、Mg2+、SO42-的溶液中,还可能大量共存的离子是( )
A. Ba2+ B. OH- C. CO32- D. Fe2+
难度: 中等查看答案及解析
-
刚刚过去的春节期间,一个名叫“福(氟)禄(氯)双全(醛)”的物质(结构简式如下图)在化学人的朋友圈中火了起来。该物质属于
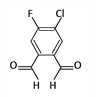
A. 单质 B. 无机物
C. 有机物 D. 氧化物
难度: 简单查看答案及解析
-
下列有关SO2的说法正确的是
A. 无色无味气体 B. 可用排水法收集
C. 具有较强的还原性 D. 可用碱石灰干燥
难度: 中等查看答案及解析
-
下列实验方法或操作正确的是

A. 转移溶液 B. 制蒸馏水 C. 分离水和酒精 D. 稀释浓硫酸
难度: 中等查看答案及解析
-
下列关于有机物的说法正确的是( )
A. 乙醇难溶于水 B. 乙烯可使酸性KMnO4溶液褪色
C. 乙酸的酸性比碳酸弱 D. 苯不能萃取碘水中的碘单质
难度: 中等查看答案及解析
-
天然气脱硫包含反应2FeCl3+H2S===2FeCl2+S↓+2HCl,下列说法正确的是( )
A. FeCl3是还原剂 B. FeCl3中氯元素被还原
C. H2S是氧化剂 D. H2S中硫元素被氧化
难度: 简单查看答案及解析
-
为确认碳酸氢钠固体中是否含有碳酸钠,下列实验操作及判断正确的是( )
A. 加热,观察是否放出气体
B. 滴加盐酸,观察是否放出气体
C. 溶于水中,滴加澄清石灰水,观察是否有白色沉淀生成
D. 溶于水中,滴加少量氯化钡溶液,观察是否有白色沉淀生成
难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是( )
A. 锌与醋酸反应:Zn +2H+===Zn2++H2↑
B. 氯气与溴化钠溶液反应:2Br-+Cl2===Br2+2Cl-
C. 氯化铝与氨水反应:Al3++3OH-===Al(OH)3↓
D. 钠与水反应:Na +H2O===Na++OH-+H2↑
难度: 简单查看答案及解析
-
下列过程吸收热量的是( )
A. 水结成冰 B. 浓硫酸溶于水
C. 生石灰投入水中 D. 煅烧石灰石
难度: 简单查看答案及解析
-
下列方案能达到实验目的的是( )
A. 用向上排空气法收集铜粉与稀硝酸反应产生的NO
B. 将Cl2与HCl混合气体通过饱和食盐水可得到纯净的Cl2
C. 用焰色反应鉴别KOH和Na2SO4
D. 用水鉴别乙醇与乙酸
难度: 中等查看答案及解析
-
美国NASA曾开发一种铁—空气二次电池。该电池放电时,其原理如下图所示,电池反应为:2Fe+O2+2H2O===2Fe(OH)2。
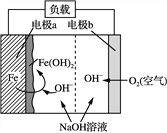
有关该电池放电时的说法正确的是( )
A. a极质量不变
B. b极为电池负极
C. 电子由a极经负载流向b极
D. 由电能转变为化学能
难度: 简单查看答案及解析
-
下列化学方程式书写正确的是( )
A. CH2=CH2 +Br2→CH3CHBr2
B. 2CH3CH2OH+O2
2CH3CHO+2H2O
C. CH3COOH+CH3CH2OH
CH3COOCH3CH2+H2O
D.
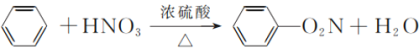
难度: 简单查看答案及解析
-
短周期主族元素X、Y、Z、W的原子序数依次增大,X与Z同主族,X-与氦原子的电子层结构相同,Y的最外层电子数是次外层的2倍,W的最高正价与最低负价代数和为4。下列说法正确的是( )
A. 原子半径:r(X)<r(Y)<r(Z)<r(W)
B. Y的最高价氧化物的水化物酸性比W的强
C. W分别与X、Z形成的化合物的化学键类型相同
D. 由X、Y两种元素组成的化合物,其分子中所有原子可能处于同一平面
难度: 中等查看答案及解析
-
一包由Cu、Fe、Fe2O3三种物质组成的混合粉末,某合作学习小组的同学拟探究其组成。他们称取该混合粉末20.40 g放入反应器中并连接气体收集装置,向反应器逐滴加入4.00 mol·L-1硫酸并缓慢搅拌。当加入硫酸a mL时,混合粉末恰好完全溶解,同时收集到b L(标准状况)H2,向反应后的溶液中滴入KSCN溶液,溶液不显红色。下列结论正确的是( )
A. 混合粉末中物质的量之间一定满足:n(Cu)+n(Fe)=n(Fe2O3)
B. 混合粉末中物质的量之间一定满足:n(Fe)>n(Cu)>n(Fe2O3)
C. 若a=72.50,b=1.12,则20.40 g混合粉末中:n(Fe)=n(Cu)= 0.05 mol、n(Fe2O3)=0.09 mol
D. 混合粉末中物质的量之间一定满足:n(Cu)+n(Fe)=n(Fe2O3)+
难度: 困难查看答案及解析