-
将4 g氢氧化钠溶解在10 mL水中,再稀释成1 L,从中取出10 mL,这10 mL溶液的物质的量浓度是
A. 1 mol·L-1 B. 0.1 mol·L-1
C. 0.01 mol·L-1 D. 10 mol·L-1
难度: 中等查看答案及解析
-
瑞典皇家科学院10月3日宣布2018诺贝尔化学奖一半颁给美国科学家弗朗西斯·阿诺德,奖励她实现了酶的定向转化,阿诺德研究的酶可以用于更加环保地制造化学产品,比如药物,还能生产可再生的燃料,让交通运输更加绿色环保。其中酶属于
A. 无机物 B. 单质 C. 氧化物 D. 有机物
难度: 简单查看答案及解析
-
只含有共价键的化合物是
A. NaOH B. K2O C. Cl2 D. HCl
难度: 简单查看答案及解析
-
下列仪器中可以直接加热的是( )
A. 烧杯 B. 容量瓶 C. 蒸发皿 D. 圆底烧瓶
难度: 简单查看答案及解析
-
13153I用于甲状腺的同位素治疗,该原子的中子数是
A. 131 B. 78 C. 53 D. 25
难度: 简单查看答案及解析
-
下列实验装置及操作不能达到实验目的的是 ( )
A.
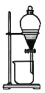 分离汽油和煤油 B.
分离汽油和煤油 B. 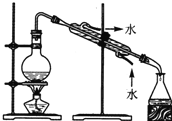 用自来水制蒸馏水
用自来水制蒸馏水C.
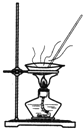 从食盐水中获取氯化钠 D.
从食盐水中获取氯化钠 D. 收集氨气
难度: 简单查看答案及解析
-
下列反应中,不属于氧化还原反应的是( )
A. 2NaOH + Cl2 ===NaCl +NaClO+ H2O
B. 3O2
2O3
C. Br2 + 2KI ===2KBr + I2
D. 3Cu +8HNO3 ===3Cu(NO3)2 +2NO↑ +4H2O
难度: 简单查看答案及解析
-
溶液、胶体和浊液这三种分散系的根本区别是( )
A. 分散质粒子直径的大小 B. 是否有丁达尔现象
C. 能不能通过滤纸和半透膜 D. 是否均一、稳定、透明
难度: 简单查看答案及解析
-
下列叙述错误的是( )
A. 碳酸氢钠可用于治疗胃酸过多的药物
B. 明矾溶于水形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
C. 二氧化硫有漂白性,可以用来漂白食物
D. 常温下,用铁、铝制容器来盛装浓硝酸
难度: 简单查看答案及解析
-
下列离子能大量共存的是
A. Na+、NH4+、Cl-、OH-
B. K+、Mg2+、NH4+、SO42-
C. Ba2+、Fe2+、NO3-、CO32-
D. H+、K+、CO32-、NO3-
难度: 简单查看答案及解析
-
下列变化不可能通过一步实验直接完成的是( )
A. Al2O3 →Al(OH)3 B. Fe→Fe3O4
C. Al→NaAlO2 D. NaHCO3→Na2CO3
难度: 简单查看答案及解析
-
若用CuSO4•5H2O晶体配制450mL0.2mol/L的CuSO4溶液,需要CuSO4•5H2O晶体的质量为( )
A. 25.0g B. 22.5g C. 9.0g D. 16.0g
难度: 简单查看答案及解析
-
下列化学用语书写不正确的是( )
A. 硫酸钾的电离方程式:K2SO4===2K+ + SO42-
B. 氯原子的结构示意图:
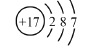
C. 用单线桥表示电子转移方向和数目:
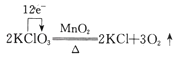
D. 用电子式表示硫化钠的形成过程:
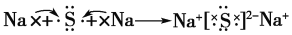
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 2.4 g Mg 与足量稀硫酸反应,转移的电子数为0.1 NA
B. 标准状况下,22.4L乙醇中所含的分子数为 NA
C. 0.1mol·L-1 KOH溶液中含有OH-的数目是0.1NA
D. 44 g CO2所含的氧原子个数为2NA
难度: 简单查看答案及解析
-
如图所示,将锌片和铜片按不同方式插入稀硫酸中,下列说法正确的是( )
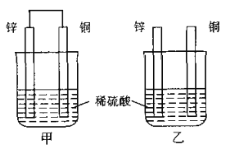
A. 甲中电子经导线从铜片流向锌片
B. 两烧杯中锌片上均发生还原反应
C. 两烧杯中铜片表面均无气泡产生
D. 一段时间后,两烧杯中溶液的c(H+)均减小
难度: 简单查看答案及解析
-
根据元素周期律判断,下列各组物质的性质比较,正确的是( )
A. 稳定性:NH3>PH3>SiH4
B. 原子半径:S > Na>O
C. 金属性:Li>Na>K
D. 酸性: H2SO4>HClO4 > H3PO4
难度: 简单查看答案及解析
-
工业制硫酸中一步重要反应是SO2在400~500℃下的催化氧化:2SO2 + O2
2SO3,下列说法不正确的是( )
A. 增大O2的浓度能加快反应速率
B. 在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题
C. 达到平衡后,正、逆反应速率相等且均为零
D. 该反应为可逆反应,故在一定条件下二氧化硫不可能全部转化为三氧化硫
难度: 简单查看答案及解析
-
下列表示对应化学反应的离子方程式正确的是
A. 向Al2(SO4)3溶液中加入过量的氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
B. 稀醋酸滴在石灰石上:CaCO3+2H+=Ca2++H2O+CO2↑
C. 向稀HNO3中加入铁粉:Fe+2H+=Fe2++H2↑
D. 氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
难度: 简单查看答案及解析
-
下列有机反应中,有一种反应类型与其他三种反应类型不同的是
A. CH3COOH+CH3CH2OH
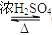 CH3COOCH2CH33+H2O
CH3COOCH2CH33+H2OB. 2CH3CH2OH+O2
 2CH3CHO+2H2O
2CH3CHO+2H2OC. CH4+Cl2
CH3Cl+HCl
D.
+Br2
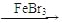
+HBr
难度: 中等查看答案及解析
-
下列有关离子(或物质)的检验及结论中,正确的是( )
A. 取少量试液于试管中,加入稀硝酸酸化的氯化钡溶液,若有白色沉淀生成,说明试液中含有SO42-
B. 某溶液中加硝酸银溶液生成白色沉淀,说明原溶液中有Cl-
C. 向某溶液中滴加NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,说明原溶液中有NH4+
D. 向某溶液中先滴加几滴氯水,再滴入几滴KSCN溶液后变成红色,说明原溶液中有Fe3+
难度: 中等查看答案及解析