-
“一带一路”是跨越时空的宏伟构思,赋予古丝绸之路崭新的时代内涵.古丝绸之路将中国的发明和技术传送的到国外.下列不涉及化学变化的是( )
A.稻草造纸 B.使用火药 C.蚕丝织布 D.冶炼金属
难度: 中等查看答案及解析
-
某学生用量筒量取液体,量筒摆放平稳,且学生面对刻度,他首先俯视凹液面的最低处读数为19mL,倾出一部分液体后,又仰视读数为10mL,则该同学实际倒出液体的体积为
A.等于9mL B.大于9mL C.小于9mL D.无法确定
难度: 中等查看答案及解析
-
下列物质的用途与其依据的性质不符合的是( )
A.氧气用于急救病人-----------氧气能供给呼吸
B.金刚石用于制作玻璃刀-----------金刚石是天然存在最硬的物质
C.氮气常用作保护气-----------氮气的化学性质稳定
D.一氧化碳用于冶金工业-----------一氧化碳难溶于水
难度: 简单查看答案及解析
-
改革开放40年来,我国环境保护事业发展迅速,贯彻绿色发展理念,坚持人与自然和谐共生,坚持节约资源和环境保护,努力建设“美丽中国”。下列做法不符合这一理念的是( )
A.提倡绿色出行,践行“低碳”理念
B.推广无纸化办公,使用再生纸且双面打印
C.大力发展新资源,禁止使用化石燃料
D.洗菜的水用来浇花
难度: 简单查看答案及解析
-
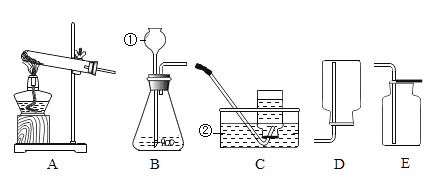
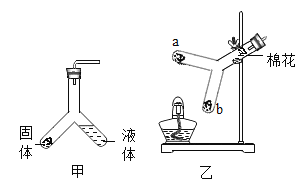
如图表示初中化学常见实验操作,其中正确的是( )
A.
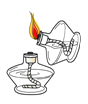 点燃酒精灯 B.
点燃酒精灯 B.检查装置的气密性
C.
读出液体的体积 D.
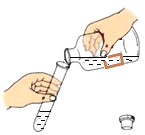 液体的取用
液体的取用难度: 中等查看答案及解析
-
下列对有关事实的解释中,错误的是
A.水银温度计液柱上升——汞原子体积变大
B.酒精需要密封保存——酒精分子在不断运动
C.冰水共存物属于纯净物——冰和水都由水分子构成
D.过氧化氢分解属于化学变化——过氧化氢分子本身发生变化
难度: 简单查看答案及解析
-
推理是学习化学的一种重要方法,但推理必须科学、严谨。下列推理正确的是( )
A.可燃物燃烧时温度需要达到着火点,所以温度达到着火点时,可燃物就一定能燃烧
B.催化剂在反应前后质量不变,因此反应前后质量不变的物质一定是催化剂
C.分子、原子可以构成物质,则物质都是由分子、原子构成的
D.同种元素的原子质子数相同,则质子数相同的原子一定是同种元素
难度: 困难查看答案及解析
-
科学、规范的操作是安全地进行实验的重要保证,下列操作中错误的是( )
A.实验过程中酒精不慎洒落到桌面上并着火应立即用水扑灭
B.闻气体时用手轻轻地在瓶口扇动,使极少量气体飘进鼻孔
C.实验中眼睛里溅进了药液要立即用水冲洗,边洗边眨眼睛
D.点燃氢气等可燃性气体前,应先检验其纯度,防止发生爆炸
难度: 简单查看答案及解析
-
学习化学的目的并不在于一定要成为化学家,重要的是善于用化学知识去分析、解决生产生活中的问题。下列有关燃烧与灭火的说法正确的是( )
A.房屋失火,消防队员用水扑灭是因为降低了可燃物的着火点
B.为防止森林大火蔓延可设置隔离带,其目的是隔离可燃物
C.汽油放置在空气中没有燃烧是因为汽油不是可燃物
D.用灯帽盖灭酒精灯是因为降低了可燃物的温度
难度: 中等查看答案及解析
-
有关碳和碳的氧化物的说法中,错误的是( )
A.金刚石和石墨都由碳原子构成,所以它们物理性质相同
B.二氧化碳的过多排放是导致温室效应的原因之一
C.用煤火取暖时应注意通风,防止一氧化碳中毒
D.古代用墨书写或绘制的字画长久不变色,是因为常温下碳的化学性质不活泼
难度: 简单查看答案及解析
-
在NH4NO3、N2、NO2、NO这四种物质中,N元素表现出来的化合价共有( )
A.2种 B.3种 C.4种 D.5种
难度: 简单查看答案及解析
-
甲、乙、丙、丁四种物质在反应前后的质关系如图所示,下列有关说法不正确的是( )

A.丙可能是该反应的催化剂
B.x的值是7
C.丁一定是生成物
D.参加反应的甲和乙质量比为14 : 26
难度: 中等查看答案及解析
-
下列实验方案,能达到实验目的是( )
选项
实验目的
实验方案
①
鉴别二氧化碳和氮气
将燃着的木条分别伸入气体中,观察现象
②
从氯酸钾与二氧化锰制取氧气后的固体中回收二氧化锰
溶解固体,过滤后对滤渣进行洗涤,烘干
③
除去二氧化碳中混有的一氧化碳
点燃
④
鉴别木炭粉末和氧化铜粉末
观察颜色
A.① B.② C.③ D.④
难度: 困难查看答案及解析
-
某学生欲称取5.3g氯化钠,他在左边托盘上放了5g砝码,又把游码移到0.3g处,然后在右托盘上加氯化钠直到天平平衡。这时托盘上氯化钠的实际质量是( )
A.5.3g B.5.0g C.4.7g D.5.6g
难度: 简单查看答案及解析
-
下图所示的四个图像,能正确反映对应变化关系的是
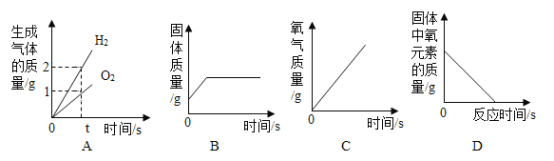
A.水的电解
B.将一定质量的硫酸铜溶液倒入盛有铁钉的烧杯中
C.向少量的H2O2溶液中加入MnO2固体
D.加热一定量KMnO4固体
难度: 简单查看答案及解析