-
密度为0.91g/cm3的氨水,质量分数为25%.该氨水用等体积的水稀释后,所得溶液中溶质的质量分数( )
A. 等于12.5% B. 大于12.5%
C. 小于12.5% D. 无法确定
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 酸雨是指pH<7的雨水,酸雨长时间放置,酸性变强
B. 用排空气法收集NO
C. 用加热浓氨水的方法可以快速制氨气,经氯化钙干燥后得到纯净的氨气
D. 8NH3+3Cl2===6NH4Cl+N2,因此可以用浓氨水检验氯气的管道是否漏气
难度: 中等查看答案及解析
-
下列关于氨水的叙述中,不正确的是( )
A. 氨水具有弱碱性 B. 氨水和液氨成分相同
C. 氨水中共有6种粒子 D. 稀氨水可作化肥
难度: 中等查看答案及解析
-
用玻璃棒分别蘸取下列各项中的两种浓溶液,将玻璃棒的下端相互靠近,没有白烟生成的是( )
A. 浓氨水和浓硝酸 B. 浓氨水和浓盐酸
C. 浓氨水和浓硫酸 D. 浓氨水和浓醋酸
难度: 中等查看答案及解析
-
下列关于二氧化硫的说法不正确的是( )
A. 能使某些有色物质褪色 B. 无色、有刺激性气味、无毒
C. 既有氧化性、又有还原性 D. 既可溶于水、又可与水反应
难度: 中等查看答案及解析
-
将固体碳酸氢铵置于试管中加热,使放出的气体依次通过盛有足量过氧化钠的干燥管、足量浓硫酸的洗气瓶,则最后得到的气体是( )
A. 氨气 B. 氧气 C. 水 D. 二氧化碳
难度: 中等查看答案及解析
-
浓硫酸与下列物质作用时,既表现氧化性又表现酸性的是( )
A. 红热的木炭 B. 硫化氢气体 C. 氧化亚铁 D. 使蔗糖变黑
难度: 中等查看答案及解析
-
下列污染现象主要与二氧化硫有关的是( )
A. 酸雨 B. 光化学烟雾 C. 臭氧层空洞 D. 温室效应
难度: 中等查看答案及解析
-
某溶液能与铝反应生成氢气,则该溶液中一定不能够大量共存的离子组是
A.NH4+、K+、Ba2+、Cl﹣ B.Na+、K+、Cl﹣、S2﹣
C.Na+、 Fe2+、Cl﹣、NO3﹣ D.K+、Na+、SO32﹣、NO3﹣
难度: 中等查看答案及解析
-
下列有关SO2气体的实验现象中不正确的是( )
A.装满SO2气体的试管倒立在滴有紫色石蕊的水槽中,进入试管的液体呈红色
B.将SO2气体通入装有品红溶液的试管里,红色逐渐褪去,给试管加热无明显变化
C.打开盛有SO2气体的集气瓶口的玻璃片,可闻到刺激性气味
D.将SO2气体通入装有溴水溶液的试管里,橙红色逐渐褪去
难度: 简单查看答案及解析
-
下列溶液可用于鉴别CO2与SO2气体的有
①品红溶液②氯化钙③酸性高锰酸钾④溴水⑤氢硫酸⑥澄清石灰水.
A. ①③④⑤ B. ①③④⑥ C. ①②③④⑥ D. ①②③④⑤⑥
难度: 中等查看答案及解析
-
用一种试剂可鉴别NH4Cl,K2SO4,(NH4)2SO4,AlCl3、FeCl3五瓶溶液,(必要时,可加热)该试剂是
A. Ba(OH)2 B. NaOH C. KSCN D. BaCl2
难度: 中等查看答案及解析
-
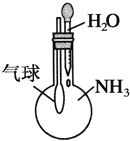
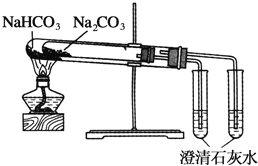
下列实验装置不能达到实验目的的是( )
A. 用SO2做喷泉实验

B. 验证Cu与浓硝酸反应的热量变化
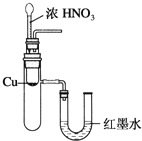
C. 验证NH3易溶于水
D. 比较Na2CO3与NaHCO3的稳定性
难度: 中等查看答案及解析
-
下列事实不能用于判断金属性强弱的是( )
A. 金属单质间发生的置换反应
B. 1 mol金属单质在反应中失去电子的多少
C. 金属元素的最高价氧化物对应水化物的碱性强弱
D. 金属元素的单质与水或酸反应置换出氢气的难易
难度: 中等查看答案及解析
-
几种短周期元素的原子半径及主要化合价如表所示:( )
元素符号
X
Y
Z
R
T
原子半径(nm)
0.160
0.080
0.102
0.143
0.074
主要化合价
+2
+2
-2,+4,+6
+3
-2
根据表中信息,判断以下说法正确的是( )
A. 单质与氢气化合的难易程度Z>T
B. 离子半径:T2- > X2+ > R3+
C. 元素最高价氧化物对应水化物的碱性:Y>R>X
D. 相同条件下,单质与稀硫酸反应的剧烈程度:R>Y>X
难度: 中等查看答案及解析
-
X、Y、Z为短周期元素,这些元素原子的最外层电子数分别为1、4、6,则由这三种元素组成的化合物的化学式可能是
A. XYZ B. X3YZ C. XYZ2 D. X2YZ3
难度: 简单查看答案及解析
-
下列关于碘元素(原子序数53)的放射性同位素131I的叙述中正确的是( )
A. 一个此碘原子中含有131个质子
B. 131I位于元素周期表中第4周期ⅦA族
C. 其氢化物为HI,比HCl的稳定性弱
D. 最高价氧化物的水化物为HIO4,比HClO4的酸性强
难度: 中等查看答案及解析
-
将1.92gCu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共产生气体1.12L(标准状况),则反应中消耗HNO3的物质的量为( )
A. 0.12mol B. 0.11mol C. 0.08mol D. 0.06mol
难度: 困难查看答案及解析