-
某元素的原子最外层只有一个电子,它与卤素结合时,所形成的化学键( )
A. 一定是离子键
B. 一定是共价键
C. 可能是离子键也可能是共价键
D. 以上说法都不正确
难度: 中等查看答案及解析
-
对于AZX和A+1ZX+两种粒子,下列叙述正确的是( )
A. 质子数一定相同,质量数和中子数一定不同
B. 化学性质几乎相同
C. 一定都由质子、中子、电子构成
D. 核电荷数、核外电子数一定相同
难度: 中等查看答案及解析
-
短周期元素X、Y、Z、W在元素周期表中位置如右图所示,若W原子最外层电子数是其内层电子总数的
。下列说法中,正确的是( )
A. X只有一种氧化物
B. 气态氢化物的稳定性Z>W
C. 原子半径由大到小的排列顺序Z>Y>X
D. 元素X是自然界中形成化合物种类最多的元素
难度: 中等查看答案及解析
-
根据中学化学教材所附元素周期表判断,下列叙述不正确的是( )
A. K层电子数为奇数的所有元素所在族的序数与该元素原子的K层电子数相等
B. L层电子数为奇数的所有元素所在族的序数与该元素原子的L层电子数相等
C. L层电子数为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等
D. M层电子数为奇数的所有主族元素所在族的序数与该元素原子的M层电子数相等
难度: 中等查看答案及解析
-
某元素X最高价含氧酸的相对分子质量为98,且X的氢化物的分子式不是H2X,则下列说法正确的是( )
A. X的最高价含氧酸的分子式可表示为H3XO4
B. X是第二周期第ⅤA族元素
C. X是第二周期第ⅥA族元素
D. X的最高正化合价为+4
难度: 中等查看答案及解析
-
运用元素周期律分析下面的推断,其中不正确的是( )
A. 锂(Li)与水反应比钠与水反应剧烈
B. 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸
C. 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂
D. HBrO4的酸性比HIO4的酸性强
难度: 中等查看答案及解析
-
下表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素原子的核电荷数为X元素的2倍。下列说法正确的是( )
X
Y
Z
W
T
A. X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次增大
B. Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次增强
C. 液态WX3汽化均需克服的作用力与NaCl相同
D. 根据元素周期律,可以推测T元素的单质具有半导体特性,T2X3具有氧化性和还原性
难度: 中等查看答案及解析
-
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法不正确的是
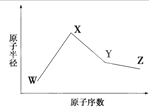
A. 对应简单离子半径X<W
B. 对应气态氢化物的稳定性Y<Z
C. 化合物XZW既含离子键也含共价键
D. Y的氧化物能与Z或X的最高价氧化物对应的水化物反应
难度: 中等查看答案及解析
-
X、Y、Z、W为四种短周期的主族元素,其中X、Z同族,Y、Z同周期,W与X、Y及不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6.下列说法不正确的是( )
A. Y元素的最高价氧化物对应的水化物的化学式为HYO4
B. 原子半径由小到大的顺序为W<X<Z
C. X与W可以形成W2X、W2X2两种物质
D. Y、Z两元素的气态氢化物中,Z的气态氢化物更稳定。
难度: 中等查看答案及解析