-
下列说法正确的是
A. 棉、麻、丝、毛织物完全燃烧只生成CO2和H2O
B. 聚乙烯中含有不饱和键,用它制成的塑料制品易老化
C. 维生素C常用作抗氧化剂说明它自身具有氧化性
D. 人体内的酶通过降低反应的活化能来提高化学反应速率
难度: 简单查看答案及解析
-
NA是阿伏加德罗常数的值,下列说法正确的是
A. 46g乙醇中含有的共价键数目为8NA
B. 1molD2O中含有的中子数为8NA
C. 标准状况下2.24LCl2溶于水转移的电子数为0.2NA
D. 0.1L 1mol·L-1Na2S溶液中S2-与HS-离子总数为0.1NA
难度: 中等查看答案及解析
-
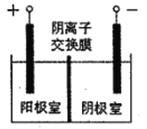
关于下列实验装置图的叙述中,正确的是
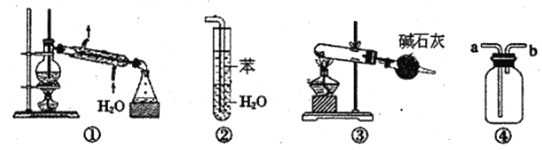
A. 装置①用于分离沸点不同的液体混合物
B. 装置②用于吸收HC1气体,能够防止倒吸
C. 装置③可用于分解NH4Cl制备NH3
D. 装置④既可收集CO2也可收集H2
难度: 简单查看答案及解析
-
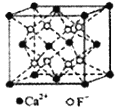
有机化合物环丙叉环丙烷结构示意图为
,下列关于该化合物的说法正确的是
A. 与环己烯互为同分异构体 B. 其二氯代物只有三种
C. 所有的碳原子均在一个平面内 D. 生成1molC6H14至少需要2molH2
难度: 中等查看答案及解析
-
短周期元素X、Y、Z、W分属三个周期,且原子序数依次增加。其中Y与X、Z均可形成1︰1或1︰2的二元化合物;X与Z最外层电子数相同;Y与W的一种化合物是一种新型的自来水消毒剂。下列说法错误的是
A. 常温常压下Y的单质为气态
B. 离子半径:W>Z>Y
C. X与Z形成的离子化合物具有还原性
D. W的最高价氧化物的水化物一定是强酸
难度: 简单查看答案及解析
-
二氧化硫一空气质子交换膜燃料电池将化学能转变成电能的同时,实现了制硫酸、发电、环保三位一体的结合,其原理如图所示。下列说法错误的是
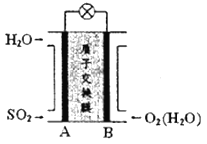
A. 负极的电极反应式为SO2+2H2O-2e-=SO42-+4H+
B. 反应总式为2SO2+O2+2H2O=2H2SO4
C. 质子的移动方向为从电极B到电极A
D. SO2气流速度的大小可能影响电池的电动势
难度: 简单查看答案及解析
-
电导率是衡量电解质溶液导电能力大小的物理量。常温下,将相同体积的盐酸和氨水分别加水稀释,溶液的电导率随加入水的体积V(H2O)变化的曲线如图所示,下列说法正确的是
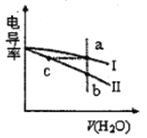
A. 曲线I表示盐酸加水稀释过程中溶液电导率的变化
B. a、b、c三点溶液的pH:a>b>c
C. 将a、b两点溶液混合,所得溶液中:c(Cl-)=c(NH4+)+c(NH3·H2O)
D. 氨水稀释过程中,c(NH4+)/ c(NH3·H2O)不断减小
难度: 中等查看答案及解析
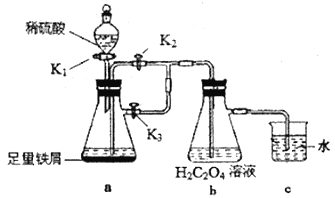


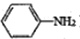 )易被氧化
)易被氧化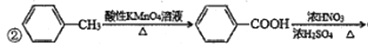
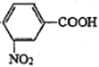
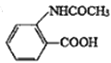 ,写出相应的合成路线流程图___________(无机试剂任选,合成路线流程图示例见本题题干)。
,写出相应的合成路线流程图___________(无机试剂任选,合成路线流程图示例见本题题干)。