-
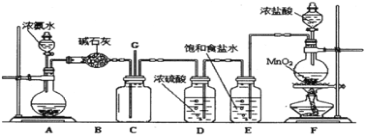
将一定量锌与100mL18mol/L浓硫酸充分反应后,若锌完全溶解同时产生气体0.8mol,将反应后的溶液稀释得400mL,测得溶液c(H+)=2mol/L,则下列叙述中错误的是( )
A. 气体中SO2和H2物质的量比为6:1 B. 反应中共消耗锌52.0g
C. 所得气体应该为SO2和H2混合物 D. 反应共转移电子1.6mol
难度: 中等查看答案及解析
-
工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2.下列说法错误的是( )
A. 硫元素既被氧化,又被还原
B. 氧化剂与还原剂的物质的量之比为2:1
C. 相同条件下,每吸收10m3SO2就会放出2.5m3CO2
D. 若生成2.24LCO2,则转移0.8mol电子
难度: 困难查看答案及解析
-
下列用途中应用了氮气的稳定性的是:( )
A. 以氮气为原料之一制造硝酸 B. 合成氨气后,制氮肥
C. 金属焊接时的保护气 D. 镁可以和氮气反应
难度: 简单查看答案及解析
-
下列推断正确的是( )
A. 铝粉在氧气中燃烧生成Al2O3,故铁丝在氧气中燃烧生成Fe2O3
B. 铁能从硫酸铜溶液中置换出铜,故钠也能从硫酸铜溶液中置换出铜
C. 钠与氧气、水等反应时钠均作还原剂,故金属单质参与化学反应时金属均作还原剂
D. 活泼金属钠保存在煤油中,故活泼金属铝也保存在煤油中
难度: 简单查看答案及解析
-
下列无色气体中,常温时遇空气很容易变为红棕色的是( )
A. NH3 B. NO C. CO2 D. SO2
难度: 简单查看答案及解析
-
下列反应中,浓硫酸既表现出强氧化性又表现出酸性的是( )
A. 2NaCl+H2SO4(浓)
Na2SO4+2NaCl B. Na2SO3+H2SO4(浓)
Na2SO4+SO2↑+H2O
C. C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O D. 2FeO+4H2SO4(浓)
Fe2(SO4)3+SO2↑+4H2O
难度: 简单查看答案及解析
-
在一些建筑工地的食堂中,常发生将工业用盐当作食用盐而引起中毒的现象.该盐的化学式为( )
A. MgCl2 B. KCl C. NaNO2 D. MgSO4
难度: 简单查看答案及解析
-
下列各组中两种微粒所含电子数不相等的是( )
A. S2-和Al3+ B. CO和N2 C. H3O+和OH- D. NH3和NH4+
难度: 简单查看答案及解析
-
如图装置中,若关闭活塞,则品红溶液无变化,石蕊试液变红,石灰水变浑浊;打开活塞,则品红溶液褪色,石蕊试液变红,石灰水变浑浊。据此判断气体和广口瓶中盛放的物质是( )
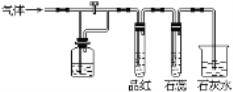
A. HCl和浓H2SO4
B. Cl2和氯水
C. Cl2和NaHCO3溶液
D. SO2和NaHCO3溶液
难度: 简单查看答案及解析
-
某元素的一种同位素X的原子质量数为A,含N个中子,它与
原子组成HmX分子.在a克HmX中所含质子的物质的量是( )
A.
(A-N+m)mol B.
(A-N)mol C.
(A-N)mol D.
(A-N+m)mol
难度: 简单查看答案及解析
-
下列化学反应的离子方程式正确的是( )
A. 将少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
B. 向稀氨水中通入少量CO2:2NH3·H2O+CO2=2NH4++CO32-+H2O
C. 用稀HNO3溶解FeS固体:FeS+2H+=Fe2++H2S↑
D. 将醋酸滴入硅酸钠溶液中:SiO32-+2H+=H2SiO3↓
难度: 困难查看答案及解析
-
下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
a
b
c
A
Al
AlCl3
Al(OH)3
B
HNO3
NO
NO2
C
Si
SiO2
H2SiO3
D
Na2O
Na2CO3
NaHCO3
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有NaHCO3、NaHSO4、KH2PO4、KHPO4等。已知 H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2,则下列说法正确的是( )
A. H3PO2属于二元酸 B. H3PO2属于三元酸
C. NaH2PO2属于酸式盐 D. NaH2PO2属于正盐
难度: 困难查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A. 1molFeCl3完全转化为Fe(OH)3胶体后生成NA个胶体粒子
B. 1.8g的NH4+中含有的电子数为NA
C. 常温常压下,32gO2和O3的混合气体中所含原子数为1.5NA
D. 1molCl2参加反应转移电子数一定为2NA
难度: 中等查看答案及解析
-
在溶液中加入适量Na2O2后仍能大量共存的离子组是( )
A. MnO4-、Ba2+、Cl-、NO3- B. Na+、Cl-、CO32-、SO32-
C. Ca2+、Mg2+、NO3-、HCO3- D. K+、AlO2-、Cl-、SO42-
难度: 困难查看答案及解析
-
1.92gCu投入到一定量的浓硝酸中,铜完全溶解,生成的气体的颜色越来越浅,共收集到 672 mL 的气体(标准状况下).将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的氧气,恰好使气体完全溶于水,则通入的氧气的体积为( )mL
A. 168 B. 224 C. 336 D. 672
难度: 中等查看答案及解析