-
下列有关物质的用途说法不正确的是
A. Si 可用于制造光导纤维 B. 钠、钾合金可用于原子反应堆作热交换剂
C. FeCl3 溶液可作为铜质电路板蚀刻剂 D. 漂白粉可用于自来水杀菌消毒
难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是
A. 钠与水反应:Na + H2O = Na+ + OH— + H2↑
B. 铁与盐酸反应:2Fe + 6H+ = 2Fe3+ + 3H2↑
C. 碳酸钙与醋酸反应:CO32-+ 2H+ = CO2↑ + H2O
D. 铜与稀硝酸反应:3Cu + 8H+ + 2NO3—= 3Cu2+ + 2NO↑ + 4H2O
难度: 中等查看答案及解析
-
室温下,下列各组离子在指定溶液中能大量共存的是( )
A. 0.1 mol·L-1的氨水:Cu2+、Na+、SO42-、NO3-
B. 0.1 mol·L-1的CaCl2溶液:Na+、K+、Cl-、NO3-
C. 0.1 mol·L-1的Na2SO3溶液:K+、H+、SO42-、NO3-
D. 0.1 mol·L-1的NaHCO3溶液:K+、Na+、NO3-、OH-
难度: 简单查看答案及解析
-
已知H2(g)+Cl2(g)=2HCl(g) △H=―184.6kJ·mol-1, 则反应HCl(g)=1/2H2(g)+1/2Cl2(g)的△H为( )
A. +184.6kJ·mol-1 B. ―92.3kJ·mol-1
C. ―369.2kJ·mol-1 D. +92.3kJ·mol-1
难度: 简单查看答案及解析
-
为了更好的解决能源问题,人们一方面研究如何提高燃料的燃烧效率,另一方面寻找新能源。以下做法不能提高燃料效率的是( )
A. 煤的汽化与液化 B. 通入大大过量的空气
C. 液体燃料呈雾状喷出 D. 将煤块粉碎
难度: 中等查看答案及解析
-
下列化学用语或模型正确的是( )
A. CH4分子的比例模型:
B. 乙醇的结构简式:C2H6O
C. Al3+的结构示意图:
D. 氯化钙的电离方程式:CaCl2===Ca2++Cl2-
难度: 中等查看答案及解析
-
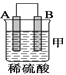
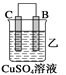
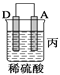
下列有关实验装置进行的相应实验,能达到实验目的的是( )
A.
收集 NO B.
 制备 NH3
制备 NH3C.
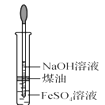 制备 Fe(OH)2 D.
制备 Fe(OH)2 D. 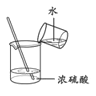 稀释浓 H2SO4
稀释浓 H2SO4难度: 中等查看答案及解析
-
下列各组离子中,能在溶液中大量共存的一组是
A.Mg2+、Al3+、Cl-、OH-
B.Na+、Ba2+、OH-、SO42—
C.K+、Na+、NO3—、HCO3—
D.K+、NH4+、CO32—、OH-
难度: 中等查看答案及解析
-
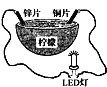
用下列方法制取氢气,反应速率最大的是 ( )
A. 夏天,粉末状锌与2mol·L一1硫酸溶液反应
B. 夏天,块状锌与2 mol·L一1硫酸溶液反应
C. 冬天,粉末状锌与2 mol·L一1硫酸溶液反应
D. 冬天,块状锌与2 mol·L一1硫酸溶液反应
难度: 简单查看答案及解析
-
下列粒子间的关系,描述不正确的是
A.
与
互为同位素 B. 乙醇和乙酸互为同系物
C.
和
属于同种物质 D. CH(CH3)3和CH3CH2CH2CH3互为同分异构体
难度: 中等查看答案及解析
-
下列有机反应属于加成反应的是
A.CH4 + Cl2
CH3Cl + HCl
B.
C.
D.
难度: 中等查看答案及解析
-
化合物X可用于合成Y.下列有关X、Y的说法正确的是( )
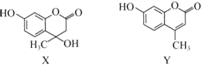
A. X分子中所有原子可能在同一平面上
B. X在一定条件下可以发生消去反应
C. Y与足量H2的加成产物中不含手性碳原子
D. X、Y与足量浓溴水反应的类型完全相同
难度: 中等查看答案及解析
-
用化学用语表示CH4+Cl2
CH3Cl+HCl中的相关微粒,其中正确的是( )
A. 中子数为20的氯原子:
B. HCl的电子式:H∶Cl
C. CH4的结构式:CH4 D. Cl的结构示意图:
难度: 简单查看答案及解析
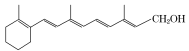

 中含有的官能团的名称为_________、__________、__________。
中含有的官能团的名称为_________、__________、__________。