-
下列说法正确的是
①NH3的水溶液能导电,故NH3是电解质 ②向含有BaCl2和NaOH的混合溶液中通入少量的二氧化硫气体,有白色沉淀生成 ③101 KPa、150℃时,agCO和H2的混合气体在足量的O2中完全燃烧,将燃烧后的产物通入足量的Na2O2固体后,Na2O2增重ag ④碱性氧化物一定是金属氧化物 ⑤22.4L的CO气体和28g N2所含的电子数相等 ⑥根据分散系是否具有丁达尔效应将分散系分为溶液、胶体和浊液 ⑦为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量 ⑧氧化还原中,有一种元素被氧化,一定有另一种元素被还原
A.②③④ B.②④⑦⑧ C.①⑤⑥⑦ D.③⑤⑥⑧
难度: 中等查看答案及解析
-
化学与环境密切相关,下列有关说法错误的是( )
A. NO2、NO含氮氧化物是光化学烟雾的主要污染物
B. 对酸性物质的排放加以控制,开发新清洁能源是减少酸雨的有效措施
C. CO2、NO2或SO2都会导致酸雨的形成
D. 大气中CO2含量的增加会导致温室效应加剧
难度: 简单查看答案及解析
-
下列关于硅及其化合物的叙述正确的是( )
A. 硅晶体可用于制造光导纤维
B. 陶瓷、玻璃、水泥都是硅酸盐产品
C. 二氧化硅在电子工业中是重要的半导体材料
D. 二氧化硅与氢氟酸和氢氧化钠均能反应,属于两性氧化物
难度: 中等查看答案及解析
-
丰富多彩的颜色变化增添了化学实验的魅力,下列有关反应颜色变化的叙述中,正确的是
①新制氯水久置后→浅黄绿色消失
②淀粉溶液遇单质碘→蓝色
③蔗糖中加入浓硫酸搅拌→白色
④SO2通入品红溶液中→红色褪去
⑤氨气通入酚酞溶液中→红色
A. ①②③④ B. ②③④⑤ C. ①②④⑤ D. 全部
难度: 中等查看答案及解析
-
下列现象说明二氧化硫具有漂白性的是( )
A. 能使高锰酸钾溶液褪色
B. 能使黄绿色的氯水褪色
C. 能使品红溶液褪色
D. 能使含酚酞的烧碱溶液褪色
难度: 中等查看答案及解析
-
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的 水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的不可能是 ( )

A. N2与NO2的混和气体 B. O2与NO2的混和气体
C. NO与NO2的混和气体 D. NO2一种气体
难度: 简单查看答案及解析
-
一定条件下,将等体积的NO2和O2的混合气体置于试管并将该试管倒置于水槽中至液面不再上升时,剩余气体的体积约为原体积的( )
A. 1/4 B. 3/4 C. 1/8 D. 3/8
难度: 中等查看答案及解析
-
氨的催化氧化是工业制硝酸的重要反应:4NH3+5O2
4NO+6H2O,对于该反应判断正确的是
A. 氧气被还原 B. 该反应是置换反应
C. 氨气是氧化剂 D. 若有17 g氨参加反应,反应中转移10 mol电子
难度: 中等查看答案及解析
-
下列事实与浓硫酸表现出的性质(括号中)对应关系正确的是( )
A. 在空气中敞口久置的浓硫酸,溶液质量增大(脱水性)
B. 在加热条件下铜与浓硫酸反应(氧化性、酸性)
C. 蔗糖与浓硫酸反应中有海绵状的炭生成(吸水性)
D. 浓硫酸可用来干燥某些气体(不挥发性)
难度: 简单查看答案及解析
-
对下列实验现象的原因分析不正确的一项是( )
选项
实验现象
原因分析
A
浓硫酸遇湿润的蓝色石蕊试纸,先变红,后变黑
硫酸有酸性,使石蕊变红,浓硫酸有脱水性,使试纸炭化变黑
B
新制氯水中滴加石蕊试液,溶液先变红,后褪色
氯气与水反应生成HCl、HClO,HCl显强酸性,使石蕊变红,HClO具有强氧化性,使其褪色
C
SO2通入溴水中,溴水褪色
SO2具有漂白性,使其褪色
D
向湿润蔗糖中加入浓硫酸,固体迅速变黑,后体积急剧膨胀
在浓硫酸脱水作用下,蔗糖被炭化,炭与浓硫酸反应生成了CO2、SO2
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体d呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是
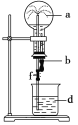
a(干燥气体)
b(液体)
A
NO
水
B
CO2
4 mol/L NaHCO3溶液
C
Cl2
饱和NaCl水溶液
D
NH3
1 mol/L盐酸
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列对于某些离子的检验及结论中一定正确的
A. 加入稀盐酸产生无色的气体,将气体通入澄清石灰水中,溶液变浑浊,一定有
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有
C. 加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有
D. 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
难度: 简单查看答案及解析
-
下列反应的离子方程式书写不正确的是( )
A. 二氧化硅与强碱溶液反应:SiO2+2OH―=SiO32―+H2O
B. 氯水与SO2溶液反应:Cl2+SO2+2H2O=4H++ClO―+SO32―
C. 二氧化锰与浓盐酸反应:MnO2+4H++2Cl―===Mn2++2H2O+Cl2↑
D. 氢氧化钙溶液与等物质的量稀硫酸混合:Ca2++2OH-+2H++
=CaSO4↓+2H2O
难度: 中等查看答案及解析