-
下列变化属于化学变化的是
A. 盐酸挥发 B. 牛奶发酵 C. 海水晒盐 D. 干冰升华
难度: 简单查看答案及解析
-
下列人体所必需的元素中,缺乏会引起贫血的是
A.铁 B.钙 C.碘 D.锌
难度: 中等查看答案及解析
-
碳酸钠是重要的化工原料,其俗称是
A. 火碱 B. 食盐 C. 纯碱 D. 小苏打
难度: 简单查看答案及解析
-
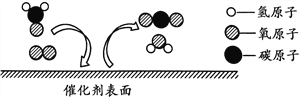
已知一种碳原子可用于测定文物的年代,该原子的原子核内含有6个质子和8个中子,则核外电子数为
A. 2 B. 6 C. 8 D. 14
难度: 中等查看答案及解析
-
下列物质的用途中,利用其物理性质的是
A. 硫酸用于除铁锈 B. 生石灰用作食品干燥剂
C. 大理石用作建筑材料 D. 熟石灰用于改良酸性土壤
难度: 简单查看答案及解析
-
下列说法不正确的是
A. 空气中O2的体积分数约为21%
B. CO2是绿色植物光合作用的原料之一
C. CO具有可燃性,在工业上可用于炼铁
D. 稀有气体化学性质稳定,可用作保护气
难度: 简单查看答案及解析
-
杨梅中含有丰富的叶酸(Cl9Hl9N7O6),对防癌抗癌有积极作用。下列说法正确的是
A. 叶酸的相对分子质量为441 g
B. 叶酸中氮元素质量分数大于氧元素质量分数
C. 叶酸由碳原子、氢原子、氮原子和氧原子构成
D. 叶酸中碳、氢、氮、氧四种元素质量比为19:19:7:6
难度: 简单查看答案及解析
-
下列基本实验的装置或操作正确的是
A.
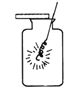 铁丝在氧气中燃烧 B.
铁丝在氧气中燃烧 B. 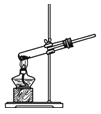 加热高锰酸钾
加热高锰酸钾C.
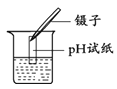 测定溶液pH D.
测定溶液pH D. 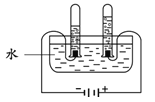 证明水的组成
证明水的组成难度: 简单查看答案及解析
-
某纯净物X燃烧的化学方程式为X+3O2 点燃 2CO2+2H2O,则X的化学式为
A. C2H2 B. C2H4 C. C2H6O D. C2H6
难度: 简单查看答案及解析
-
下列食品中,含营养素种类最多的是
A.
 汉堡 B.
汉堡 B.  大米粥
大米粥C.
 面包 D.
面包 D.  油条
油条难度: 简单查看答案及解析
-
如图表示化学反应中溶液的颜色变化。下列叙述不正确的是

A. 若X是稀盐酸,a可能是紫色石蕊溶液
B. 若X是稀盐酸,b可能是氧化铁
C. 若X是稀硫酸,c不可能是单质
D. 若X是稀硫酸,d不可能是单质
难度: 困难查看答案及解析
-
高氯酸钾( KClO4) 可用作火箭推进剂,其溶解度如下表。下列说法不正确的是
温度/℃
20
40
60
80
溶解度/g
1.68
3.73
7.3
13.4
A. 高氯酸钾的溶解度随温度降低而减小
B. 80℃的高氯酸钾饱和溶液冷却至40℃一定有晶体析出
C. 60℃时,高氯酸钾饱和溶液中溶质的质量分数小于7.3%
D. 20℃时,向2 g高氯酸钾中加入98 g水,所得溶液的溶质质量分数为2%
难度: 中等查看答案及解析