-
下列可用于验证铜、铁、锌三种金属的活动性强弱的药品有
A. Cu、Zn、FeSO4溶液 B. Cu、Fe、ZnSO4溶液
C. Zn、FeSO4溶液、CuSO4溶液 D. Fe、CuSO4溶液、ZnSO4溶液
难度: 困难查看答案及解析
-
能将氢氧化钠溶液、石灰水、稀盐酸三种溶液区分开的一种试剂是 …( )
A. 酚酞试液 B. 紫色石蕊试液 C. 碳酸钠溶液 D. 氯化钠溶液
难度: 简单查看答案及解析
-
三甲基一氯硅烷[(CH3)3SiCl]是一种生产有机硅化合物的原料,遇火能燃烧甚至会发生爆炸,与水接触可产生盐酸。则下列说法错误的是
A. 保存三甲基一氯硅烷时应密封防水
B. 三甲基一氯硅烷由碳、氢、硅、氯四个原子构成
C. 三甲基一氯硅烷元素质量比C:H:Si:Cl=24:18:56:71
D. 三甲基一氯硅烷充分燃烧的产物之一是二氧化碳
难度: 困难查看答案及解析
-
今有60g溶质的质量分数为10%的NaNO3溶液,欲将其溶质的质量分数增大一倍,应采用的方法是
A.把溶剂蒸发掉一半 B.加入6gNaNO3晶体
C.把溶剂蒸发掉30g D.加入20%的NaNO3溶液30g
难度: 中等查看答案及解析
-
打雷放电时,空气中有极少的氧气(O2)会转变成臭氧(O3),氧气(O2)和臭氧(O3),以下说法错误的是
A. 该变化是物理变化 B. 该变化是化学变化
C. 氧气和臭氧是同一种物质 D. 氧气和臭氧是两种不同的物质
难度: 简单查看答案及解析
-
诺贝尔化学奖曾授于发现C60的三位科学家,现在C70也已制得,对C60 和C70这两种物质的叙述错误的是
A.互为同素异形体 B.式量之差为120
C.是由碳元素组成 D.是两种新型的有机物
难度: 困难查看答案及解析
-
我国化工专家侯德榜创立了“侯氏制碱法”,促进了世界制碱技术的发展。流程简图如下
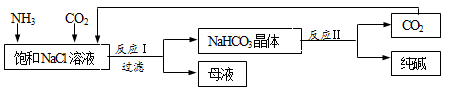
(已知:氨气极易溶于水。母液中有一种物质是NH4Cl) ,下列有关说法错误的是
A. 反应中先通入氨气的目的是促进二氧化碳的吸收,提高产率
B. 反应II得到的CO2可以循环使用
C. 反应I的方程式为NaCl+NH3+CO2 =NaHCO3↓+NH4Cl
D. “母液”中一定只含有两种溶质
难度: 困难查看答案及解析
-
向盛有饱和澄清石灰水的烧杯中持续通入CO2出现了异常现象(先变浑浊后又变澄清),兴趣小组同学利用数字分析仪进行研究,测定记录得到溶液的导电性变化随二氧化碳的质量关系如图所示。
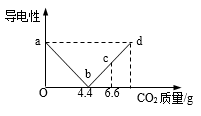
下列说法不正确的是
A. ab段溶液变浑浊,bd段溶液变澄清
B. b点溶液溶液碱性最强
C. bd段反应为CaCO3+CO2+H2O=Ca(HCO3)2
D. c点溶液中含有2种溶质,沉淀质量为15g
难度: 中等查看答案及解析
-
下图所示的一组实验可用于研究燃烧条件。下列说法中,正确的是

A.此组实验烧杯中的热水只起提高温度的作用
B.图1中铜片上的白磷和红磷对比说明燃烧必须有氧气
C.图1中铜片上的红磷和水下的白磷对比说明燃烧必须达到可燃物的着火点
D.图1和图2中水下白磷对比说明燃烧必须要有氧气
难度: 中等查看答案及解析
-
烧杯中盛有CuCl2和HCl的混合溶液100g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示。下列说法正确的是
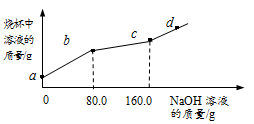
A. ab段反应产生蓝色沉淀
B. bc段溶液增加70.2g
C. c点对应的溶质质量分数为4.9%
D. d点溶液中溶质有2中,且PH>7
难度: 极难查看答案及解析
-
某CuO与C的混合物,共10 g,加热至不再有气体生成的时候,将生成的气体通入足量的澄清石灰水中,得到沉淀5 g,则原混合物中CuO的质量可能为
A. 8 g B. 8.4 g C. 8.6 g D. 9.4 g
难度: 极难查看答案及解析