-
NA为阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,0.2gH2中含有的氢原子数为0.2NA
B. 标准状况下,2.24 LH2O中含有的水分子数为0.1NA
C. 1L0.1mol/LNa2CO3溶液中含有的钠离子数为0.1NA
D. 点燃条件下,56g铁丝与足量氯气反应,转移的电子数为0.2NA
难度: 简单查看答案及解析
-
下列有关苯、乙酸、乙醇说法正确的是
A. 都不易溶于水
B. 除乙酸外,其余都不能与金属钠反应
C. 苯能与溴水在铁作催化剂下发生取代反应
D. 乙醇与乙酸都能发生取代反应
难度: 简单查看答案及解析
-
下列对化学反应的认识错误的是
A. 会引起化学键的变化 B. 会产生新的物质
C. 必然引起物质状态的变化 D. 必然伴随着能量的变化
难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是
A. 石灰石与稀醋酸反应:CaCO3+2CH3COOH==Ca2++2CH3COO-+H2O+CO2↑
B. 三氯化铁溶液与氢氧化钠溶液反应:FeCl3+3OH-==Fe(OH)3↓+3Cl-
C. 氢氧化钡溶液与硫酸铜溶液反应:Ba2++SO42-=BaSO4↓
D. 钠投入水中:Na+2H2O=Na++2OH-+H2↑
难度: 简单查看答案及解析
-
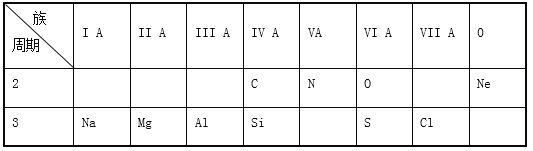
下列有关周期表的说法正确的是( )
A. 短周期是第一、二、三、四周期 B. 元素周期表有18个族
C. 第ⅠA族的元素全部是金属元素 D. 元素周期表含元素最多的族是第ⅢB族
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 新发现的核素
中,电子数比中子数多179
B. 白磷和红磷互为同分异构体
C. 氕、氘、氚互为同素异形体
D. CH3CH2CH2CH3 和C(CH3)4互为同系物
难度: 简单查看答案及解析
-
下列化学用语正确的是( )
A. 甲烷的结构式CH4 B. K的原子结构示意图:

C. 苯的分子式C6H6 D. 氯化钠的电子式
难度: 简单查看答案及解析
-
等物质的量的CH4和NH3相比较,下列结论错误的是( )
A. 他们的分子个数比是1:1 B. 他们的原子个数比是1:1
C. 他们的氢原子个数比是4:3 D. 他们所含氢的质量比是4:3
难度: 简单查看答案及解析
-
下列各组离子在溶液中可以大量共存的是( )
A. Na+、Ba2+、Cl-、SO42- B. H+、NH4+、CO32-、SO42-
C. K+、Na+、NO3-、OH- D. H+、Cl-、CH3COO-、NO3-
难度: 简单查看答案及解析
-
下列物质不能通过化合反应制得的是( )
A. Fe(OH)3 B. Fe(OH)2 C. CaSiO3 D. FeCl3
难度: 简单查看答案及解析
-
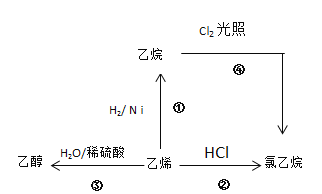
下列物质间的转化不能一步实现的是( )
A. N2→NO2 B. HNO3→O2 C. SO2→H2SO4 D. H2SO4→SO2
难度: 简单查看答案及解析
-
下列关于化学键的叙述正确的是
A. 离子化合物中一定含有离子键
B. 单质分子中均存在化学键
C. 离子化合物中只有离子键
D. 含有共价键的化合物一定是共价化合物
难度: 简单查看答案及解析
-
常温下,下列物质与水混合后静置,出现分层的是( )
A. 氯化氢 B. 乙醇 C. 苯 D. 乙酸
难度: 简单查看答案及解析
-
下列实验装置正确(固定装置略去)且能达到实验目的的是( )
A. 制备氢氧化亚铁
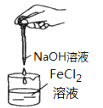 B. 石油的蒸馏
B. 石油的蒸馏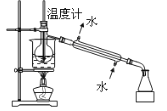 C. 分离苯和水
C. 分离苯和水 D. 实验室制乙酸乙酯
D. 实验室制乙酸乙酯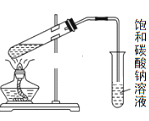
难度: 简单查看答案及解析
-
将4 mol A气体和2 mol B气体充入2 L的密闭容器中,一定条件下发生如下反应: 2A(g)+B(g)
2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,下列几种说法正确的是( )
①用物质A表示的反应平均速率为0.3 mol·L-1·s-1
②用物质B表示的反应平均速率为0.3 mol·L-1·s-1
③2 s时物质A的转化率为70%④2 s时物质B的浓度为0.7 mol·L-1
A. ①③ B. ①④ C. ②③ D. ③④
难度: 中等查看答案及解析
-
一定温度下,密闭容器中可逆反应3X(g)+Y(g)
2Z(g)达到限度的标志是
A. X的生成速率与Z的生成速率相等 B. 单位时间内生成3n mol X,同时消耗n mol Y
C. 某时刻X、Y、Z的浓度相等 D. 某时刻X、Y、Z的分子个数比为3:1:2
难度: 困难查看答案及解析
-
铜和浓硝酸反应产生的气体,用排水法收集到a L气体(标准状况),被还原的硝酸是( )
A. a/22.4 mol B. a/11.2 mol C. 3a/22.4 mol D. 3amol
难度: 简单查看答案及解析
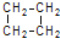 可简写为
可简写为