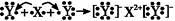-
将SO2通入BaCl2溶液至饱和,未见沉淀生成,继续通入另一种气体,仍无沉淀,则通入的气体可能是( )
A.CO2 B.NH3 C.NO2 D.H2S
难度: 简单查看答案及解析
-
短周期元素X、Y、Z所在的周期数依次增大,它们的原子序数之和为20,且Y2-与Z+核外电子层的结构相同。下列化合物中同时存在极性和非极性共价键的是( )
A. Z2Y B. X2Y2 C. Z2Y2 D. ZYX
难度: 中等查看答案及解析
-
下列物质中所有原子均满足最外层8电子稳定结构的化合物是
A. PCl5 B. P4 C. CCl4 D. NH3
难度: 简单查看答案及解析
-
硼的最高价含氧酸的化学式不可能是( )
A. HBO2 B. H2BO3 C. H3BO3 D. H2B4O7
难度: 简单查看答案及解析
-
制备(NH4)2Fe(SO4)2·6H2O的实验中,需对过滤出产品的母液(pH<1)进行处理。常温下,分别取母液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是( )
A.通入过量Cl2:Fe2+、H+、NH4+、Cl-、SO42-
B.加入少量NaClO溶液:NH4+、Fe2+、H+、SO42-、ClO-
C.加入过量NaOH溶液:Na+、Fe2+、NH4+、SO42-、OH-
D.加入过量NaClO和NaOH的混合溶液:Na+、SO42-、Cl-、ClO-、OH-
难度: 中等查看答案及解析
-
将相同质量的铜分别和过量浓硝酸、稀硝酸反应,下列叙述正确的是( )
A.反应剧烈程度,两者相同 B.消耗硝酸的物质的量:前者多,后者少
C.反应生成气体的颜色:前者浅,后者深 D.反应中转移的电子总数:前者多,后者少
难度: 中等查看答案及解析
-
一定条件下,一种反应物过量,另一种反应物仍不能完全反应的是( )
A.过量的铁与浓硝酸 B.过量的浓盐酸与二氧化锰
C.过量的铜与浓硫酸 D.过量的锌与18mol/L硫酸
难度: 简单查看答案及解析
-
不能作为判断硫、氯两种元素非金属性强弱的依据是
A. 单质氧化性的强弱 B. 单质与氢气化合的难易
C. 单质沸点的高低 D. 最高价氧化物对应的水化物酸性的强弱
难度: 中等查看答案及解析
-
从化学键的观点看,化学反应的实质是“旧键的断裂,新键的形成”,据此你认为下列变化属于化学变化的是( )
①金刚石变成石墨 ②NaCl熔化
③HCl溶于水电离出H+和Cl- ④电解熔融的Al2O3制取A1
A. 只有④ B. ①④ C. ②③ D. ②③④
难度: 中等查看答案及解析
-
下列试剂保存不正确的是( )
A. 碘必须保存在煤油中 B. 新制的氯水用棕色试剂瓶装并密封保存
C. 氢氟酸用塑料瓶装保存 D. 液溴用一薄层水封盖再密闭保存于低温处
难度: 简单查看答案及解析
-
不能通过单质间直接化合一步得到的是( )
A. SO3 B. FeS C. Cu2S D. Na2O2
难度: 简单查看答案及解析
-
下列物质久罝于空气中均会发生颜色变化,由于被氧气氧化而引起的是( )
A. 溴化银 B. 氯水 C. 硫酸亚铁 D. 浓硝酸
难度: 中等查看答案及解析
-
下列物质:①氯气②二氧化硫③活性炭④漂白粉,都能使品红溶液褪色,但褪色过程不发生氧化还原反应的是( )
A. ①② B. ②③ C. ①④ D. ②③④
难度: 中等查看答案及解析
-
两种元素原子的核外电子层数之比与最外层电子数之比相等,则在周期表的前10号元素中,满足上述关系的元素共有 ( )
A. 1对 B. 2对 C. 3对 D. 4对
难度: 简单查看答案及解析
-
某元素X,其原子的电子层数为(n-1),最外层电子数为(2n-1)。下列有关元素x 的说法中正确的是( )
A. 元素X的气态氢化物一定极易溶于水 B. 由X形成的含氧酸均为强酸
C. X不能形成化学式为KXO4的含氧酸盐 D. X可能是金属元素
难度: 中等查看答案及解析
-
下列有关NO的说法不正确的是( )
A. NO可看作亚硝酸(HNO2)的酸酐 B. NO任意排放会造成大气污染
C. 实验室制取NO气体可用排水法收集 D. 氨催化氧化可生成NO
难度: 中等查看答案及解析
-
如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物。则下列说法错误的是( )
A. 常温下,单质a呈气态 B. 单质c具有强氧化性
C. 稳定性:d>e D. f受热易分解为d和e
难度: 中等查看答案及解析
-
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是( )
X
Y
Z
W
Q
A. 元素X与元素Z的正化合价之和的数值等于8
B. 原子半径的大小顺序为rX>rY>rZ>rW>rQ
C. Y和Z形成了共价化合物
D. 元素W周期表中的位置是第三周期,第VI主族
难度: 中等查看答案及解析
-
为了除去氯气中混有的少量水蒸气,可使含杂质的氯气通过某特定的干燥管,此干燥管中装有下列药品中的.
A.五氧化二磷粉未 B.浓硫酸 C.饱和食盐水 D.碱石灰
难度: 简单查看答案及解析
-
只用一种试剂就能把Na2SO4、NaCl、(NH4)2SO4、NH4Cl四种溶液区分开来,这种试剂是
A.AgNO3 B.NaOH C.BaCl2 D.Ba(OH)2
难度: 中等查看答案及解析
-
第三周期元素按原子序数递增的顺序(稀有气体除外),以下说法正确的是( )
A. 原子半径和离子半径均减小 B. 金属性减弱,非金属性增强
C. 氧化物对应的水化物碱性减弱,酸性增强 D. 氧化性最弱的简单阳离子是Al3+
难度: 中等查看答案及解析
-
下列叙述不正确的是( )
A. NH3易液化,液氨常用作制冷剂
B. 与金属反应时,稀HNO3可能被还原为更低价态,则HNO3氧化性强于浓HNO3
C. 氨盐受热易分解,因此贮存氨态氮肥时要密封保存,并放在阴凉通风处
D. 由NH3制碳酸氢铵和硫酸铵不是氮的固定
难度: 中等查看答案及解析
-
将O2和NH3的混合气体448mL通过加热的三氧化二铬(催化剂),充分反应后,再通过足量的水,最终收集到44.8mL O2。原混合气体中O2的体积可能是(假设氨全部被氧化;气体体积均已换算成标准状况)( )
A. 134.4mL B. 313.6mL C. 287.5mL D. 268.8mL
难度: 中等查看答案及解析
-
下列指定反应的离子方程式正确的是( )
A. 将 Cl2通入 Ca(OH)2饱和溶液中:2Cl2+2Ca(OH)2= 2Ca2++2Cl-+2ClO-+2H2O
B. 向(NH4)2SO4和NH4HSO4混合溶液中滴入少量的NaOH 溶液:H+ +OH-=H2O
C. 向酸性 KMnO4溶液中通入 SO2:2MnO4-+5SO2+4OH-=2Mn2++5SO42-+2H2O
D. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+
难度: 困难查看答案及解析