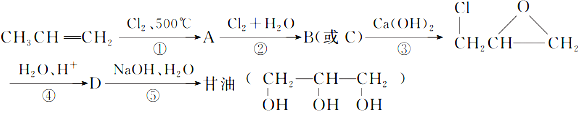-
下列叙述中,正确的是( )
A. 12g碳所含的原子数就是阿伏加德罗常数
B. 1molHCl的质量是36.5 g·mol-1
C. Cl2的摩尔质量等于它的相对分子质量
D. 摩尔是表示物质的量的单位,每摩尔物质含有阿伏加德罗常数个微粒
难度: 简单查看答案及解析
-
下列叙述正确的( )
A. 酸性氧化物和碱性氧化物都是电解质
B. 将NaOH溶液,逐滴加入FeCl3溶液,可制备氢氧化铁胶体
C. 硫酸、氢氧化钠、氯化钠均为强电解质,都属于离子化合物
D. 离子键一定只存在于离子化合物中,共价键不一定只存在于共价化合物中
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 淀粉和纤维素的分子式不同,所含的碳、氢、氧元素的质量比也不同
B. 苯酚钠溶液中通入少量二氧化碳气体,生成苯酚和碳酸钠
C. 鉴别地沟油和矿物油,可以加入足量的氢氧化钠溶液共热,不分层的是地沟油
D. 分离四氯化碳和甲苯的方法与分离汽油和水的方法一样
难度: 简单查看答案及解析
-
在反应中乙醇分子会断裂C—O键的是( )
A. 乙醇与丁酸的取代反应 B. 乙醇与金属钠反应
C. 乙醇在浓硫酸存在下发生消去反应 D. 乙醇在铜丝存在条件下发生催化氧化
难度: 简单查看答案及解析
-
不能与溴水发生反应的是①苯 ②苯酚③亚硫酸④NaOH溶液⑤AgNO3溶液⑥裂化汽油⑦己烷⑧镁粉( )
A. ①③⑦ B. ①④⑧ C. ①⑦ D. ②⑤⑦
难度: 简单查看答案及解析
-
下列化学用语正确的是( )
A. 乙酸根离子的结构式:
B. CO2分子的球棍模型:
C. 醛基的电子式为:
D. 3,3–二甲基–1–丁烯的结构简式:(CH3)3CCH=CH2
难度: 简单查看答案及解析
-
下列物质一定属于同系物的是( )
①
②C3H6 ③
④CH2=CH-CH=CH2
⑤
 ⑥C2H4 ⑦
⑥C2H4 ⑦ ⑧
⑧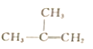
A. ⑦⑧ B. ①③ C. ④⑦ D. ②⑥⑧
难度: 简单查看答案及解析
-
某羧酸酯的分子式为C57H104O6,1mol该酯完全水解可得到3mol羧酸M和1mol甘油,羧酸M的分子式为( )
A. C18H34O2 B. C18H36O2 C. C17H32O2 D. C19H36O2
难度: 简单查看答案及解析
-
下列化合物中,核磁共振氢谱只出现两组峰且峰面积之比为3:1的是
A.
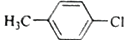
B.
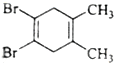
C.
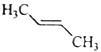
D.
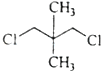
难度: 简单查看答案及解析
-
下列各化合物中,能发生酯化、还原、加成、消去四种反应的是
A.
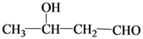 B.
B. 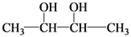
C. CH3—CH=CH—CHO D.

难度: 中等查看答案及解析
-
结构简式为
的高分子材料的单体的正确组合为( )
①HOOC-COOH ②HOCH2CH2OH ③HOCH2COOH
④
⑤
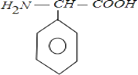 ⑥HOCH2CH2CH2OH
⑥HOCH2CH2CH2OHA. ①③④ B. ①②⑤ C. ①④⑥ D. ②③④
难度: 简单查看答案及解析
-
设NA代表阿伏加德罗常数的值,下列有关叙述正确的是( )
A. 2g21H2所含质子数为2NA
B. 1molCnH2n+2所含的化学键数为(3n+1)NA
C. 0.1mol/L的NH4NO3溶液中含氮原子数目为0.2NA
D. 在标准状况下,NA个CHCl3分子所占的体积约为22.4L
难度: 中等查看答案及解析
-
下列所得溶液的物质的量浓度等于0.1mol/L的是( )
A. 将0.1mol氨气充分溶解在1L水中
B. 将10g质量分数为98%的硫酸与990g水混合
C. 将8g三氧化硫溶于水并配成1L溶液
D. 将0.1mol氧化钾溶于水并配成1L溶液
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A. 同温同压下,相同体积的物质,它们的物质的量必相同
B. 常温常压下,等质量的N2与CO所含分子数相同
C. VLO2的质量一定比VLCO2的质量小
D. A容器中的H2与B容器中的NH3所含原子总数相等,则两容器的体积比为2:1
难度: 简单查看答案及解析
-
下列物质的分类正确的是( )
纯净物
碱性氧化物
酸性氧化物
强电解质
①
漂白粉
SiO2
CO2
AlCl3溶液
②
CuSO4•5H2O
Na2O2
N2O5
NH4NO3
③
福尔马林
CaO
Mn2O7
HClO
④
冰醋酸
Na2O
SO2
HCl
A. ① B. ② C. ③ D. ④
难度: 简单查看答案及解析
-
20℃时,KCl的溶解度为34g,若忽略固体溶解引起的溶液体积变化,则在该温度下,所配KCl溶液中KCl的物质的量浓度不可能是( )
A. 2mol/L B. 3mol/L C. 4mol/L D. 5mol/L
难度: 简单查看答案及解析
-
在aLAl2(SO4)3和(NH4)2SO4的混合溶液中加入bmolBaCl2,恰好使溶液中的SO42﹣离子完全沉淀;如加入足量强碱并加热可得到c mol NH3,则原溶液中的Al3+浓度(mol/L)为( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
下列反应属于消去反应的是( )
①CH3CH2OH+HBr
CH3CH2Br+H2O
②2CH3CH2OH
CH3CH2OCH2CH3+H2O
③CH3CH2CH2Br
CH3CH===CH2↑+HBr
④2CH3CH2OH+O2
2CH3CHO+2H2O
⑤CH3CH2Br+NaOH
CH3CH2OH+NaBr
⑥
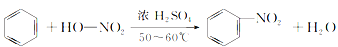
⑦CH3CH2OH
CH2===CH2↑+H2O
⑧CH3CH2OH+HCOOH
HCOOCH2CH3+H2O
A. ⑤⑦⑧ B. ②③ C. ③④⑤ D. ③⑦
难度: 简单查看答案及解析
-
某有机物A的分子式为C6H12O2,已知D不与Na2CO3溶液反应,C和E都不能发生银镜反应,又知转化关系如图,则A的结构可能有( )
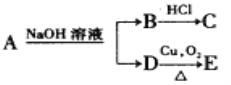
A. 2种 B. 4种 C. 6种 D. 8种
难度: 中等查看答案及解析
-
某激光染料,应用于可调谐染料激光器,分子球棍模型如图所示,下列有关叙述正确的是( )
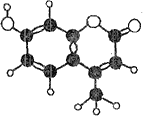
①能与溴水发生反应且1 mol该物质最多消耗2 mol Br2
②1 mol该物质最多能与4 mol H2加成
③能使酸性KMnO4溶液褪色
④1 mol该物质最多能与含2 mol NaOH的溶液反应
A. ①②③ B. ①③④ C. ③④ D. ②③
难度: 中等查看答案及解析



 )。
)。