-
等物质的量浓度的KCl、MgCl2、AlCl3三种溶液。现欲完全沉淀其中的Cl—,消耗相同物质的量浓度的AgNO3溶液的体积比为3:2:1,则上述三种溶液的体积比为
A. 1:1:1 B. 9:3:1 C. 3:2:1 D. 9:3:2
难度: 中等查看答案及解析
-
下列溶液中Cl-浓度与50mL1mol/L AlCl3溶液中Cl-浓度相等的是( )
A. 150mL1mol/L的NaCl溶液 B. 75mL2mol/L的NH4Cl溶液
C. 150mL2mol/L的KCl溶液 D. 75mL1mol/L的FeCl3溶液
难度: 中等查看答案及解析
-
下列分离混合物的实验计划中不正确的是( )
A. 分离乙酸(沸点77.1℃)与某种液态有机物(沸点120℃)的混合物——蒸馏
B. 从含有少量NaCl的KNO3溶液中提取KNO3——热水溶解、降温结晶、过滤
C. 用CCl4萃取水中的碘,待液体分层后——下层液体从下口放出,上层液体从上口倒出
D. 将溴水中的溴转移到有机溶剂中——加入酒精萃取
难度: 简单查看答案及解析
-
关于粗盐提纯的下列说法中正确的是( )
A. 溶解粗盐时,应尽量让溶液稀些,防止食盐不完全溶解
B. 将制得的食盐晶体转移到新制过滤器中用大量水进行洗涤
C. 当蒸发到剩余少量液体时,停止加热,利用余热将液体蒸干
D. 为除去粗盐中的Ca2+、 Mg2+、SO42-,可依次向溶液中加入足量的碳酸钠溶液、氢氧化钠溶液、氯化钡溶液、稀盐酸
难度: 简单查看答案及解析
-
在11g某化合物X2S中.含S2﹣0.1 mol.则X的相对原子质量为( )
A. 23 B. 24 C. 39 D. 40
难度: 简单查看答案及解析
-
某固体A在一定条件下可完全分解,生成B、C、D三种气体的混合物。反应方程式如下:2A=B↑+2C↑+3D↑,此时测得混合气体的相对平均分子质量为30,则固体A的摩尔质量为( )
A. 30g/mol B. 90g/mol C. 30 D. 90
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A. 摩尔是物质的量的单位
B. 氢的摩尔质量为2g/mol
C. NaOH的摩尔质量是40g
D. 2molH2O的摩尔质量是1molH2O摩尔质量的2倍
难度: 简单查看答案及解析
-
下列叙述中,正确的是 ( )
A. 1molH2O中含有1molH2和1mol O
B. 等质量的O2和O3中所含的氧原子数相同
C. 等质量的CO与CO2中所含碳原子数之比为7︰11
D. 98g H2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2 mol•L-1
难度: 简单查看答案及解析
-
下列装置或操作能达到实验目的的是

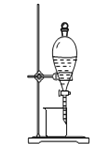
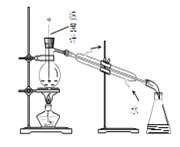
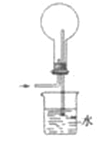
A. 检查装置气密性 B. 从碘的四氯化碳溶液中分离出碘
C. 分离甲苯和乙醇(互溶) D. 氨气的吸收
难度: 简单查看答案及解析
-
下列叙述错误的是( )
①用试管夹夹持试管时,试管夹从试管底部往上套,夹在离试管管口的1/3处
②给盛有液体的体积为1/2容积的试管加热
③把鼻孔靠近容器口去闻气体的气味
④将试管平放,用纸槽往试管里送入固体粉末后,然后竖立试管
⑤取用放在细口瓶中液体时,取下瓶塞倒放在桌面上,倾倒液体时,瓶上标签对着地面
⑥将滴管垂直伸进试管内滴加液体
⑦用坩埚钳夹取加热后的蒸发皿
⑧稀释浓硫酸时,把水迅速倒入盛有浓硫酸的量筒中
⑨检验装置的气密性时,把导管的一端浸入水中,用手捂住容器的外壁或用酒精灯微热
A. ②③⑤⑥⑧ B. ①④⑦⑨ C. ①④⑤⑦ D. ②④⑦⑨
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列说法错误的是
A. 常温常压下,48gO2含有的氧原子数为3NA
B. 1.7g NH3含有的质子数为NA
C. 标准状况下,11.2L氦气和氢气的混合气含有的分子数为0.5NA
D. 1L 0.1 mol/LCH3CH2OH水溶液中含H原子数目为0.6NA
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,22.4L四氯化碳分子数为NA
B. 常温下,46g NO2、N2O4组成的混合气体中所含有的原子数为3NA
C. 常温下,1mol/L的AlCl3溶液中含有的Cl-离子数为3NA
D. 18gNH4+离子中所含的电子总数为12NA
难度: 简单查看答案及解析
-
标准状况下,将V LA气体(摩尔质量为M g/mol)溶于0.1 L水中,所得溶液密度为ρ g/mL,则此溶液物质的量浓度为(mol·L-1)
A.
B.
C.
D.
难度: 简单查看答案及解析
-
在一定温度和压强下,2.4克CH4的体积为30mL,则在此状况下,4.8克氧气的体积为
A.40mL B.30mL C.20mL D.10mL
难度: 中等查看答案及解析
-
有关 98%的浓硫酸的问题叙述错误的是:
A. 硫酸和水的物质的量比9:1
B. 物质的量浓度大于10 mol·L-1
C. 和水等体积混合,所得溶液质量分数大于49%
D. 和水等质量混合,所得溶液质量分数大于49%
难度: 简单查看答案及解析


