-
下列对实验过程的评价正确的是( )
A. 某固体中加入稀盐酸,产生了无色气体,证明该固体一定是CaCO3
B. 某溶液中滴加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定含SO42—
C. 某无色溶液滴入无色酚酞试液显红色,该溶液一定显碱性
D. 验证烧碱溶液中是否含有Cl-,先加稀盐酸除去OH-,再加硝酸银溶液,有白色沉淀出现,证明含Cl-
难度: 简单查看答案及解析
-
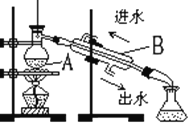
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
A. 分液、萃取、蒸馏 B. 萃取、蒸馏、分液
C. 分液、蒸馏、萃取 D. 蒸馏、萃取、分液
难度: 简单查看答案及解析
-
配制一定体积、一定物质的量浓度的溶液时,下列操作会使得所配溶液的浓度偏小的是( )
A. 容量瓶中原有少量蒸馏水
B. 定容时俯视容量瓶刻度线
C. 滴管加水时,有少量水滴到容量瓶外
D. 溶液从烧杯转移到容量瓶后没有洗涤烧杯
难度: 中等查看答案及解析
-
1mol CO 和 1mol CO2 具有相同的
① 分子数 ② 原子总数 ③ C原子数 ④ O原子数
A. ①③ B. ②④ C. ①④ D. ①②③
难度: 简单查看答案及解析
-
在盛放酒精的试剂瓶的标签上应印有下列警示标记中的 ( )
A.
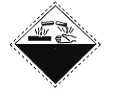 B.
B.  C.
C. 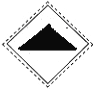 D.
D. 
难度: 简单查看答案及解析
-
欲萃取碘水中的I2 ,不能作为萃取剂的是( )
A. 酒精 B. 苯 C. CCl4 D. 汽油
难度: 中等查看答案及解析
-
下列各组物质,按化合物、单质、混合物顺序排列的是
A. 烧碱、液态氧、碘酒 B. 生石灰、白磷、熟石灰
C. 干冰、铁、氯化氢 D. 空气、氮气、胆矾
难度: 中等查看答案及解析
-
实验室里有4个药品橱,已经存放以下物品:
药品橱
甲橱
乙橱
丙橱
丁橱
药品
盐酸,硫酸
氢氧化钠,氢氧化钙
红磷,硫
铜,锌
实验室新购进一些碘,应该将这些碘放在( )
A. 甲橱 B. 乙橱 C. 丙橱 D. 丁橱
难度: 简单查看答案及解析
-
有CuO、Fe、H2、Ba(OH)2溶液、K2CO3溶液、NaOH溶液、稀硫酸七种物质,在常温下两种物质两两间能发生反应最多有
A. 4个 B. 5个 C. 6个 D. 7个
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A. 1 mol CO2 的质量为44g/mol
B. CO2的摩尔质量为44g
C. CO2的摩尔质量等于CO2的相对分子质量
D. NA个CO2分子的质量(以克为单位)与CO2的相对分子质量在数值上相同
难度: 简单查看答案及解析
-
下列叙述错误的是
A. 1mol任何物质都含有6.02×1023个分子 B. 0.012Kg12C中含有6.02×1023个碳原子
C. 1molH2O中含有2 mol H和1mol O D. 1molH2O中含有3 mol原子
难度: 中等查看答案及解析
-
下列各组物质中,所含分子数相同的是
A. 9g H2O和0.5molCl2 B. 11.2L N2和22g CO2
C. 20g H2 和20g O2 D. 224mLH2(标准状况)和0.1molN2
难度: 中等查看答案及解析
-
下列叙述不正确的是 ( )
A. 同温同压下,相同体积的气体,其气体分子物质的量也相等
B. 任何条件下,等物质的量的甲烷和一氧化碳所含的分子数一定相等
C. 不同的气体,若体积不同,则它们所含的分子数也不同
D. 相同条件下的一氧化碳气体和氮气,若体积相等,则质量也相等
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数,下列叙述正确的是
A. 标准状况下,22.4L H2含有的原子数为NA
B. 等质量的O2和O3中所含的氧原子数相同
C. 常温常压下,28g N2含有电子数为7NA
D. 等体积的CO与CO2中所含碳原子数之比为1﹕1
难度: 中等查看答案及解析
-
下列有关CuSO4·5H2O的叙述正确的是
A. 1 mol CuSO4·5H2O的质量为250g/mol
B. CuSO4·5H2O的摩尔质量为250g
C. CuSO4·5H2O的摩尔质量为250g/mol
D. 配制100mL 0.1mol/L 硫酸铜溶液需要CuSO4·5H2O 1.6g
难度: 简单查看答案及解析
-
下列溶液中,Cl-的物质的量与50ml 1mol/LAlCl3溶液中Cl-物质的量相等是( )
A. 150ml 3mol/LKCl溶液 B. 100ml 0.75mol/LMgCl2溶液
C. 100ml 1mol/LNaCl溶液 D. 15ml 2mol/LAlCl3溶液
难度: 简单查看答案及解析
-
已知3.01×1023个X2气体分子的质量为16g,则X的相对原子质量是( )
A. 16 B. 32 C. 64g /mol D. 32g /mol
难度: 简单查看答案及解析
-
实验室需配制一种强酸溶液500mL,c(H+)=2mol/L,下列配制方法可行的是
A. 取100mL5mol/LH2SO4,加入400mL水
B. 取200mL5mol/LHCl,加水稀释至500mL
C. 取100 mL5mol/LH2SO4,加500mL水稀释
D. 取100 mL5mol/LHNO3,加水稀释至500mL
难度: 简单查看答案及解析
-
下列关于实验操作的陈述中正确的是( )
A. 用规格为20mL的量筒一次量取16mL溶液,比用规格为10mL的量筒分两次量取16mL溶液的误差小
B. 受热后的蒸发皿要用坩锅钳夹取,并立即用自来水冲洗
C. 过滤时,为了加速溶液透过滤纸,可以用玻璃棒末端轻轻搅拌滤纸上的混合物
D. 配制一定物质的量浓度溶液时,为了避免溶质的损失,直接把称量的固体溶质转移到容量瓶中
难度: 中等查看答案及解析
-
用饱和的氯化铁溶液制取氢氧化铁胶体,正确的操作是( )
A. 将饱和氯化铁溶液滴入氢氧化钠溶液中即可
B. 滴入1mol氯化铁生成的氢氧化铁胶体中有6.02×1023个分散质微粒
C. 将饱和氯化铁溶液滴入沸水中,并继续煮沸至生成红褐色液体即可
D. 将饱和氯化铁溶液滴入沸水中,并继续煮沸至生成红褐色沉淀即可
难度: 简单查看答案及解析