-
括号内是区别下列各组常见物质的试剂、方法,其中错误的是
A. 硬水与软水 ( 肥皂水,振荡)
B. 水与双氧水(加入少量二氧化锰粉末)
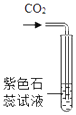
C. 二氧化碳与氮气(燃着的木条)
D. 食盐水与蒸馏水(蒸发)
难度: 困难查看答案及解析
-
把X、Y、Z三种光亮的金属片分别插入稀盐酸中,X、Z表面有气泡产生,Y无变化;再把X插入Z的盐溶液中,X表面无变化,则三种金属活动性顺序为( )
A. Z>X>Y B. Z>Y>X C. X>Y>Z D. X>Z>Y
难度: 简单查看答案及解析
-
下列实验现象描述不正确的是()
A. 细铁丝在氧气里剧烈燃烧,火星四射 B. 一氧化碳燃烧产生蓝色火焰
C. 二氧化碳气体通入无色酚酞溶液,溶液变红色 D. 白磷在空气中自燃产生大量白烟
难度: 简单查看答案及解析
-
在硫酸根离子SO42﹣中S的化合价是( )
A. +4 B. +6 C. +2 D. ﹣2
难度: 中等查看答案及解析
-
从海水(含氯化镁)中提取镁的步骤有:①将含碳酸钙的贝壳制成石灰乳;②在海水中加入石灰乳,沉淀、过滤、洗涤;⑧将沉淀物与盐酸反应,结晶、过滤、干燥;④电解无水氯化镁可得到金属镁.下列有关说法不正确的是( )
A. 此法的优点之一是原料来源丰富
B. 步骤①、②、③的目的是从海水中提取MgCl2
C. 步骤②中沉淀、过滤、洗涤的过程既有物理变化又有化学变化
D. 以上反应中包含了化合反应、分解反应和复分解反应
难度: 中等查看答案及解析
-
如图是表示气体微观粒子的示意图,图中“●”和“○”分别表示不同元素的原子.其中表示纯净物的是()
A.
B.
C.
D.
难度: 中等查看答案及解析
-
下列操作中,不正确的是( )
A. 把氢氧化钠固体放在天平左盘的玻璃器皿中称量
B. 用胶头滴管向试管中滴加液体时,把滴管伸入试管内
C. 在实验室里制取氧气,先检查装置的气密性
D. 浓硫酸沾到皮肤上,要立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液
难度: 简单查看答案及解析
-
下列化学用语与所表述的意义不相符的是()
A. N2——氮气 B. 2H——2个氢元素 C. 2H2O——2个水分子 D. CuO——氧化铜
难度: 简单查看答案及解析
-
水是重要的资源。下列说法正确的是
A.过滤能使硬水转化为软水
B.为防止水污染,应禁止使用化肥和农药
C.活性炭能使海水转化为淡水
D.电解水实验说明水是由氢、氧元素组成的
难度: 中等查看答案及解析
-
“类推”是化学学习过程中常用的思维方法.现有以下类推结果,其中正确的是( )
A. 因为碱溶液呈碱性,所以呈碱性的溶液一定是碱溶液
B. 金属铝与盐酸反应生产AlCl3和H2,所以金属铁与盐酸反应生产FeCl3和H2
C. 因为燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件
D. 因为蜡烛燃烧生成二氧化碳和水,所以蜡烛中一定含有碳元素和氢元素
难度: 简单查看答案及解析
-
将一小块金属钾放在装水的烧杯中能够发生剧烈反应放出大量热,其反应是:2K+2H2O═2X+H2↑( )
A. X是一种氧化物 B. X中只含K,O元素
C. 发生爆炸是氢气燃烧引起的 D. X的相对分子质量为112
难度: 中等查看答案及解析
-
化学与生活密切相关,下列做法不会危害人体健康或不存在安全隐患的是
A. 冬天用燃气热水器洗澡时,门窗紧闭 B. 厨房中燃气泄漏时,迅速打开排气扇
C. 儿童和老年人在医生指导下适量补钙 D. 用工业盐亚硝酸钠(NaNO2)代替食盐烹调
难度: 中等查看答案及解析
-
向一定量的Ba(OH)2溶液中滴加稀H2SO4,下列图象能正确描述对应关系的是
A.
 B.
B. 
C.
 D.
D. 
难度: 困难查看答案及解析
-
粗盐提纯实验的部分操作如下图所示,其中不正确的是( )
A. 取一定量粗盐
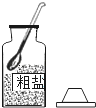 B. 溶解
B. 溶解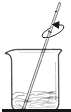
C. 蒸发
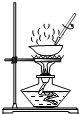 D. 过滤
D. 过滤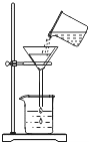
难度: 简单查看答案及解析
-
下列离子在溶液中能大量共存的是( )
A. K+、 Na+、 SO42−、 Cl− B. Na+、 H+、 NO3−、 HCO3−
C. NH4+、 K+、 OH−、 SO42− D. Ag+、 Mg2+、 NO3−、 Cl−
难度: 中等查看答案及解析