-
下列关于营养与健康的说法,不正确的是( )
A. 摄入维生素不足,不会患营养缺乏症
B. 人体内的脂肪储备着丰富的热量
C. 如果蛋白质摄入量不足,会使人生长发育迟缓
D. 低血糖的人会出现乏力、疲倦等症状,需尽快补充葡萄糖
难度: 简单查看答案及解析
-
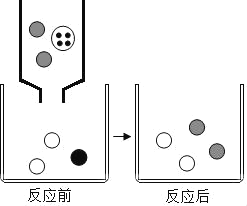
有关C+2CuO
2Cu+CO2↑的反应,说法正确的是( )
A. CuO具有氧化性
B. C发生了还原反应
C. 反应前后元素的化合价没有改变
D. 该反应是化合反应
难度: 中等查看答案及解析
-
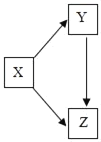
通过一步化学反应实现如图所示的X、Y、Z三种物质间转化,表格中X、Y、Z对应的物质不能实现这种转化的是( )
X
Y
Z
A
CO2
Na2CO3
CaCO3
B
NaNO3
Na2CO3
NaCl
C
HCl
BaCl2
NaCl
D
Mg
MgO
MgCl2
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
甲、乙、丙、丁四种溶液中,分别含有 Ba2+、Mg2+、Na+、H+、OH﹣、Cl﹣、CO32﹣、SO42-中的一种阳离子和一种阴离子,为确定四溶液中分别含有哪种阳离子或阴离子,进行了下面实验:将甲溶液分别与其他三种溶液混合,都观察到白色沉淀生成;将乙、丁溶液混合,有气泡产生;向丙溶液中滴入硝酸银溶液,可明显观察到白色沉淀,加稀硝酸后,沉淀不消失.分析实验得到的以下结论,不正确的是( )
A. 甲溶液中一定含有钡离子
B. 乙溶液中可能含有硫酸根离子
C. 丙溶液中一定含有氯离子
D. 丁溶液中一定含有钠离子
难度: 困难查看答案及解析
-
下列关于水的说法,正确的是( )
A. 活性炭净水器里,活性炭的作用是吸附、并过滤水中的杂质
B. 在自来水厂净水的过程中,发生的变化都是物理变化
C. 天然水中硬水属于混合物,软水属于纯净物
D. 电解水时,与电源负极相连的玻璃管内得到的是氧气
难度: 简单查看答案及解析