-
下列关于某些离子的检验及结论,一定正确的是( )
A. 加入稀盐酸产生无色气体,将该气体通入澄清石灰水中变浑浊,则一定有CO32-
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则一定有SO42-
C. 加入浓烧碱溶液加热,产生的气体能使湿润的红色石蕊试纸变蓝,则一定有NH4+
D. 加入Na2CO3溶液产生白色沉淀,再加盐酸,白色沉淀消失,则一定有Ba2+
难度: 困难查看答案及解析
-
下列有关物质性质与用途具有对应关系的是( )
A. Na2O2吸收CO2产生O2,可用作呼吸面具供氧剂
B. ClO2具有还原性,可用于自来水的杀菌消毒
C. SiO2硬度大,可用于制造光导纤维
D. NH3易溶于水,可用作制冷剂
难度: 中等查看答案及解析
-
古丝绸之路贸易中的下列商品,主要成分属于无机物的是



A.瓷器
B.丝绸
C.茶叶
D.中草药
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
化学在人类生活中扮演着重要角色,以下应用正确的是
A. 用浸泡过高锰酸钾溶液的硅土吸收水果释放的乙烯,可达到水果保鲜的目的
B. 为改善食物的色、香、味并防止变质,可在其中加入大最食品添加剂
C. 使用无磷洗衣粉,可彻底解决水体富营养化问题
D. 天然药物无任何副作用,可长期服用
难度: 中等查看答案及解析
-
对下列化学用语的理解正确的是 ( )
A. 原子结构示意图
可以表示12C,也可以表示14C
B. 比例模型
 可以表示二氧化碳分子,也可以表示水分子
可以表示二氧化碳分子,也可以表示水分子C. 电子式
可以表示羟基,也可以表示氢氧根离子
D. 分子式C2H4O2可以表示乙酸,也可以表示乙二醇
难度: 困难查看答案及解析
-
NA为阿伏加德罗常数,下列叙述错误的是
A.18gH2O中含有的质子数为10NA
B.常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA
C.46g NO2和N2O4混合气体中含有原子总数为3NA
D.1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
难度: 中等查看答案及解析
-
下列过程中,共价键被破坏的是( )
A. 碘晶体升华 B. 溴蒸气被木炭吸附
C. 酒精溶于水 D. HCl气体溶于水
难度: 简单查看答案及解析
-
据国外媒体报道,“火星快车”号和“金星快车”号探测器日前分别在火星和金星大气层中发现了一种非常特殊的气态化合物。这种化合物的存在不但会导致金星上的温室效应被成倍的放大,而且可能会在火星上也诱发温室效应的产生。它的结构式为:16O=C=18O。下列说法正确的是( )
A16O与18O为同种核素
B16O=C=18O与16O=C=16O互为同位素
C16O=C=18O的化学性质与16O=C=16O几乎相同
D 用16O=C=18O与Na216O2反应生成的氧气中含18O
难度: 简单查看答案及解析
-
下列关于元素周期表的说法正确的是
A. 第IA族的所有元素都是金属元素
B. 稀有气体元素原子的最外层电子数均为8
C. 同周期主族元素中,第ⅦA族元素原子半径最小
D. 第 IA族元素金属性强于第ⅡA族元素
难度: 简单查看答案及解析
-
下列反应的离子方程式正确的是
A. 铝片跟氢氧化钠溶液反应:Al+2OH-=AlO2-+H2↑
B. 硫酸镁溶液跟氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓
C. 碳酸钙跟醋酸反应:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑
D. 铜片跟稀硝酸反应:Cu+NO3-+4H+=Cu2++NO↑+2H2O
难度: 简单查看答案及解析
-
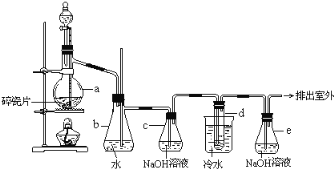
下列各图均为检查装置气密性的方法,根据实验现象判断,其中漏气的是( )
A.
 B.
B. 
C.
 D.
D. 
难度: 中等查看答案及解析
-
对可逆反应4NH3(g)+ 5O2(g)
4NO(g)+ 6H2O(g),下列叙述正确的是
A. 达到化学平衡时,4υ正(O2)= 5υ逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态
C. 达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大
D. 化学反应速率关系是:2υ正(NH3)= 3υ正(H2O)
难度: 中等查看答案及解析
-
某两种气态烃组成的混合物,取其2.24L(标准状况下)充分燃烧,得到0.16mol二氧化碳气体和3.6g液态水。据此判断下列分析中不正确的是( )
A. 此气体中一定含有甲烷
B. 此混合气体中可能含有乙烷
C. 此混合气体中一定不含有丙烷
D. 此气体若是乙烯与甲烷的混合气体,则甲烷与乙烯的体积比为2∶3
难度: 中等查看答案及解析