-
根据下列元素和根的化合价,写出符合要求的物质的化学式
4
(1)一种酸________
(2)一种难溶于水的碱________
(3)一种易溶于水的盐________.难度: 中等查看答案及解析
-
甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
(1)25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为________g.
(2)要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是________.
(3)现有操作步骤:a.溶解 b.过滤 c.降温结晶d.加热浓缩;若甲固体中含有少量乙,则提纯甲的操作步骤是________(填字母序号).
(4)将35℃时丙的饱和溶液降温到25℃,则其溶液的溶质质量分数________(填“变大”、“变小”或“不变”).
(5)向100g35℃的水中加入45g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出.你认为“全部溶解”的原因可能是________.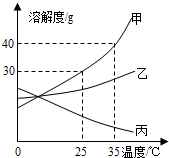
难度: 中等查看答案及解析
-
右图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.
(1)氢氧化钠和盐酸恰好完全反应时,溶液的pH________7(填“大于”或“小于”或“等于”)
(2)根据曲线图判断,该反应是将________(填“氢氧化钠溶液”或“盐酸”,下同)滴入________中,理由是________.
(3)当滴入溶液的体积为5mL时,所得溶液中的溶质为________(写化学式),若在此溶液中滴入石蕊试液,溶液显________色.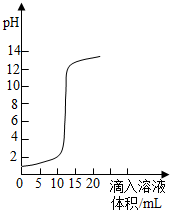
难度: 中等查看答案及解析