-
通过化学变化不可能实现的是
A.由分子生成新分子 B.由离子生成新离子
C.由原子生成新原子 D.由单质生成一种新单质
难度: 中等查看答案及解析
-
化学上用符号“
X”表示原子的组成,其中X代表元素符号,Z表示原子核内的质子数,A表示原子核内质子数与中子数之和。已知
Xn+和
Ym-的核外电子数目相同,则下列关系正确的是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
若用实验证明FeCl3溶液显黄色不是由Cl﹣离子造成的,下列实验无意义的是
A.观察KCl溶液的颜色
B.向FeCl3溶液中滴加适量氢氧化钠溶液振荡后静置,溶液黄色消失
C.向FeCl3溶液中滴加适量无色硝酸银溶液,振荡后静置,溶液黄色未消失
D.加水稀释后FeCl3溶液黄色变浅
难度: 中等查看答案及解析
-
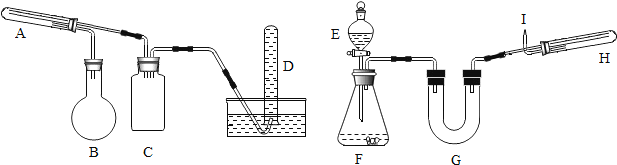
下列对a、b、c、d四套装置中,在注入酸起反应后对气球的变化情况作出正确分析的是( )

A. 气球
不胀大,
都能迅速胀大
B. 气球
逐渐胀大,气球
迅速胀大
C. 气球
逐渐胀大,气球
缓缓膨胀后停止,气球
迅速胀大
D. 以上都不正确
难度: 中等查看答案及解析
-
将CO2通入滴有酚酞的BaCl2、NaOH混合溶液中,出现白色沉淀。下列说法错误的是( )
A. 溶液的红色逐渐变浅或变为无色
B. 产生白色沉淀的化学方程式为:

C. 反应后的溶液中一定有NaCl
D. 反应过程中,溶液里的
、NaOH的质量分数均减小
难度: 中等查看答案及解析
-
将一定量铝粉和氧化铜混合加热,反应的化学方程式为3CuO+2Al
3Cu+A12O3.反应结束后,为了检验氧化铜是否完全反应,取少量反应后的固体,加入足量稀硫酸,充分反应后,将铁片插入溶液中。下列叙述的现象中,能说明氧化铜没有完全反应的是( )
A. 加入稀硫酸后,有气泡生成
B. 加入稀硫酸后,没有气泡生成
C. 加入稀硫酸后,溶液中有红色不溶物质
D. 插入溶液中的铁片表面有红色物质析出
难度: 困难查看答案及解析
-
如图所示,将气体X和气体Y同时通入液体Z,最终一定能看到液体变浑浊的是( )
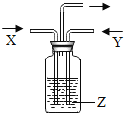
X
Y
Z
A
H2
N2
水
B
HCl
CO2
石灰水
C
CO2
O2
烧碱溶液
D
HCl
O2
硝酸银溶液
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列三组物质混合后 一定有沉淀生成的为
A. 氢气、氮气、水
B. 氯化氢气体、二氧化碳气体、水
C. 二氧化碳、烧碱、氧气
D. 硝酸银、稀盐酸、水
难度: 困难查看答案及解析
-
在相同温度,相同压强的条件下,气体体积之比等于气体所含分子个数之比。某混合气体中可能含有N2,CO,HCl,将其依次通过KHCO3溶液和灼热的CuO,气体体积无变化,但有红色物质生成(设各步反应均充分),再通过足量的NaOH溶液,气体体积明显减少,将燃着的木条伸入盛有剩余气体的集气瓶中,木条熄灭。则可推断该混合气体中
A.一定有N2和CO,肯定无HCl B. 一定有N2 和CO,可能有HCl
C.一定有 CO, HCl和N2 D.一定有 CO,可能有HCl和N2
难度: 困难查看答案及解析
-
工业用CaO 和硝酸反应制Ca(NO3)2·4H2O 晶体,为确保制备过程既不补充水分,又无水剩余,则应选用的硝酸质量分数
A. 30% B. 63% C. 70% D. 84%
难度: 中等查看答案及解析
-
高温加热碳和氧化铜的混合物,恰好完全反应生成铜和二氧化碳,下列有关物质的质量与反应时间的关系中正确的是( )
A.
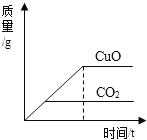 B.
B. 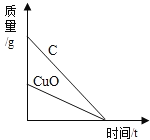
C.
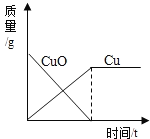 D.
D. 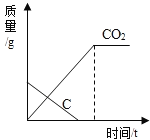
难度: 困难查看答案及解析