-
如果把厨房中的①食盐、②料酒、③豆油、④白糖、⑤面粉、⑥面酱分别放入水中充分搅拌,能够得到溶液的是( )
A. ①②④
B. ①②⑥
C. ④⑤⑥
D. ③⑤⑥
难度: 简单查看答案及解析
-
下列反应完毕后的混合物不是溶液的是( )
A. 二氧化碳与澄清石灰水恰好完全反应
B. 纯净的碳酸钙粉末与足量的稀盐酸反应
C. 锌粒与足量的稀硫酸反应
D. 二氧化碳通入足量的水中
难度: 中等查看答案及解析
-
下列叙述中,属于金属化学性质的是
A. 纯铁是银白色固体
B. 铝在空气中易与氧气反应生成致密的氧化膜
C. 铜容易传热、导电
D. 钨有很高的熔点
难度: 中等查看答案及解析
-
有机合成材料的出现是材料史上的重大突破,下列物质属于有机合成材料的是( )
A.羊毛 B.棉花 C.塑料 D.天然橡胶
难度: 简单查看答案及解析
-
往AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后,有金属析出,过滤、洗涤后往滤渣中加入稀盐酸,有无色气体放出,则滤液中一定存在的物质是( )
A. AgNO3、Cu(NO3)2、Fe(NO3)2
B. Cu(NO3)2、Fe(NO3)2
C. Fe(NO3)2
D. AgNO3、Fe(NO3)2
难度: 简单查看答案及解析
-
神州十号飞船在2013年夏天与“天宫一号”交会对接。其中用于制作飞船自展天线的是被人们称为“形状记忆合金”的镍钛合金。对于此天线制作材料的描述错误的是
A. 具有形状记忆功能
B. 具有极低的熔点
C. 具有良好的延展性
D. 具有良好的导电性
难度: 简单查看答案及解析
-
金属R与CuCl2溶液反应的化学方程式为R+CuCl2===RCl2+Cu,则下列说法错误的是( )
A. 该反应是置换反应
B. 金属R可能是铝
C. 金属R活动性比Cu强
D. 该反应前后R的化合价发生了改变
难度: 困难查看答案及解析
-
工业上用Mg(NO3 )2作为浓缩HNO3的吸水剂,向m1g溶质质量分数为65%的硝酸溶液中加人m2g溶质质量分数为72 %的Mg (NO,)2溶液,蒸馏,分别得到97.5%硝酸溶液和60%硝酸镁溶液,若蒸馏过程中,硝酸、硝酸镁和水均无损耗,则投料质量比m1/m2为
A.0.3 B.0.4 C.0.5 D.0.6
难度: 中等查看答案及解析
-
化学肥料和农药对农业的高产丰收具有重要作用。下列有关说法错误的是( )
A.KNO3 是复合肥料
B.残留农药可通过农作物转移到人体中
C.熟石灰可用于改良酸性土壤
D.化肥能提高粮食产量,施用越多越好
难度: 中等查看答案及解析
-
在某无色溶液中能大量共存的是
A. K+、Cu2+、
、
B. Na+、H+、CO32-、
C. Ba2+、
、OH-、
D. Ba2+、K+、
、OH-
难度: 中等查看答案及解析
-
如图所示,托盘天平两边各放了一只盛有足量等质量、等质量分数稀硫酸的小烧杯,向左右两边分别加入等质量的不同的金属,实验开始后发现左边先下沉,一段时间后右边下沉。符合这一现象的组合是(前面的放左盘,后面的放右盘)
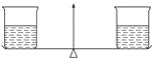
A. 铁、锌
B. 铁、铜
C. 锌、铁
D. 镁、铁
难度: 中等查看答案及解析
-
下列实验中利用提供的方案不能达到目的的是
选项
实验目的
实验方案
A
除去铁粉中混有的少量银粉
用足量稀盐酸溶解后过滤
B
鉴别纯羊毛织品和涤纶织品
取样灼烧后闻气味
C
证明分子在不断运动
将一滴红墨水滴入一杯纯净水中
D
收集二氧化碳时,检验集气瓶是否集满
用一根燃着的木条放在集气瓶口
难度: 中等查看答案及解析
-
下列属于合金的是
A. 铁粉和铜粉混
B. 黄铜
C. 铁
D. 氧化铁
难度: 简单查看答案及解析
-
微量元素在人体内的质量总和不到人体质量的千分之一,但这些元素对人体的正常发育和健康起着重要作用。下列各元素全部属于人体中微量元素的是
A. Na、Cl、O
B. H、O、N
C. N、Ca、C
D. I、Fe、Zn
难度: 简单查看答案及解析
-
利用能源、节约能源是我们大家共同关注的社会问题。下列属于节能图标的是
A.

B.

C.

D.

难度: 简单查看答案及解析
-
下列物质与足量稀硫酸反应后,能得到无色、透明的溶液的是
A. CuO
B. Fe(OH)3
C. Fe2O3
D. Na2CO3
难度: 中等查看答案及解析
-
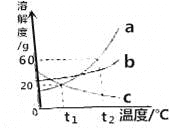
向下表的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系,能用下图曲线表示的是
序号
甲
乙
①
HNO3和Mg(NO3)2的混合溶液
KOH溶液
②
Ag-Zn合金
稀H2SO4
③
久置空气中的铝片
稀盐酸
④
含有Na2CO3的NaOH溶液
稀HNO3
⑤
HCl和H2SO4的混合酸
Ba(NO3)2溶液

A. ②⑤
B. ①③④
C. ①②④
D. ①③⑤
难度: 中等查看答案及解析
-
化学实验操作中常常有许多“先后”之分,否则就会出现事故或者使实验失败。下列实验操作的先后顺序正确的是
A. 稀释浓硫酸先加水,后加酸
B. 炼铁时先加热,后通CO,节约药品
C. 实验室制取二氧化碳时,先加稀盐酸,后加石灰石
D. 排水法收集氧气,先熄灭酒精灯,后移出导气管
难度: 中等查看答案及解析
-
在铁制品上连接比铁活泼的金属是防止铁生锈的方法之一。下列金属中,可行的是
A. 银
B. 金
C. 铜
D. 锌
难度: 简单查看答案及解析
-
用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少?
难度: 困难查看答案及解析