-
随着城市的发展,汽车的拥有量越来越多,城市道路经常出现拥堵现象,于是人们改用骑自行车出行,既体现了健康的生活方式又体现了绿色环保,下列有关说法正确的是( )

A. 自行车车架用锰钢制造,具有韧性好、硬度大的优点
B. 自行车有些部件用铝合金制成,铝合金具有密度小、熔点高、抗腐蚀性的好的性质
C. 自行车链条是用喷漆来进行防锈
D. 自行车整体都是由金属材料制成
难度: 中等查看答案及解析
-
下列实验操作正确的是( )
A.
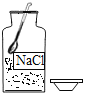 取用固体药品 B.
取用固体药品 B. 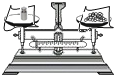 称量药品质量
称量药品质量C.
液体的量取 D.
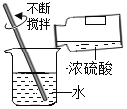 稀释浓硫酸
稀释浓硫酸难度: 简单查看答案及解析
-
下列物质的用途错误的是( )

A. 用黄铜制作马踏飞燕 B. 用钛合金制人造骨
C. 用硫酸作汽车铅酸蓄电池 D. 用盐酸制药
难度: 中等查看答案及解析
-
下列生活中的做法正确的是( )
A. 如果不慎将浓硫酸沾在皮肤或衣服上,应立即用大量的水冲洗,然后再涂上3%—5%的氢氧化钠溶液
B. 向鱼缸中通入空气,可以增加水中含氧量
C. 用硫酸铜和氢氧化钠加水配制农业上的杀菌剂波尔多液
D. 用硫酸长时间浸泡生锈的铁制品,从而达到较好的除锈效果
难度: 中等查看答案及解析
-
下列实验现象记录正确的是( )
A. 把一根铁钉放入足量的稀盐酸中,固体表面产生气泡,固体逐渐减少至消失,放热,溶液由无色变为浅绿色
B. 一氧化碳通入氧化铁中加热,红棕色固态逐渐变成银白色,澄清石灰水变白色浑浊
C. 向氢氧化镁中加入几滴无色酚酞溶液,无色酚酞溶液变红
D. 浓盐酸打开瓶盖冒白雾
难度: 中等查看答案及解析
-
下列应用的原理、化学方程式及基本反应类型表示均正确的是( )
A. 铝有很好的抗腐蚀性能:4Al + 3O2 △ 2Al2O3 化合反应
B. 用氢氧化铝治疗胃酸过多症:2Al(OH)3 + 6HCl = 2AlCl3 + 6H2O 复分解反应
C. 用盐酸除铁锈:Fe2O3 + 6HCl = 2FeCl3 + 3H2O 复分解反应
D. 比较铜和镁的活动性顺序:Cu + MgSO2 = Cu + MgSO4 置换反应
难度: 困难查看答案及解析
-
下列叙述正确的是( )
A. 某无色溶液中加入几滴无色酚酞溶液变红,该溶液一定是碱溶液
B. 取牵牛花在研钵中捣烂,加入水浸泡,可制得指示剂
C. 硫酸是重要的化工原料,用于生产化肥、农药、火药等
D. 同一种溶质的饱和溶液,其溶质的质量分数一定比不饱和溶液的溶质质量分数大
难度: 困难查看答案及解析
-
葡萄糖存在与葡萄糖汁和其他带甜味的水果里,是一种重要的营养物质,是人类生命活动所需能量的重要来源之一。下列关于葡萄糖的说法错误的是( )

A. 葡萄糖分子中C、H、O三种元素的原子个数比为1 :2 :1
B. 一个葡萄糖分子中含有6个碳原子、12个氢原子和6个氧原子
C. 葡萄糖分子中氢元素的质量分数最小
D. 葡萄糖是由多原子分子构成的化合物
难度: 困难查看答案及解析
-
下列关于资源和能源的叙述中正确的是( )
A. 目前已制得的纯金属只有90余种,合金已达几百种
B. 海洋是巨大的资源宝库,海水中含有80多种元素
C. 现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量的40%以上
D. 地壳中含量最多的金属元素及目前世界年产量最高的金属都是铁
难度: 中等查看答案及解析
-
对下列事实的微观解释错误的是( )
选项
亊实
解释
A
溶液导电的原因
溶液中有自由移动的粒子
B
酸有相似的化学性质
酸溶液中有相同的氢离子
C
硫酸亚铁溶液和硫酸铁溶液颜色不同
溶液中的阳离子不同
D
碱溶液能使紫色石蕊溶液变蓝
碱溶液中含有氢氧根离子
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
实验室区分下列各组物质的两种方法都合理的是( )
选项
待区分物质
方法一
方法二
A
生铁和钢
用磁铁吸引
加稀盐酸
B
浓硫酸和浓盐酸
尝味道
打开瓶盖闻气味
C
氢氧化钠和硝酸铵
加入水中观察
观察颜色
D
氧化铜和氧化铁
观察颜色
加入足量的稀盐酸
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
甲、乙两种固体物质(均不含结晶水)溶解度曲线如图所示,下列说法正确的是( )
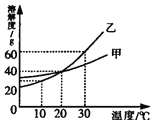
A. 30℃时,甲、乙两物质的饱和溶液降到20℃,所得溶液的溶质质量分数甲大于乙
B. 20℃时,等质量的甲、乙溶液蒸发等质量的水,析出晶体的质量一定相等
C. 把100g溶质质量分数为10%的乙溶液从30℃降温到10℃其质量分数减小
D. 10℃时,向50g水中加入乙可得65饱和溶液,则乙在该温度下的溶解度为30g
难度: 困难查看答案及解析
-
除去下列物质中的少量杂质.所用试剂和操作方法都正确的是( )
选项
物质
杂质
试剂和操作方法
A
CO2
CO
点燃
B
NH3
H2O
通过足量的浓硫酸
C
CuSO4溶液
H2SO4
加入过量的氧化铜,过滤
D
FeSO4溶液
ZnSO4
加入过量的镁粉,过滤
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
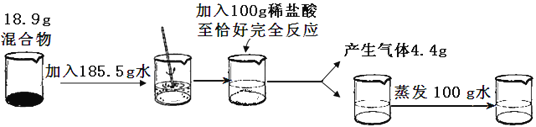
某赤铁矿石样品160g与75g含碳36%的一氧化碳和二氧化碳的混合物恰好完全反应,则该赤铁矿石的纯度为( )
A. 40% B. 50% C. 60% D. 80%
难度: 困难查看答案及解析