-
金属材料在现实生活中有极为重要的作用.下列金属材料的运用与金属所具有的性质不一致的是( )
A. 制造白炽灯灯丝——熔点高
B. 制造飞机——坚硬而质轻
C. 制造装化工原料的容器——耐腐蚀
D. 制造保险丝——硬度大
难度: 中等查看答案及解析
-
调味剂是重要的食品添加剂,将下列调味剂加入水中,不能形成溶液的是( )
A. 食盐 B. 蔗糖 C. 味精 D. 芝麻油
难度: 简单查看答案及解析
-
下列物质属于合成橡胶制品的是( )
A. 茶壶 B. 易拉罐 C. 不粘锅 D. 汽车轮胎
难度: 简单查看答案及解析
-
2013年12月2日,“嫦娥三号”宇宙飞船成功登月,并将“玉兔号”月球车永远留在了月球。月球车大量使用了新材料“铝锂合金”,使其能轻便运行,为科学实验提供有力的保障。下列关于合金的说法中正确的是( )
A. 合金不属于金属材料
B. 合金的硬度一般比各成分金属大
C. 合金属于金属单质
D. 多数合金的熔点高于组成它的成分金属
难度: 简单查看答案及解析
-
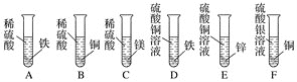
社会上一些不法分子以铜锌合金(金黄色,俗称黄铜)假冒黄金进行诈骗活动。为了鉴别黄铜和黄金,以下方法可行的是( )
A. 观察颜色
B. 称量质量
C. 加稀硫酸
D. 磁铁吸引
难度: 简单查看答案及解析
-
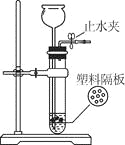
某电镀厂的电镀液中含有金盐,为了回收其中的金元素,技术人员制作了如图的“吸金球”,“吸金球”是装入一些“吸金”物质的纱袋,把“吸金球”浸入电镀液,能“吸”出盐溶液中的金,据上所述,“吸金球”中的“吸金”物质可能是( )

A.活性炭(C) B.磁石(主要成分是Fe3O4)
C.铁屑(Fe) D.胆矾(CuSO4•5H2O)
难度: 简单查看答案及解析
-
将等质量的镁和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是( )

A. 反应结束后镁一定有剩余
B. 反应消耗盐酸的总质量一定相等
C. O—t1时段,产生氢气的质量镁比铁大
D. O—t2时段,参加反应的镁的质量与铁相等
难度: 中等查看答案及解析
-
生产生活中下列做法,正确的是( )
A.为解决“白色污染”问题,应将废旧塑料袋焚烧处理
B.降低新装修房屋内的甲醛含量,最好的方法是紧闭门窗并在房间内放一盆水
C.为提高农作物产量并减少对环境的污染,应合理使用农药和化肥
D.提倡节日大量燃放烟花爆竹,增加喜庆气氛
难度: 简单查看答案及解析
-
有关人体的组成元素的说法中错误的是( )
A. 组成人体自身的元素约有50多种
B. 人体内的碳、氢、氧、氮四种元素主要以水、糖类、油脂、蛋白质和维生素形式存在
C. 人体内含量较多的元素有11种
D. 由于微量元素的含量非常少,因此,对人体健康的影响也很小
难度: 简单查看答案及解析
-
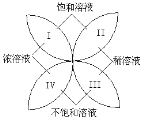
如图是a、b、c三种物质的溶解度曲线。由图示判断下列说法中不正确的是()

A. c的溶解度随温度的升高而减小
B. 在t2℃时,a、b两溶液中的溶质的质量分数相等
C. a的饱和溶液从t2℃降温至t1℃时仍为饱和溶液
D. t1℃时,a的饱和溶液60g中含有溶剂50g
难度: 简单查看答案及解析
-
电影《黄金大劫案》上映后,里面用“王水”(浓盐酸与浓硝酸的混合液)溶解黄金的情引起了广泛的热议。黄金溶解在“王水”中形成HAuCl4(四氯合金酸),没有氢气产生。根据以上信息,下列有关说法正确的是( )
①“王水”溶解黄金是化学变化;②金比氢活泼;③HAuCl4中,Au的化合价为+3价;④“王水”可以用铁质容器盛装。
A. ①④ B. ①②③ C. ③④ D. ①③
难度: 中等查看答案及解析
-
人们对事物的认识常需经历一个不断修正和完善的过程,如对酸的认识就是如此。下列各项是不同时期对酸的认识,其中与我们现在所学酸的定义最相近的是
A. 有酸味的物质 B. 只有氢才是酸不可缺少的元素
C. 一切酸中都含有氧 D. 与碱作用时失去原有性质的物质
难度: 中等查看答案及解析
-
表中列出几种物质的熔点,据此判断以下说法正确的是()
物质名称
汞
金
铜
铁
钨
氧
熔点/℃
-38.8
1064
1083
1535
3410
-218
A. 铜球掉入铁水中不会熔化
B. 在-220℃时,氧呈液态
C. 水银温度计可测量-40℃的温度
D. 用钨制成的灯丝不易熔化
难度: 简单查看答案及解析
-
下列建设地铁过程中使用的材料属于合金的是()
A. 锰钢
B. 水泥
C. 玻璃
D. 塑料
难度: 简单查看答案及解析
-
下列关于“生活中的化学”的叙述中,不正确的是
A. 胃酸过多可服用适量的小苏打
B. 纯碱可除去热水瓶中的水垢
C. 食用加碘食盐可预防甲状腺肿大
D. 白醋可除去白衬衫上的铁锈
难度: 简单查看答案及解析
-
甲、乙两物质的溶解度曲线如图所示,下列说法不正确的是( )

A.t1℃时,甲和乙的溶解度相等
B.甲和乙的溶解度都随温度的升高而增大
C.t1℃时,甲和乙各30g分别加入90g水中,均能完全溶解
D.t2℃时,在100g水中放入60g甲,形成饱和溶液
难度: 简单查看答案及解析
-
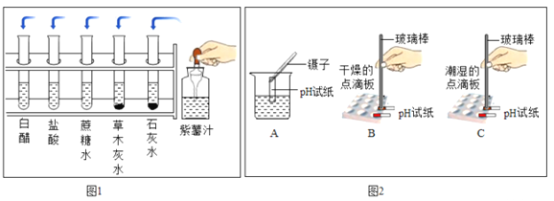
下列实验能达到实验目的是( )
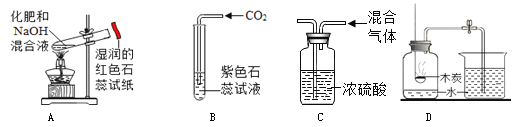
A. 鉴别两种化肥NH4Cl和KNO3 B. 检验二氧化碳
C. 除去氧气中的水蒸气 D. 探究空气中氧气的含量
难度: 中等查看答案及解析
-
科学家提出“硅是未来的石油”,制备粗硅的反应为SiO2+2C
Si+nCO↑,下列说法正确的是()
A. 该反应为置换反应
B. 该化学方程式中n=1
C. 反应前后原子总数发生变化
D. 硅是地壳中含量最高的元素
难度: 简单查看答案及解析
-
向氯化铜、氯化锌、盐酸的混合液中加入过量的铁粉,充分反应后,溶液中一定含有的物质( )
A. 氯化锌、盐酸
B. 氯化亚铁、氯化铜
C. 氯化铜、盐酸
D. 氯化锌、氯化亚铁
难度: 简单查看答案及解析