-
施用钾肥能增强农作物的抗倒伏能力。下列物质可用作钾肥的是
A. NH4HCO3 B. K2CO3 C. CO(NH2)2 D. Ca(H2PO4)2
难度: 简单查看答案及解析
-
2013年12月2日,“嫦娥三号”宇宙飞船成功登月,并将“玉兔号”月球车永远留在了月球。月球车大量使用了新材料“铝锂合金”,使其能轻便运行,为科学实验提供有力的保障。下列关于合金的说法中正确的是( )
A. 合金不属于金属材料
B. 合金的硬度一般比各成分金属大
C. 合金属于金属单质
D. 多数合金的熔点高于组成它的成分金属
难度: 简单查看答案及解析
-
食品与卫生、健康密切相关。下列做法符合食品安全要求的是
A.用硫磺燃烧产生的二氧化硫熏制笋干、银耳等 B.用碳酸氢钠焙制糕点
C.在果汁中加入“塑化剂”使其口感更佳 D.用工业石蜡抛光水果、瓜子
难度: 中等查看答案及解析
-
金属在人类生活和生产中有着非常广泛、重要的用途,下列关于金属的描述中正确的是( )
A. 烹制食物用铁锅是因为铁的密度大
B. 导线常用铜制是因为铜的导电性好
C. 铝是地壳中含量最多的元素
D. 钙是生活生产中使用最多的金属
难度: 简单查看答案及解析
-
食品安全是人类健康永恒的话题,下列做法正确的是
A.用甲醛溶液浸泡海产品 B.烹调食物时不能用亚硝酸钠代替食盐
C.霉变的大米用水清洗后可以食用 D.油炸食品要常吃,以补充能量
难度: 中等查看答案及解析
-
锡(Sn)是五金之一,它的金属活动性顺序位于铁和铜之间,则下列反应不会发生的是( )
A. Zn+Sn(NO3)2===Zn(NO3)2+Sn
B. Sn+2HCl===SnCl2+H2↑
C. Sn+2AgNO3===Sn(NO3)2+2Ag
D. Sn+MgSO4===SnSO4+Mg
难度: 中等查看答案及解析
-
用实验比较铜、锌、银的金属活动性,最好的方法是选用下列试剂中的( )
A. ZnSO4溶液
B. NaOH溶液
C. 稀硫酸
D. CuSO4溶液
难度: 中等查看答案及解析
-
中学生需要摄入足够的钙促进骨骼的生长。因此最好多食用的食物是( )
A. 米饭

B. 菠菜

C. 豆制品和奶制品

D. 麻辣烫

难度: 简单查看答案及解析
-
今年“世界环境日”的主题是“提高你的呼声,而不是海平面”,海平面上升的主要原因是由于温室效应导致的全球气候变暖。下列获取电能的途径会加剧温室效应的是()
A.火力发电 B.水力发电 C.风力发电 D.核能发电
难度: 简单查看答案及解析
-
化学中常常出现“1+1≠2”的有趣现象,但也有例外。下列符合“1+1=2”的事实是
A. 10L水与10L酒精混合后的体积等于20L
B. 10g硫粉在10g氧气中完全燃烧后生成20g二氧化硫
C. 10g锌片与10g稀硫酸充分反应后所得的溶液质量为20g
D. 25℃,10g氯化钠饱和溶液中加入10g氯化钠固体能得到20g氯化钠溶液
难度: 中等查看答案及解析
-
镁条在空气中燃烧时,可观察到的现象是( )
A. 发出蓝色火焰
B. 发出耀眼的白光
C. 发出黄色火焰
D. 剧烈燃烧,火星四射
难度: 简单查看答案及解析
-
医生建议小明多吃蔬菜,则小明需要补充的营养素主要是( )
A. 蛋白质
B. 油脂
C. 维生素
D. 无机盐
难度: 简单查看答案及解析
-
下列有关浓硫酸的相关实验,其中合理的是( )
序号
实验目的
实验过程
①
稀释浓硫酸
取少量浓硫酸放入烧杯中,缓慢倒入水,并用玻璃棒搅拌
②
证明腐蚀性
取少量浓硫酸,滴在纸张或木片上
③
证明吸水性
取少量浓硫酸,置于空气中一段时间,其溶质质量分数增大
④
除氧气中水分
将混合气体通过盛有浓硫酸的洗气瓶,并用向上排气法收集
A. ②③
B. ①③
C. ②④
D. ①④
难度: 简单查看答案及解析
-
下来生活中的物品主要由有机合成材料制成的是
A.羊毛手套 B.纯棉衬衫 C.真丝围巾 D.尼龙背包
难度: 中等查看答案及解析
-
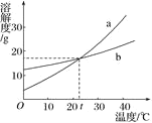
右图是甲、乙、丙三种固体物质的溶解度曲线。下列说法不正确的是( )

A.在t2℃时,甲、乙两种物质的溶解度相等
B.0℃时,将20g甲物质加入50g水中,所得溶液质量为70g
C.t1℃时,将丙的饱和溶液升温至t2℃,有晶体析出
D.在tl℃时,甲的饱和溶溶和丙的饱和溶液中溶质的质量分数相同
难度: 困难查看答案及解析
-
向CuSO4溶液中加入一定质量的铝粉,完全反应后过滤,得滤渣和蓝色滤液。下列说法正确的是( )
A. 向滤渣中滴加稀盐酸,无气泡产生
B. 滤渣中一定有Cu,可能有Al
C. 滤液中只有Al2(SO4)3
D. 滤液中只有CuSO4
难度: 中等查看答案及解析
-
人类使用材料的历史就是人类的进步史,下列物品的主要材质在自然界中以单质形式存在的的是( )
A. 青铜器
B. 铸铁宝剑
C. 黄金首饰
D. 塑料制品
难度: 简单查看答案及解析
-
人类每年从自然界中提取大量的金属铁,下列关于铁的说法正确的是( )
A. 炼铁的过程是把单质铁变成氧化铁
B. 回收利用废旧金属耗费人力物力,不如直接丢弃
C. 铁是地壳中含量最多的金属元素
D. 铁制品锈蚀要及时除锈
难度: 简单查看答案及解析
-
下列关于化肥的说法中,正确的是( )
A. (NH4)2SO4属于复合肥料
B. 从外观即可把NH4NO3与KCl区别开
C. 农作物所必需的营养元素只有氮、磷和钾三种
D. NH4Cl与熟石灰混合有刺激性气味气体放出
难度: 简单查看答案及解析
-
物质性质决定它的用途,还决定了它的保存方法.固体NaOH具有以下性质:
①白色片状固体 ②有腐蚀性 ③易吸收水分而潮解 ④易溶于水,溶解放热 ⑤能与空气中的二氧化碳反应.实验室中必须将它密封保存的主要原因是( )
A. ①② B. ①②③ C. ②③④ D. ③⑤
难度: 中等查看答案及解析