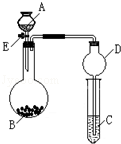
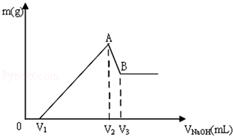
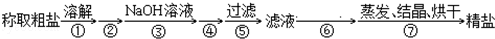-
保护环境,就是关爱自己.下列说法中你认为不正确的是
A.空气质量日报的主要目的是树立人们环保意识,同时也让人们知道了二氧化硫、二氧化氮和可吸入颗粒物是大气主要污染物
B.酸雨属空气污染,是指pH小于7的雨水,主要是人为的向大气中排放大量酸性物质造成的
C.为了减少二氧化硫和二氧化氮的排放,工业废气排放到大气之前必须回收处理
D.氯气是一种黄绿色、有毒气体,但可以用于自来水的杀菌消毒
难度: 简单查看答案及解析
-
下列物质为纯净物的是
A.水泥 B.水玻璃 C.氨水 D.液氯
难度: 简单查看答案及解析
-
2013年3月1日武汉至宜昌高速45辆车因雾连环追尾,事故导致2人不幸死亡,25人受伤,其中重伤2人,汉宜高速封闭近5小时,近千名旅客滞留.雾属于下列分散系中的
A.乳浊液 B.溶液 C.胶体 D.悬浊液
难度: 简单查看答案及解析
-
下列图示的四种实验操作名称从左到右依次是

A.过滤、蒸发、蒸馏、萃取分液 B.过滤、蒸馏、蒸发、萃取分液
C.蒸发、蒸馏、过滤、萃取分液 D.萃取分液、蒸馏、蒸发、过滤
难度: 中等查看答案及解析
-
中国女药学家屠呦呦因发现青蒿素对疟疾的治疗作用而成为2015年诺贝尔生理医学奖获得者,青蒿素的分子式为C15H22O5,它属于有机物,易溶于乙酸、苯,可溶于乙醇、几乎不溶于水,下列说法不正确的是
A.人工合成青蒿素经过了长期的实验研究,实验是化学研究的重要手段
B.从青蒿中提取青蒿素的方法是以萃取原理为基础,萃取是一种物理变化
C.可以用苯把溶解在乙醇中的青蒿素萃取出来,静置分层后,下层为苯的青蒿素溶液
D.现代化学分析测试中,可用元素分析仪确定青蒿素中的C、H、O元素
难度: 中等查看答案及解析
-
下列物质在水溶液中没有漂白作用的是
A.Cl2 B.Na2O2 C.NaOH D.SO2
难度: 简单查看答案及解析
-
NO在人体内起着多方面的重要生理作用.下列关于NO的说法错误的是
A.NO是汽车尾气的有害成分之一
B.NO是红棕色气体
C.在雷雨天可以生成NO
D.NO2与水反应有NO生成
难度: 简单查看答案及解析
-
列叙述正确的是
A.常温常压下,1.5 mol NO2的体积约为33.6 L
B.NaOH的摩尔质量是40 g
C.100 mL水中溶解了8.4 g NaHCO3,则溶液中Na+的物质的量浓度为1 mol/L
D.同温同压下,相同体积的C12和SO2气体所含的分子数一定相同
难度: 中等查看答案及解析
-
在无色透明强酸性溶液中,能大量共存的离子组是
A.K+、Ca2+、HCO3﹣、SO42﹣
B.Cl﹣、NO3﹣、Fe2+、K+
C.Na+、OH﹣、MnO4﹣、Ba2+
D.K+、Mg2+、NO3﹣、SO42﹣
难度: 中等查看答案及解析
-
下列叙述正确的是
A.二氧化硅是酸性氧化物,不与任何酸反应
B.因为CO2通入水玻璃中可制得硅酸,说明碳酸的酸性比硅酸酸性强
C.SiO2是制造光导纤维的材料,SiO2晶体中,每个硅原子与两个氧原子相连
D.工业上制玻璃的主要原料有:黏土、石灰石、石英
难度: 中等查看答案及解析
-
下列叙述中,正确的是
A.氨气喷泉实验说明氨气极易溶解于水
B.NaHCO3的热稳定性比Na2CO3强
C.过量铁粉加入CuCl2溶液中,充分反应后溶液中的阳离子主要是Fe3+
D.氯气中含有的少量氯化氢,可用氢氧化钠溶液除去
难度: 简单查看答案及解析
-
下图所示的实验操作,不能达到相应目的是
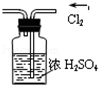
A.干燥Cl2
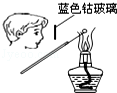
B.检验K2CO3中的K+

C.证明氨气极易溶于水

D.实验室制取氨气
难度: 中等查看答案及解析
-
通过化学实验现象得出相应的结论是探究物质性质的一种重要方法,下列化学实验现象与结论对应完全正确的是
化学实验现象
解释与结论
A
钠与水反应时浮在水面上
钠与水生成的气体托举钠浮在水面上
B
铁与氯气反应剧烈燃烧产生红棕色的烟
产物为红棕色小颗粒,燃烧不一定需要氧气
C
氯水呈黄绿色
氯气与水反应生成了黄绿色物质
D
氢气在氯气中燃烧时瓶口有白雾
氯气逸出结合空气中的水蒸气而呈白雾状
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列离子方程式书写正确的是
A.铁粉跟稀硫酸反应 2Fe+6H+=2Fe3++3H2↑
B.铝跟氢氧化钠溶液反应 2Al+2H2O+2OH﹣=2 AlO2﹣+3H2↑
C.氯气和水的反应 C12+H2O=2H++C1﹣+ClO﹣
D.少量铜屑放入稀硝酸中 Cu+4H++2NO3﹣=Cu2++2NO2↑+2H2O
难度: 中等查看答案及解析
-
在xR2++y H++O2=4R3++n H2O的离子方程式中,下列判断正确的是
A.y=4,R2+是氧化剂
B.y=2,R2+是还原剂
C.y=2,R3+是还原产物
D.y=4,R3+是氧化产物
难度: 中等查看答案及解析
-
将一定质量的Mg、Zn、Al混合物与足量稀H2SO4反应,生成H2 2.24L(标准状况),原混合物的质量可能是
A.1.8 g B.6.5 g C.3 g D.10 g
难度: 困难查看答案及解析
-
以下物质间的每步转化通过一步反应能实现的是
A.Al﹣﹣Al2O3﹣﹣Al(OH)3﹣﹣NaAlO2
B.Fe﹣﹣FeO﹣﹣Fe(OH)2﹣﹣Fe(OH)3
C.S﹣﹣SO3﹣﹣H2SO4﹣﹣MgSO4
D.Na﹣﹣Na2O2﹣﹣Na2CO3﹣﹣NaOH
难度: 中等查看答案及解析