-
推理是一种重要的思维方法,以下推理合理的是
A. 酸中一定含有氢元素,所以含有氢元素的物质一定是酸
B. 置换反应有单质生成,所以有单质生成的反应一定是置换反应
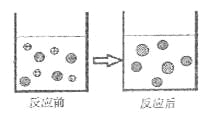
C. 化学反应前后原子总数不变,所以化学反应前后分子总数也不变
D. 化学反应伴随能量变化,所以金属腐蚀过程中一定伴随能量变化
难度: 中等查看答案及解析
-
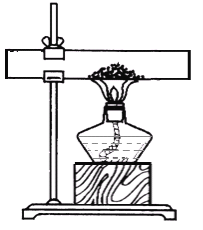
化肥中的氮肥很多是铵盐。已知氨气通入水中后,其溶液呈碱性。将硫酸铵和氢氧化钙混合后放入试管加热,用湿润的红色石蕊试纸放在试管口,湿润红色石蕊试纸会变蓝色,这是检验铵盐的方法。上述实验现象说明( )
A. 铵盐和碱的反应是属于复分解反应类型
B. 氨气比空气轻
C. 能使红色石蕊试纸变蓝色就是氨气
D. 铵盐能和碱反应放出氨气
难度: 简单查看答案及解析
-
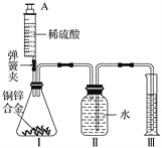
某学生要用实验证明铁、铜、银三种金属的活动性顺序,现有铁片、铜片、硝酸银溶液、稀盐酸四种物质,他设计的下列实验方案中可行的是( )
A. ①Cu+HCl ②Fe+AgNO3 ③Cu+AgNO3
B. ①Fe+HCl ②Cu+HCl ③Fe+AgNO3
C. ①Fe+HCl ②Fe+AgNO3 ③Cu+AgNO3
D. ①Fe+HCl ②Cu+HCl ③Cu+AgNO3
难度: 简单查看答案及解析
-
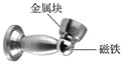
如图是生活中常用来固定房门的“门吸”,它由磁铁和金属块两部分组成。该金属块能被磁铁所吸引,是因为可能含有以下材料中的( )
A. 银
B. 铁
C. 铝
D. 锌
难度: 简单查看答案及解析
-
日常生活中的下列物质中加入紫色石蕊溶液无明显变化的是( )
A. 柠檬汁
B. 苹果汁
C. 纯净水
D. 石灰水
难度: 中等查看答案及解析
-
甲、乙两种固体物质的溶解度曲线如图所示,下列结论正确的是( )
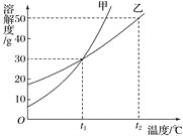
A. 乙的溶解度小于甲的溶解度
B. 甲的溶解度受温度影响比乙大
C. t2℃时,100 g乙的饱和溶液中含乙50 g
D. 相同质量的甲、乙的饱和溶液由t2℃降至t1℃,析出晶体较多的是乙
难度: 中等查看答案及解析
-
一定条件下,下列各组内物质两两混合后都能发生化学反应的一组是( )
A. 氢气、氧化铜、稀盐酸
B. 锌粒、硝酸银溶液、氯化镁溶液
C. 碳酸钠溶液、稀硫酸、澄清石灰水
D. 二氧化碳、氢氧化钠溶液、氯化钾溶液
难度: 简单查看答案及解析
-
下列有关资源的说法错误的是( )
A. 回收利用废旧金属可以减少污染
B. 目前世界上年产量最多、使用最多的金属是铁
C. 地球上的金属资源只广泛存在于地壳中,多数以化合物的形式存在
D. 目前已经广泛用塑料来代替钢和其他金属制造管道、齿轮和汽车零部件等
难度: 简单查看答案及解析
-
食品安全是人类健康永恒的话题,下列做法正确的是
A.用甲醛溶液浸泡海产品 B.烹调食物时不能用亚硝酸钠代替食盐
C.霉变的大米用水清洗后可以食用 D.油炸食品要常吃,以补充能量
难度: 中等查看答案及解析
-
中国海域辽阔,拥有航空母舰保卫祖国海疆一直是中国人的梦想,而建造航母需要大量的金属材料,一种新兴的金属由于其密度小,延展性好,耐腐蚀性强,它和它的合金在航空、航海和化学工业等领域正逐步取代铝和铝合金而被广泛应用,该金属是( )
A. 锌
B. 钛
C. 镁
D. 锰
难度: 简单查看答案及解析
-
了解安全知识,可以更好地保护人身和财产安全。下列做法不正确的是( )
A. 发现燃气泄漏应立即开窗通风关阀门
B. 用亚硝酸钠腌制鱼肉和蔬菜
C. 霉变的大米、瓜子、花生等不能食用
D. 室内起火应压低身体逃离火场
难度: 中等查看答案及解析
-
下列有关事实不能用金属活动性顺序解释的是( )
A. 不能用金属铜与稀硫酸反应制取氢气
B. 银的导电性强于铜
C. 镁和铝与稀盐酸反应的剧烈程度不同
D. 铜能将银从硝酸银溶液中置换出来
难度: 中等查看答案及解析
-
中学生需要摄入足够的钙促进骨骼的生长。因此最好多食用的食物是( )
A. 米饭

B. 菠菜

C. 豆制品和奶制品

D. 麻辣烫

难度: 简单查看答案及解析
-
酸与碱中和生成盐和水,现将20 g 20%的NaOH溶液与20 g 20%的H2SO4溶液充分反应后滴入紫色石蕊溶液,混合物呈现( )
A. 蓝色
B. 紫色
C. 红色
D. 无色
难度: 简单查看答案及解析
-
人们的衣食住行离不开各种材料。下列材料中属于天然有机高分子材料的是( )
A. 不锈钢
B. 水泥
C. 涤纶
D. 羊毛
难度: 简单查看答案及解析
-
下列有关资源的说法错误的是( )
A. 回收利用废旧金属,既可以节约资源,又可以减少污染
B. 地球上含量最多的金属元素是铁
C. 地球上的金属资源广泛存在于地壳和海洋中,大多数以化合物的形式存在
D. 大力开发新能源,合理使用化石燃料
难度: 简单查看答案及解析
-
在高速发展的信息时代,我们要学会获取和辨别信息,下列信息中正确的是
A. 为了提高粮食产量,应大量使用农药、化肥
B. 用甲醛水溶液浸泡海鲜产品来延长食品保质期
C. 锌元素有“智力之花”美称,补锌口服液喝得越多越好
D. 塑料薄膜可用于大棚蔬菜,同时也会造成“白色污染”
难度: 中等查看答案及解析
-
近年来,经过我国科学家的努力,制造出了国产芯片“龙芯一号”和“龙芯二号”,芯片的核心部件是以高纯度的单质硅为原材料制造的。用化学方法制得高纯度硅的反应原理是
,该反应属于( )
A. 化学反应
B. 分解反应
C. 复分解反应
D. 置换反应
难度: 简单查看答案及解析
-
下列有关金属的说法错误的是
A. 铁是地壳中含量最多的金属元素 B. 金属回收利用有利于保护金属资源
C. 喷漆可以防止铁制品生锈 D. 铜做导线利用了其良好的导电性
难度: 简单查看答案及解析
-
下列材料中,属于合成材料的是( )
A.大理石 B.沙子 C.塑料 D.铝合金
难度: 简单查看答案及解析